vysvětlíme, co je iont a jak je tvořen, a některé příklady. Také, co je anion a kation.
¿co je to ion?
V chemii, iont je elektricky nabitý částice, která se skládá z atomu nebo molekuly, které není elektricky neutrální, to znamená, že v jeho ústavu získal nebo ztratil elektrony. Proces, kterým se produkují ionty, se nazývá „ionizace“.
Ionty se může skládat ze dvou nebo více atomů (polyatomic) různého charakteru, nebo jednoho atomu (monoatomic). V každém případě budeme mluvit o kation (nebo kationtů), když je kladně nabitý ion (tzn., že původní neutrální atom nebo molekula přineslo elektrony), a budeme mluvit o anion (nebo aniontů), pokud je záporně nabitých iontů (tj., že původní neutrální atom nebo molekula přijal elektrony).
Další typy iontů jsou také známo, na základě jejich elektrický náboj, známý jako dianions (když jsou přítomny dva záporné náboje), zwitterions (když představují kladný a záporný náboj, které jsou izolované, ale ve stejné sloučeniny, protože to je neutrální), nebo iontové radikály (ionty obrovské reaktivitu a nestabilitu, protože mají volné elektrony). Obecně jsou ionty vysoce reaktivní a mají tendenci se kombinovat s jinými ionty, atomy nebo molekulami elektrostatickými interakcemi.
Ionty hrají nezastupitelnou roli v životě, zejména těch, vápníku, draslíku a sodíku, jejichž význam v tranzitu buněčných membrán a neurotransmiterů, byl intenzivně studován. Porozumění iontům nám navíc umožnilo vyvinout plazmovou technologii a dokonce měřit kvalitu vody na základě iontových solí rozpuštěných v ní.
Viz také: Chemické vazby
Anion
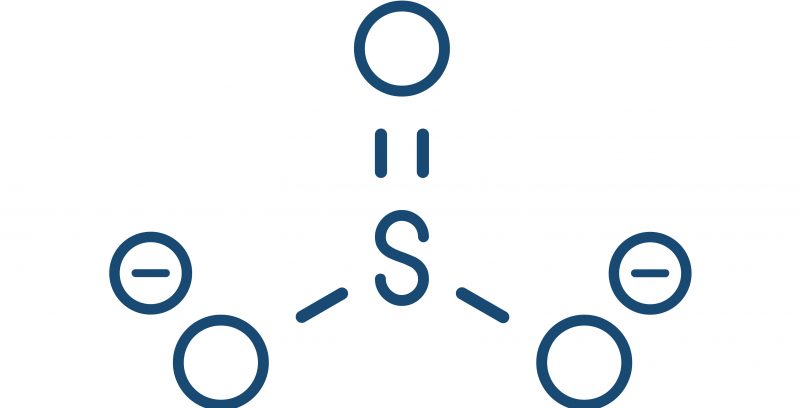
Anion (nebo anionty) je ion, který má negativní elektrický náboj, který je získal elektrony v chemické reakci, která vedla k nim. Mohou se skládat z jednoho nebo několika atomů, ale i ve druhém případě je globální náboj molekuly (její oxidační stav) vždy negativní.
existují tři typy aniontů:
- Monoatomické. Ty, které se skládají z jediného atomu, který získal elektrony. Například: chlorid (Cl -).
- polyatomické. Pocházejí z molekuly, která získala elektrony v chemické reakci, nebo z kyseliny, která ztratila protony. Například: siřičitan (SO32 -).
- kyseliny. Pocházejí z kyseliny polyprotové (která má více ionizovatelných vodíků), ze které byly extrahovány protony. Například: diacid fosfát (H2PO4 -).
kation
kationty jsou ionty, které mají kladný elektrický náboj, to znamená, že ztratily jeden nebo více elektronů. Podobně jako anionty mohou být kationty také složeny z jednoho nebo více atomů za předpokladu, že celkový náboj sloučeniny je v tomto případě kladný.
jednou z nejdůležitějších funkcí kationtů je jejich účast na biologických procesech. Například kationty Na+ a k+ hrají klíčovou roli při přenosu nervových impulzů.
příklady iontů

nejznámější ionty jsou:
- jednoduché kationty. Skládá se z jednoho atomu s kladným nábojem:
- Hliník (Al3+)
- Cesium (Cs+)
- Chromium (III) nebo ion chromová (Cr3+)
- Chromium (VI) nebo ion percrómico (Cr6+)
- Vodíku či protonu (H+)
- Helium nebo alfa částice (He2+)
- Lithium (Li+)
- Železo (II) ion železnatý (Fe2+)
- Železo (III) nebo železitý iont (Fe3+)
- Niklu (III) nebo ion niquélico (Ni3+)
- Tin (II) nebo ion estanoso (Sn2+)
- Cínu (IV) nebo ion estánico (Sn4+)
- Kation polyatomic. Skládá se ze dvou nebo více kladně nabitých atomů:
- Amonný (NH4+)
- Oxonium (H3O+)
- Nitronium (NO2+)
- Mercury (I) nebo rtuti iontů (Hg22+)
- Jednoduché anionty. Skládá se z jednoho atomu s negativním nábojem:
- Azid (N3–)
- Bromid (Br–)
- Karbid (C4-)
- Chlorid (Cl–)
- Fluoridů (F–)
- Fosfid (P3-)
- Nitridu (N3-)
- Sulfid (S2-)
- Oxoaniones. Skládá se z kyslíku a dalších prvků, mají záporný náboj:
- Arsenate (AsO43-)
- Boritanem (BO33-)
- Hipobromito (BrO–)
- Hydrogenuhličitan (HCO3–)
- Chlorečnanů (ClO3–)
- Chlorit (ClO2–)
- Chlornanu (ClO–)
- Dichroman (Cr2O72-)
- Hidrógenosulfato nebo hydrogensíran sodný (HSO4–)
- Hidrógenosulfito nebo bisulfite (HSO3–)
- Silikátové (SiO44-)
- Anionty organických kyselin. Pocházející z organických molekul, mají záporný náboj:
- Acetát (C2H3O2–)
- Oxalát (C2O42-)
- Bioxalate (HC2O4–)
- Ostatní anionty. S negativní náboj a většina z atomu:
- Bisulphide (HS–)
- Amiduro (NH2–)
- Kyanatan (OCN–)
- Thiokyanát (SCN–)
- Kyanid (CN–)
- Hydroxidu sodného (OH–)
Poslední úprava: 12. prosince roku 2020. Jak citovat: „Ion“. Autor: María Estela Raffino. Z: Argentina. Komu: Concepto.de. k dispozici na adrese: https://concepto.de/ion/. Citováno: Březen 26, 2021.