イオンとは何か、それがどのように構成されているか、いくつかの例を説明します。 また、陰イオンと陽イオンとは何ですか。
¿イオンとは何ですか?
化学において、イオンは電気的に中性ではない原子または分子からなる荷電粒子であり、その構成において電子を獲得または失ったものである。 イオンが生成されるプロセスは「イオン化」と呼ばれます。
イオンは、異なる性質の二つ以上の原子(多原子)、または単一の原子(単原子)から構成されていてもよいです。 いずれの場合も、正に帯電したイオンであるとき(すなわち、最初の中性原子または分子が電子をもたらしたとき)に陽イオン(または陽イオン)について話し、負に帯電したイオンであるとき(すなわち、最初の中性原子または分子が電子を受け入れたとき)に陰イオン(または陰イオン)について話す。
他のタイプのイオンも知られており、その電荷に基づいて、二アニオン(二つの負電荷を有する場合)、双性イオン(中性であるために正と負の電荷を有する場合)、イオンラジカル(自由電子を有するために巨大な反応性と不安定性を有するイオン)として知られている。 一般に、イオンは非常に反応性が高く、静電相互作用によって他のイオン、原子または分子と結合する傾向がある。
イオンは生命、特に細胞膜や神経伝達物質の輸送における重要性が広く研究されているカルシウム、カリウム、ナトリウムの重要な役割を果た さらに、イオンを理解することで、プラズマ技術を開発し、その中に溶解したイオン塩に基づいて水質を測定することさえできました。
化学結合
陰イオン
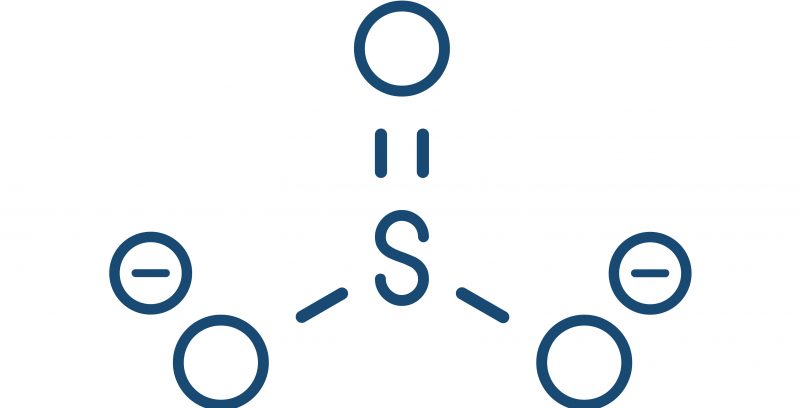
陰イオン(または陰イオン)は、負の電荷を有するイオン、すなわち化学反応で電子を獲得してそれらを生じさせたイオンである。 それらは1つまたはいくつかの原子で構成されていてもよいが、後者の場合でさえ、分子の大域的電荷(その酸化状態)は常に負である。
アニオンには三つのタイプがあります:
- 単原子 電子を獲得した単一の原子で構成されているもの。 例えば、塩化物(Cl-)。
- それらは、化学反応で電子を獲得した分子、または陽子を失った酸から来ます。 例えば:亜硫酸塩(SO32-)。
- それらは、プロトンが抽出されたポリプロチン酸(複数のイオン化可能な水素を有する)から来る。 例えば:二酸の隣酸塩(H2PO4-)。
陽イオン
陽イオンは、正の電荷を持つイオン、つまり1つ以上の電子を失ったイオンです。 したがって、アニオンのように、カチオンはまた、化合物の全電荷が、この場合には、正であることを条件として、一つ以上の原子から構成することがで
陽イオンの最も重要な機能の1つは、生物学的プロセスへの関与です。 例えば、Na+およびK+陽イオンは、神経インパルスの伝達において重要な役割を果たす。
イオンの例

最もよく知られているイオンは次のとおりです:
- 単純な陽イオン。
- アルミニウム(Al3+)
- セシウム(Cs+)
- クロム(III)またはイオンクロム(Cr3+)
- クロム(VI)またはイオン過クロム(Cr6+)
- 水素またはプロトン(H+)
- ヘリウムまたはアルファ粒子(he2+)
- リチウム(Li+)
- 鉄(Ii)イオン鉄(Fe2+)
- 鉄(Iii)または鉄イオン(Fe3+)
- ニッケル(iii)またはイオンNiquélico(Ni3+)
- 錫(Ii)またはイオンestanoso(sn2+)
- 錫(Iv)またはイオンエスタニコ(Sn4)
- 錫(Iv)またはイオンエスタニコ(Sn4)
+)
- アンモニウム(NH4+)
- オキソニウム(H3O+)
- ニトロニウム(NO2+)
- 水銀(I)または水銀イオン(Hg22)
- 水銀(I)または水銀イオン(Hg22)
- 水銀(I)または水銀イオン(Hg22)
- 水銀(I)または水銀イオン(Hg22)
- +)
- アジド(N3–)
- 臭化物(Br–)
- 炭化物(C4-)
- 塩化物(Cl–)
- フッ化物(F–)
- リン化物(P3-)
- ヒ酸塩(Aso43-)
- ホウ酸塩(BO33-)
- ヒポブロミト(BrO–)
- 重炭酸塩(HCO3–)
- 塩素酸塩(Clo3–)
- 亜塩素酸塩(Clo2–)
- ホウ酸塩(Bo33–)
- ホウ酸塩(Bo33-)
- ホウ酸塩(Bo33–)
- 重炭酸塩(HCO3–)
- 塩素酸塩(Clo2-)
- 次亜塩素酸塩(clo-)
- 重クロム酸塩(Cr2O72-)
- ヒドロゲノスルフィートまたは重硫酸塩(Hso4-)
- ヒドロゲノスルフィートまたは重硫酸塩(hso3-)
- ケイ酸塩(Sio44-)
- 酢酸塩(C2H3O2–)
- シュウ酸塩(C2O42-)
- バイオキサレート(HC2O4–)
- 重硫化物(HS–)
- アミドロ(NH2–)
- シアン酸塩(OCN–)
- チオシアン酸塩(SCN–)
- シアン酸塩(CN–)
- 水酸化物(OH)
- 水酸化物(OH)
- 水酸化物(OH)
- 水酸化物(OH)
- 水酸化物(OH)
- 水酸化物(OH)
- 水酸化物(OH)
- –)
最後の編集:2020年12月12日。 どのように引用する:”イオン”。 著者:マリア-エステラ-ラフィーノ アルゼンチン出身。 へ:Concepto.dehttps://concepto.de/ion/ 取得:月26、2021。