Découvrir les causes sous-jacentes de la kératopathie de bande (BK) n’est en aucun cas une tâche simple, mais c’est quelque chose que chaque optométriste est équipé pour gérer. Le processus nécessite une approche globale pour recueillir les antécédents du patient et utiliser des techniques de test. En plus de cela, le clinicien qualifié est responsable de décider si — et quand — traiter. Si le cas l’exige, l’OD peut souvent traiter de manière non invasive en ambulatoire à la lampe à fente.
Cet article fournit un aperçu détaillé de chaque étape du traitement d’un patient BK, de la présentation à la prise en charge chirurgicale.
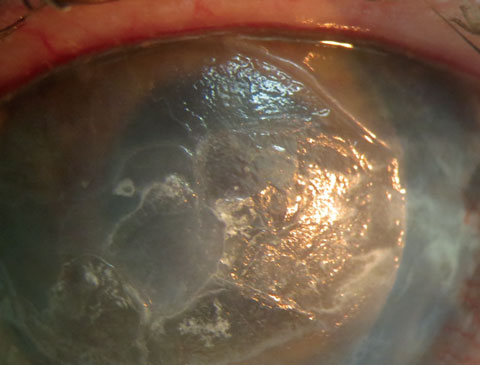
Ce patient présente une kératopathie de bande dans un œil droit pré-phthisis qui ne voit pas. L’élimination assistée par EDTA a été initiée pour résoudre le défaut central non cicatrisant. Cliquez sur l’image pour l’agrandir.
Présentation
Les patients atteints de kératopathie à bande peuvent se présenter pour des soins avec diverses plaintes. Les cas de diminution de la vision, de sensation de corps étranger, d’irritation des yeux, de photophobie ou de préoccupation quant à la modification de l’apparence de leurs yeux ont tous le potentiel d’être BK.1 Une KB précoce peut passer inaperçue du patient et n’apparaître qu’après un examen de routine à la lampe à fente. Dans de nombreux cas, cependant, la KB est associée à une maladie oculaire de longue date et le patient en est pleinement conscient.1
Une étude montre que les causes les plus fréquentes de BK sont l’œdème cornéen chronique (28%) et idiopathique (26%).2
Un examen approfondi du diagnostic différentiel, des causes possibles et des options de traitement est essentiel. Les cliniciens doivent mettre l’accent sur le risque de perte de vision et les options de traitement, car les patients asymptomatiques peuvent ne pas considérer cosmesis comme une raison suffisante pour subir une intervention chirurgicale.
BK se caractérise par l’apparition d’une bande interpalpébrale horizontale opaque blanc grisâtre sur la cornée centrale. Il est formé par la précipitation de sels de calcium sur la couche de Bowman, directement sous l’épithélium.1 L’extrême périphérie de la cornée peut être épargnée en raison de la présence de vaisseaux sanguins limbaux exerçant un effet tampon. Des trous dans la plaque sont souvent présents et sont causés par des nerfs cornéens traversant la membrane de Bowman jusqu’à la surface épithéliale. La bande s’initie généralement en périphérie et progresse vers le centre, mais peut, à l’occasion, commencer au centre. Les dépôts de calcium peuvent être très fins ou épais et ressemblant à une plaque. Les plaques épaisses ont tendance à s’écailler partiellement, en particulier à la périphérie. Cela provoquera des défauts épithéliaux et des douleurs. Chez les patients ayant des yeux autrement sains, l’acuité visuelle diminuera proportionnellement à la densité du dépôt de sel de calcium sur la cornée centrale.
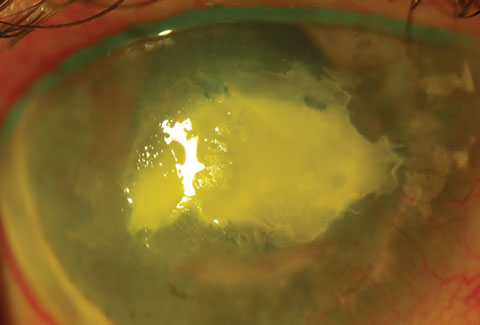
Cette image montre le même œil que celui de l’image précédente, après la procédure. Malheureusement, l’œil est devenu phthisique et a dû être énucléé. Cliquez sur l’image pour l’agrandir.
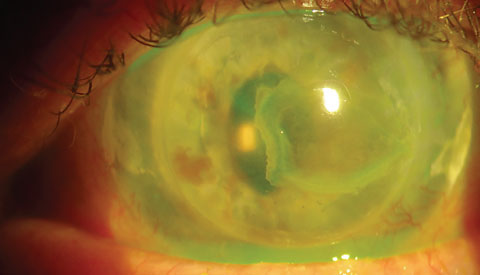
Récidive de BK en voyant l’œil gauche du même patient. Cet œil avec de l’ACIOL et une kératoplastie pénétrante pour la kératopathie à bande a eu une récidive malgré les efforts pour traiter les causes systémiques (arrêt de la vitamine D chez le patient). Cliquez sur l’image pour l’agrandir.
Causes locales
La cause sous-jacente de la BK est des niveaux anormaux de calcium et de phosphate, qui sont tous deux présents près de leur limite de solubilité dans les larmes, l’humeur aqueuse et le tissu cornéen. L’évaporation accrue des larmes favorise la précipitation de ces sels, en particulier dans la zone interpalpébrale. Par conséquent, la kératite sicca est un facteur de risque important pour la KB et doit être exclue en tant que cause. Même lorsque les niveaux de calcium et de phosphate sont normaux, l’élévation du pH de surface (alcalose) favorise la précipitation. L’alcalose peut être observée dans les yeux enflammés de manière chronique et peut expliquer le risque accru de KB chez les patients atteints d’uvéite chronique.3-5 Conditions telles que l’arthrite juvénile idiopathique avec uvéite, l’herpès simplex chronique et la kératite au zona, la sarcoïdose, le lupus érythémateux discoïde et la sclérose tubéreuse sont toutes associées à la KB.3-5
Un compromis endothélial et un œdème cornéen associé peuvent également entraîner un dépôt de calcium et de BK. Ce processus est parfois observé chez les patients aphaques qui ont de l’huile de silicone à l’intérieur de l’œil, et semble être dû au contact de l’huile avec la cornée postérieure.6-8 Une étude a conclu que la BK était l’une des principales complications chez 8% des patients traités avec de l’huile de silicone chez lesquels l’huile est restée dans l’œil pendant une moyenne de 30 mois, ce qui est nettement plus long que d’habitude.6 Les raisons exactes de cette association restent floues.7,8
Les affections oculaires associées à la KB, mais dont le mécanisme n’est pas clair, comprennent le glaucome au stade terminal, les dystrophies cornéennes et la kératite neurotrophique.9,10 Il est possible que le compromis endothélial joue un rôle dans certaines de ces conditions.
Un certain nombre de médicaments topiques peuvent provoquer une précipitation du calcium et de la BK, y compris des gouttes ophtalmiques contenant des phosphates, telles que des phosphates stéroïdes et d’autres gouttes ophtalmiques contenant des tampons phosphatés.11 Une étude montre que le risque de BK a doublé lorsque les brûlures d’alcali cornéen ont été traitées avec des gouttes ophtalmiques contenant du phosphate.12 Il a été démontré que la pilocarpine contenant des conservateurs à base de mercure augmentait également le risque de BK.12 Le mercure provoque des changements dans le collagène cornéen qui, à son tour, provoque un dépôt de calcium. Certaines interventions chirurgicales qui modifient la surface cornéenne ou l’endothélium augmentent le risque de KB, tout comme l’utilisation de certaines préparations viscoélastiques précoces et, comme mentionné, la présence intraoculaire d’huile de silicone et l’utilisation intraoculaire d’activateur tissulaire du plasminogène.12
Enfin, les patients exposés à des vapeurs de mercure ou de bichromate de calcium, qui peuvent survenir dans certaines professions industrielles, peuvent développer une KB.12
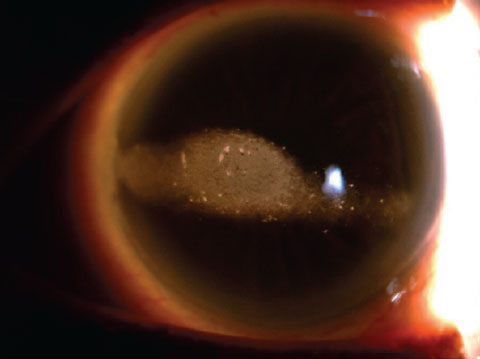
Cet œil autrement sain affiche clairement la bande keratopahty.
Causes systémiques
Outre les causes locales de déséquilibre du calcium et du phosphate, des taux sériques élevés associés à une maladie systémique peuvent également faire pencher la balance vers les précipitations. En particulier chez les patients présentant une nouvelle KB sans aucun facteur de risque oculaire, une cause systémique doit être étudiée. Les maladies systémiques corrélées à la KB sont généralement associées à une hypercalcémie et comprennent une hyperparathyroïdie, un apport excessif en vitamine D, une insuffisance rénale terminale, une hypophosphatasie, un syndrome de l’alcali du lait, une maladie de Paget, une sarcoïdose, un lupus érythémateux discoïde, la goutte (sous forme de cristaux d’urate), une tumeur maligne (comme le mélanome de l’iris) et une sclérose tubéreuse.13,14 Le syndrome lait-alcali (également appelé syndrome calcium-alcali), causé par un apport excessif de carbonate de calcium généralement pour la dyspepsie, est à la hausse et est actuellement la troisième cause la plus fréquente de patients admis à l’hôpital pour hypercalcémie.15 L’hypophosphatasie est une mutation héréditaire rare de l’enzyme phosphatase alcaline qui entraîne une dégradation des os et des dents. Les SACO doivent communiquer efficacement avec le fournisseur de soins primaires du patient pour s’assurer que la prise en charge systémique appropriée est terminée avant de commencer le traitement cornéen. Le contrôle systémique de l’hypercalcémie est complexe et peut nécessiter une intervention chirurgicale (par exemple avec une glande parathyroïde hyperactive) ou des médicaments comprenant des calcimimétiques, des biphosphonates et de la prednisone (selon la cause de l’hypercalcémie). Cela peut entraîner une urgence médicale en cas de taux de calcium extrêmement élevés et peut nécessiter une administration rapide de liquides intraveineux et de diurétiques pour éviter une arythmie cardiaque et des dommages au système nerveux.16
Diagnostic différentiel
Un certain nombre d’affections cornéennes peuvent présenter des caractéristiques similaires à celles de la KB.17,18
La goutte peut être associée à des dépôts d’acide urique cornéen d’apparence similaire à la BK et est en fait considérée comme une forme de BK par certains. La goutte est associée à des douleurs articulaires, à un gonflement et à une rougeur.
La kératite interstitielle peut se présenter de la même manière; cependant, une cicatrisation stromale plus profonde est attendue.
La dégénérescence calcaire primaire et secondaire de la cornée, bien que grossièrement similaire, peut facilement être distinguée à la lampe à fente; car le dépôt de calcium est également présent dans le stroma.19
La calciphylaxie, une condition de calcification vasculaire et de nécrose cutanée, était autrefois considérée comme une réaction d’hypersensibilité à des antigènes spécifiques, mais est maintenant considérée comme multifactorielle.20 Elle est plus fréquente chez les patients atteints d’insuffisance rénale terminale et généralement associée à des lésions cutanées violet foncé extrêmement douloureuses. C’est une maladie potentiellement mortelle.21
La dégénérescence sphéroïdale, également connue sous le nom de kératopathie du Labrador, est généralement associée à des environnements soumis à une exposition chronique intense aux UV. Les lésions cornéennes peuvent être plus élevées et d’apparence plus jaune, et souvent des découvertes conjonctivales interpalpébrales sont également trouvées.
Les dépôts cristallins de ciprofloxacine (et aussi d’ofloxacine et de norfloxacine) peuvent également être confondus avec la BK. Un historique détaillé devrait permettre au praticien de déterminer sa cause. L’arrêt du traitement entraîne généralement une résolution, tandis que des dépôts plus étendus peuvent interférer avec la réépithélialisation.
La dystrophie avancée de la membrane basale ou la dégénérescence nodulaire de Salzmann peuvent provoquer une opacification sous-épithéliale qui peut sembler grossièrement similaire à la BK. Contrairement à la BK, elle a généralement une composante vasculaire et n’épargne pas le limbe et ne présente pas d’îlots clairs dans la lésion.
La KB familiale est un trouble rare présentant un héritage autosomique (un héritage dominant et récessif a été rapporté) que le praticien astucieux peut découvrir en l’absence de causes locales ou systémiques après une analyse approfondie du pedigree.22
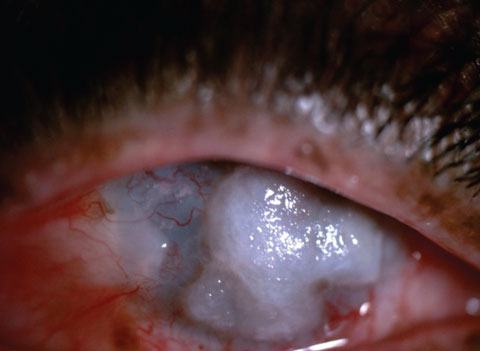
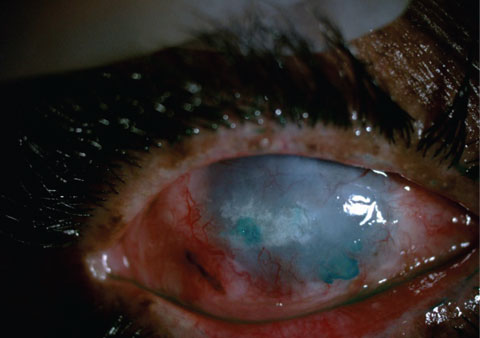
Un patient pré- (en haut) et post- (en bas) EDTA a aidé au grattage de grandes plaques calciques. L’objectif avec ce patient était le confort, pas la rééducation visuelle.
Considérations systémiques
Pour les patients qui présentent une KB en l’absence de cause sous-jacente connue, les taux sériques de calcium et de phosphate doivent être obtenus avec des tests de la fonction rénale, tels que l’azote uréique sanguin et la créatinine. Si un sarcoïde est suspecté, à partir de découvertes oculaires ou systémiques, un test enzymatique de conversion de l’angiotensine, une radiographie thoracique ou un scanner en spirale thoracique doivent être obtenus. Dans les cas autrement idiopathiques, les niveaux d’hormone parathyroïdienne doivent également être vérifiés. Si le traitement chirurgical est décidé par le DO et le patient, traitez d’abord toute affection systémique ou oculaire sous-jacente, sinon une récidive de la KB est hautement probable. Des modifications alimentaires sont indiquées chez les patients présentant un excès de vitamine D ou un syndrome lait-alcali.
Prise en charge non chirurgicale
De nombreux patients présenteront une KB causée par des antécédents de chirurgie oculaire, d’inflammation chronique ou de phthisie. Ces patients peuvent ne pas être symptomatiques et ne pas bénéficier visuellement d’un traitement chirurgical. Faites preuve de prudence avec les patients qui demandent un traitement chirurgical uniquement pour des raisons esthétiques, car les yeux atteints de BK ont souvent d’autres conditions et peuvent ne pas guérir aussi bien.2
Lorsqu’un tel patient présente des symptômes, un traitement alternatif non chirurgical peut inclure la pose d’une lentille de contact à bandage. Un traitement topique antimicrobien doit être instauré pour réduire le risque d’infection en cas de port de lentilles de contact pendant la nuit sur une cornée compromise. Les lentilles de contact opaques prothétiques peuvent également être adaptées à des problèmes cosmétiques. La lubrification sous forme de larmes artificielles, de gels et de pommades ophtalmiques peut aider de manière significative chez les patients présentant une sensation de corps étranger, des déchirures et une photophobie et devrait être un traitement de première intention. Il a également été démontré que l’application d’un dispositif à membrane amniotique favorise la guérison de la BK.1
Prise en charge chirurgicale
Une fois que les causes systémiques et oculaires de la KB sont éliminées et / ou traitées, et après discussion des risques et des avantages avec le patient, une offre rapide de traitement chirurgical profitera à vos patients. Une étude a montré que la majorité des patients présentaient un soulagement symptomatique partiel ou complet (98%) tandis qu’un tiers des patients amélioraient deux lignes à deux mois et 36 mois.2
Le traitement est relativement simple et peut même être effectué à la lampe à fente. Elle nécessite toujours l’ablation de l’épithélium cornéen, suivie d’un débridement superficiel (raclage cornéen) en présence d’acide éthylènediaminetétraacétique (EDTA).23,24 Dans certains cas, lorsque la surface est encore irrégulière après l’élimination du calcium, un laser excimère est utilisé pour lisser la surface cornéenne, mais cela entraînera un changement de réfraction.25
Les patients doivent être informés des résultats indésirables possibles, y compris des cicatrices cornéennes et une perte de vision, mais l’incidence de telles complications a été rapportée comme proche de zéro.24
Procédure
L’élimination du calcium est de préférence effectuée au microscope opératoire par chélation à l’aide d’une solution d’EDTA à 3% mais peut être effectuée à la lampe à fente si nécessaire. Les étapes de la procédure sont:17
1. Anesthésiez l’œil avec un anesthésique topique (par exemple, la proparacaïne) et placez un spéculum sur les paupières.
2. Débride l’épithélium cornéen. Cela peut être fait avec une lame de castor stérile ou un épurateur Amoils.
3. La solution d’EDTA à 3% est ensuite appliquée sur la zone de kératopathie de bande. Cela se fait généralement à l’aide d’un disque de papier filtre / écran cornéen, de bandes découpées de Weck-Cel ou d’applicateurs stériles en coton imbibés d’EDTA. Alternativement, un réservoir tel qu’un puits LASIK peut être placé sur la cornée et rempli d’EDTA. L’EDTA est appliqué à intervalles de trois minutes, en alternance avec une irrigation complète avec une solution saline équilibrée. Ceci est fait jusqu’à ce que le calcium disparaisse, ce qui peut prendre de 10 à 60 minutes. Des précautions doivent être prises pour éviter la toxicité pour les cellules limbales et minimiser l’irritation de la conjonctive. Les dépôts minces de calcium peuvent se détacher en cinq minutes, tandis que les plaques épaisses peuvent prendre de 30 à 45 minutes pour se dissoudre.
Terminer la procédure à la lampe à fente permet une meilleure visualisation. Cependant, lorsque la procédure est effectuée en position verticale, le drainage de l’EDTA dans le fornix inférieur augmente le risque de brûlure chimique conjonctivale. Placer des éponges contenant de l’EDTA sur la cornée est également beaucoup plus facile en position inclinée.
Le principal avantage de l’utilisation de l’EDTA est de minimiser les dommages à la couche de Bowman et de réduire le risque d’une surface réfractive irrégulière pouvant résulter d’un débridement agressif avec une lame. Un grattage doux entre les applications d’EDTA peut être effectué et peut aider à accélérer le processus.
5. Si la surface cornéenne est extrêmement irrégulière après la procédure, le polissage de la couche de Bowman avec une bavure de diamant de 5 mm ou une kératectomie photothérapeutique peut lisser la surface. Il est à noter que s’il reste du calcium résiduel, le traitement au laser excimère entraînera une aggravation de l’irrégularité cornéenne, car le laser ablate préférentiellement le calcium.25 Alternativement, une lentille de contact perméable aux gaz peut être utilisée ensuite.
6. Une lentille de contact souple est généralement placée à la fin de la procédure et des antibiotiques topiques prophylactiques sont utilisés jusqu’à ce que le défaut épithélial soit guéri. Nous prescrivons fréquemment des stéroïdes topiques pour moduler la guérison et réduire les cicatrices. Nous utilisons occasionnellement une membrane amniotique sans suture pour améliorer la guérison, en particulier lorsque l’épithélialisation retardée est anticipée, comme chez les patients atteints d’une maladie neurotrophique, d’une inflammation chronique de la surface oculaire ou d’un âge avancé. Ces cas peuvent être réservés à un spécialiste car un défaut épithélial non cicatrisant peut s’ensuivre et doit être traité de manière agressive.
Les cas plus avancés, en particulier ceux qui envahissent la membrane de Bowman, peuvent nécessiter une technique de kératectomie lamellaire plus étendue telle que la kératoplastie lamellaire antérieure profonde (DALK).26
Une kératectomie étendue peut provoquer des saignements des vaisseaux limbaux, en particulier dans les cas associés à une néovascularisation cornéenne superficielle ou à une kératite interstitielle. Cela peut être contrôlé avec des vasoconstricteurs sous pression ou topiques, et la cautérisation doit être évitée pour éviter d’endommager les cellules souches limbales.
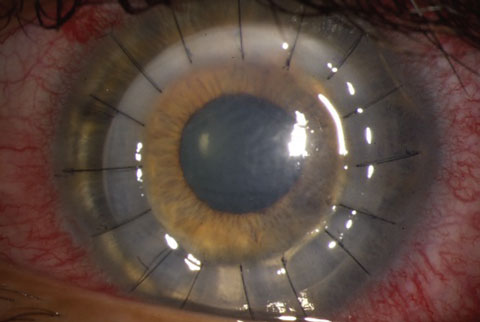
L’œil gauche d’un patient suite à une intervention DALK.
Soins postopératoires
Le patient doit être examiné cinq à sept jours après la chirurgie. L’examen de l’épithélium sous la lentille de contact peut être effectué avec de la fluorescéine. Les stéroïdes sont effilés et les lentilles de contact et les gouttes d’antibiotiques sont interrompues une fois que le défaut épithélial guérit.
Les cicatrices stromales antérieures résiduelles peuvent se prêter au laser excimère PTK pour améliorer la vision. Le PTK peut également être utilisé pour améliorer la surface oculaire et prévenir les érosions récurrentes.
Le patient doit être contrôlé tous les trois à 12 mois, en fonction de la gravité des symptômes. L’ablation chirurgicale peut être répétée si la kératopathie de la bande se reproduit.
Complications
Les principales complications liées à l’élimination des dépôts de calcium sur la surface cornéenne comprennent la douleur, les cicatrices cornéennes, l’œdème cornéen, l’infection, une diminution de la vision, un défaut épithélial non cicatrisant et une augmentation de l’astigmatisme irrégulier. L’EDTA est toxique pour la surface oculaire et une élimination inadéquate pendant ou après la procédure entraînera une brûlure chimique. Les récidives sont fréquentes et des traitements répétés peuvent être nécessaires. La récidive est la plus fréquente dans les cas de BK induite par l’uvéite.1,2
Parfois, une légère brume sous-épithéliale peut être observée des semaines après la chélation de l’EDTA, qui peut se résorber d’elle-même. Un stéroïde topique doux (par exemple, fluorométholone 0,1%) peut aider à résoudre ce trouble. S’il y a des dommages importants à la membrane de Bowman, la brume peut être permanente.
La BK significative est une maladie qui peut et doit être traitée par ablation chirurgicale assistée par EDTA. BK chez des patients par ailleurs en bonne santé doit être évalué pour les causes systémiques, y compris l’hypercalcémie. Les considérations de traitement incluent la probabilité de récupération visuelle, la présence de douleur, la photophobie et la sensation de corps étranger et le souci de la cosmèse.
La santé globale de l’œil et sa capacité à guérir après le traitement doivent également être prises en compte. Lorsque le traitement chirurgical n’est pas une option, la lubrification active ou l’utilisation d’un bandage ou d’une lentille de contact prothétique sont également des options.
Le Dr Stokkermans est le directeur des Services optométriques et le Dr Gupta est le directeur de la Cornée et des maladies externes des hôpitaux universitaires Cleveland Medical Center. Drs. Stokkermans, Gupta et Sayegh fréquentent le corps professoral de l’Université Case Western Reserve et proposent une approche d’équipe pour le traitement de la maladie de la cornée.
1. Jhanji V, Rapuano C, Vajpayee R. Kératopathie de la bande calcifique cornéenne. Curr Opin Ophthalmol. 2011 Juil; 22(4): 283-9.
2. Najjar D, Cohen E, Rapuano C, Laibson P. Chélation EDTA pour la kératopathie à bande calcique: résultats et suivi à long terme Am J Ophthalmol. 2004 Juin; 137(6): 1056-64.
3. Bernauer W, Thiel M, Kurrer M, et coll. Calcification cornéenne suite à un traitement intensifié avec des larmes artificielles au hyaluronate de sodium. Br J Ophthalmol. 2006 Mars; 90(3): 285-8.
4. Doostdar N, Manrique C, Hamill M, Barron A. Synthesis of calcium-silica composites: a route towards an in vitro model system for calcific band keratopathy precipitates. J Biomed Mater Res A. 2011 Nov; 99 (2): 173-83.
5. Daniel E, Pistilli M, Pujari S, et al. Risque d’hypotonie dans l’uvéite non infectieuse. Ophtalmologie. 2012 Novembre; 119 (11): 2377-85.
6. Morphis G, Irigoyen C, Eleuteri A, et al. Examen rétrospectif de 50 yeux avec tamponnade à l’huile de silicone à long terme pendant plus de 12 mois. Graefes Arch Clin Exp Ophthalmol. 2012 Mai; 250 (5): 645-52.
7. Sternberg P, Hatchell D, Foulks G, et al. L’effet de l’huile de silicone sur la cornée. Ophthalmol Arch. 1985 Jan; 103(1):90-4.
8. Federman J, Schubert H. Complications associées à l’utilisation d’huile de silicone dans 150 yeux après une chirurgie rétinienne-vitreuse. Ophtalmologie. 1988 Juil; 95(7): 870-6.
9. Kennedy R, Roca P, Landers P. Kératopathie à bande atypique chez les patients glaucomateux. Am J Ophthalmol. 1971 Nov; 72 (5):917-22.
10. Lam H, Wiggs J, Jurkunas U. Présentation inhabituelle d’une dystrophie polymorphe postérieure présumée associée à une hétérochromie de l’iris, à une kératopathie de bande et à un kératocône. Cornée. 2010 Oct; 29 (10): 1180-5.
11. Taravella M, Stulting R, Mader T, et al. Kératopathie à bande calcique associée à l’utilisation de préparations topiques de stéroïdes-phosphates. Ophthalmol Arch. 1994 Mai; 112(5): 608-13.
12. Kompa S, Redbrake C, Dunkel B, et al. Calcification cornéenne après des brûlures oculaires chimiques causées par des gouttes oculaires contenant du tampon phosphate. Burns. 2006 Sep; 32(6): 744-7.
13. Porter R, Crombie A. Calcification cornéenne et conjonctivale dans l’insuffisance rénale chronique. Br J Ophthalmol. 1973 Mai; 57(5): 339-43.
14. Shah P, Shields C, Shields J, Di Marco C. Kératopathie de bande secondaire à un mélanome de l’iris. Cornée. 1991;10(1):67-9.
15. Patel A, Goldfarb S. Vous avez du calcium? Bienvenue dans le syndrome calcium-alcalin. Je Suis Soc Néphrol. 2010;21(9):1440-3.
16. Personnel de la clinique Mayo. Maladies et affections: Hypercalcémie. Disponible à www.mayoclinic.org/diseases-conditions/hypercalcemia/basics/treatment/con-20031513 . Consulté le 9 décembre 2016.
17. Gerstenblith A, Rabinowitz M. Le Manuel des yeux Wills: Diagnostic et traitement des maladies oculaires au Bureau et aux urgences. 6e Éd. Il est le fils de Lippincott Williams & Wilkins; 2012.
18. Roy FH. Calcification cornéenne et conjonctivale. Dans: Roy FH, Fraunfelder FW, Fraunfelder FT.La thérapie oculaire actuelle de Roy et Fraunfelder. 6e éd. Série de thérapie actuelle. Philadelphie: Elsevier/ Saunders; 2008: 337-8.
19. Lavid F, Herreras J, Calonge M, et al. Dégénérescence cornéenne calcaire: rapport de deux cas. Cornée. 1995 Jan; 14(1): 97-102.
20. Il s’agit de l’Atlas des couleurs et du Synopsis de la dermatologie clinique de Wolff K, Johnson R, Saavedra A. Fitzpatrick. 7e éd. McGraw Hill : 429.
21. Angelis M, Wong L, Wong L, Myers S. Calciphylaxie chez les patients sous hémodialyse: Une étude de prévalence. Chirurgie. 1997;122:1083–90.
22. Arora R, Shroff D, Kapoor S, et coll. Kératopathie calcique familiale en forme de bande: rapport de deux nouveaux cas avec récidive précoce. J Ophtalmol indien. 2007 Jan-Fév; 55(1): 55-7.
23. Najjar D, Cohen E, Rapuano C, Laibson P. Chélation EDTA pour la kératopathie à bande calcique: résultats et suivi à long terme. Am J Ophthalmol. 2004 Juin; 137(6): 1056-64.
24. Im S, Lee K, Yoon K. Chélation combinée de l’acide éthylènediaminetétraacétique, kératectomie photothérapeutique et transplantation de membrane amniotique pour le traitement de la kératopathie à bande. J coréen Ophthalmol. 2010 Avril; 24 (2): 73-7.
25. Sharma N, Mannan R, Sinha R, et al. Kératectomie photothérapeutique au laser excimer pour le traitement de la kératopathie en forme de bande induite par l’huile de silicone. Lentilles de Contact avec les Yeux. 2011 Sep; 37(5): 282-5.
26. Wee S, Choi S, Kim J. Deep anterior lamellar keratoplasty using irradiated acellular cornea with amniotic membrane transplantation for intractable ocular surface diseases. Korean J Ophthalmol. 2015 Apr;29(2):79-85.