はじめに
植込み型除細動器(ICD)の心停止を減少させる利点は、多くの研究で実証されている。1-4初期ICD療法は、通常、遅い心室頻拍(VT)に対して抗静脈ペーシング(ATP)であり、速いVTおよび心室細動(VF)は高エネルギーショックで治療される。 VFゾーンで検出された心室性不整脈のほとんど(66%–76%)は、高エネルギーショックを必要とせずにATPによって終了することができる高速単形VT5-8です。9-11いくつかの研究は、経験的に高速VTゾーンで1ATPバーストをプログラミングすることが320と240ミリ秒(ms)の間のサイクル長(CL)と高速VTを終了するのに非常に効果的であることを実証しているATPは罹患率を増加させることなく、高エネルギーショックの必要性を減らすことができることを示唆している。6-8,12,13しかし、公開されたデータは、VT CL
270ms、7の場合、ATPの有効性が低いことを示唆しているが、非常に速いVTのATPバースト数を増加させる有効性は依然として議論の問題である。8,14さらに、short CLはATP故障とVT加速の予測因子です。11,15最後に、効果のないATPの場合、デバイスはショック送達前に再検出とコンデンサ充電を必要とし、エピソード持続時間が長くなり、失神のリスクが高 さらに、いくつかの研究では、ショックは無害ではなく、死亡リスクの3倍の増加につながる可能性があることが示されています。16-18
VFゾーンでの充電前(BC)および/または充電中(DC)のATPバーストをプログラミングする可能性(EnTrust study19)は、VFゾーンで無害なVT終了の可能性を維持しながら、ATP障害の場合の高エネルギーショック投与の遅延を回避するために開発された。 このタイプのプログラミングの有効性は毎日の臨床練習の患者の広い人口で評価されませんでした。 本研究の目的は、VFゾーンで検出された高速VTを有するICD患者におけるATP BCおよび/またはATPDCの有効性および安全性プロファイルを評価し、私たちの集団
方法研究設計と目的
私たちは、CareLinkモニタリングシステムがフォローアップICD患者を含む多施設前向き観察研究であるUMBRELLA試験のデータを分析しました。 VFゾーンで検出された持続的な単型VTのエピソードを持っていた患者が登録されました。 我々は、VTエピソード(CL200-320ms)の終了のための2つの連続したATPシーケンス(ATP BC/ATP DC)の戦略と単一のATPバーストDCの安全性と有効性を比較しました。 我々は、ATP有効性の予測因子を記述するために一変量および多変量解析を行った。
アンブレラレジストリ
本調査は、国立アンブレラレジストリ(Medtronic Implantable Cardiac Defibrillator Implant、NCT01561144を有するスペイン人集団における不整脈の発生率)の枠組みの中で開発された。 このレジストリは、スペインでMedtronic ICDを移植した人口の前向きおよび遡及的研究です。 UMBRELLA研究の将来的な部分(2011年以降)には、スペインでMedtronic ICDを移植したすべての患者が含まれ、CareLinkモニタリングシステムを介してすべての不整脈イベントとICD介入の将来的な収集が含まれている。 2011年以前にMedtronic ICDを移植し、CareLinkシステムを介して既にフォローアップされたすべての患者は、UMBRELLAレジストリに含まれ、icdインプラントの時点で臨床的および人口学的特徴が収集され、モニタリングシステムによって報告されたすべての不整脈事象およびICD介入が含まれた。 これらの患者は2011年以来前向きにフォローアップされています。 今回の調査では、患者は研究とレジストリの両方から進行した。 CareLink監視中にICDから取得されたすべての情報が分析されました。 記録されたエピソードは、査読者の委員会によってレビューされました。 このレジストリの詳細な説明は、他の場所で報告されています。20
この亜解析が完了すると、UMBRELLA研究では38のセンターから1645人の患者と6829エピソードのVTが発生しました。 1645人の患者のうち、288はvfゾーンで検出された心室リズムの1149エピソードを経験した。 それらのうち、662はATP BC/ATP DCを受けた単形VTを持続させた。 662エピソードのうち、120は、選択バイアスを避けるために分析から排除された(詳細については以下を参照)。 本研究では、240人の患者の残りの542エピソードを分析した(図1)。 研究から除外された心室イベントは、主にVF/多型VT(287)またはATPバースト(79)後のVFゾーンに加速遅いVTであった。 この研究は倫理的承認を得て実施された。 全患者から書面によるインフォームドコンセントを得た。
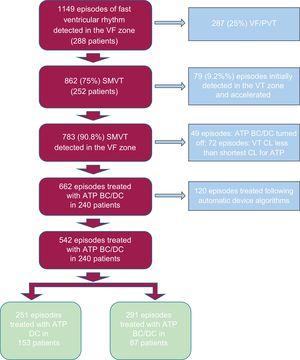
Selection algorithm for ventricular arrhythmias episodes detected in the VF zone. ATP, antitachycardia pacing; BC, before charging; CL, cycle length; DC, during charging; SMVT, sustained monomorphic ventricular tachycardia; VF, ventricular fibrillation; PVT, polymorphic ventricular tachycardia.
不整脈の定義とデバイスプログラミング
所定の基準に従って、不整脈は、心拍数の急激な変化から始まるときにVTとして分類され、規則的なR–R間隔 不整脈CLは、検出に先行する8つの間隔の平均として報告された。 VFゾーンで検出された320-200msの間のCLと心室起源のエピソードは、研究に含まれていました。
ATP BC/ATP DCがプログラムされたエピソードのみが含まれていた。 エピソードは、ATP BC/ATP DC機能の2つのプログラムモダリティに基づいて分割されました(図2)21。 初期のATP DC機能プログラミング(ATP DCまたはATP BC/ATP DC)は、臨床医の裁量によるものであった。 患者とエピソードは、初期の装置プログラミングに基づいて2つのグループに分けられた。
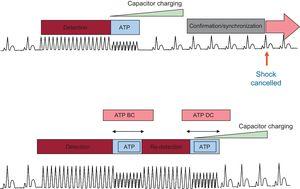
ATP BCおよびDCのための植込み型除細動器機能アルゴリズム。 ATP DCのみ(上部パネル)およびBC/DC(下部パネル)。 ATP、抗不整脈ペーシング;BC、充電前;DC、充電中。 Schwab et al.からの許可を得て変更されました。21
最初のモダリティ(ATP DC)は、充電中に1つのATPバーストで構成されています:検出後、ICDは充電を開始し、同時に1つのATPバーストを提供します。 コンデンサの充電終了後の最初の5つの間隔のうち4つがVTゾーンにない場合、ショックは中止され、そうでない場合はそれ以上の遅延なしに高エネル 第二のモダリティ(ATP BC/ATP DC)プログラム1ATPバーストBC:検出後、ICDは充電を開始せずに1ATPバーストを提供します。 これに続いて、VTが持続する場合、第二のバーストが配信されている間に充電を開始する再検出アルゴリズムが続きます。 このアルゴリズムは、衝撃送達までの時間をわずかに延長する。 それにもかかわらず、それは2つのATPバーストの管理を可能にし、第一バーストと第二バーストの間に再検出アルゴリズムを導入し、第一バーストが有効である場合にコンデンサの充電を回避する。 検出に必要な間隔の数は、名目上、ATP BC/ATP DC群の最初のバーストの後に12/16に設定された。 残りの装置の特徴は、患者の特徴および根底にある心臓病に従って、医師の裁量でプログラムされた。
ATP BC/ATP DC機能は、エピソード内の最初のATPバーストの有効性に基づいて、その後のエピソードでATP DCからATP BCに切り替えたり、ATPをオフにしたりすることができる3つの自動アルゴリズムによって強化されている。 この自動プログラミングは、ATPの有効性の誤った解釈につながる可能性があります。 したがって、自動変更後のエピソードは分析から排除され、それらの90%は、ATP DCで効果的に処理されたVTの1エピソード後にATP DCからATP BC/ATP DCへの自動スイッ このスイッチの目的は、バッテリの消耗を節約し、充電を回避し、必要に応じて2つのATPバースト(ATP BCおよびATP DC)を供給することです。 エピソードは、選択バイアスを導入し、ATP BC/ATP DCの有効性を過大評価する可能性があるため、分析から排除されました。
利用可能な場合は、検出前の遠視野心電図を検討し、リズム分類を支援しました。 エピソード持続時間は、最初の頻脈拍から最初の非頻脈拍までを測定した。 加速は、治療後に10%を超えるCL減少として定義された。 ATPバースト後に加速され,VFゾーンで検出されたv tまたは高速V tゾーンのエピソードは除外された。
ICDに記録された心室率の高いすべてのエピソードは、エピソードレビュー委員会によってレビューされました。 委員会は6人の専門家で構成され、3つのペアに分かれていた。 委員会の分類アルゴリズムは以前に詳細に説明されています。20
統計分析
連続変数は、正規分布に従っているかどうかに応じて、平均±標準偏差または中央値として表され、カテゴリ変数は数値およびパーセンテージ 正規または非正規の連続変数にはStudent t検定またはMann-Whitney U検定を使用し、カテゴリ変数にはカイ二乗検定またはFisher完全検定を適切に使用しました。 患者ごとの複数のエピソードを考慮に入れるようにATP有効性推定を調整するために、一般化推定式(GEE)法を使用した22; 特に、クラスタ化されたデータがバランスが取れておらず、クラスタ内の観測値の論理的な順序がないことを検証し、交換可能な相関行列を使用しました。 ATPの有効性に関連することが知られている変数、またはその関係が以前に公開されていた変数は、単変量解析に含まれていました。 多変量解析は、ベースラインと各エピソードとの間の経過時間としての共変量としての時間の次元を含む、ロジスティック回帰GEE調整分析を使用して行 P
を使用した前の単変量解析の任意の変数。モデルには2つが含まれていました。 統計的有意性をPに設定した。05(2-尾). データは、SPSS18.3for Windows(SPSS Inc)を使用して分析した。結果心室頻脈エピソードの研究人口と特徴
構造性心疾患を有する合計240人の患者が研究に含まれ、38ヶ月間フォローアップされた(中央値)。 ベースライン特性を表1に示す。 患者はATP DCの特徴の最初のプログラミングに基づいて2つのグループに分けられました。 1ATP DCでプログラムされた患者とATP BC/ATP DCでプログラムされた患者との間に差は観察されなかった。 フォローアップ中に、VFゾーンに登録された持続的な単形VTの542エピソードは、ATP BC/ATP DCによって処理されました。 患者あたりのエピソードの中央値は1であり、エピソードの最大数は単一の患者で28エピソードであった。
患者のベースライン特性
| 合計 (n=24) |
充電中 (n=153) |
充電前/充電中 (n=87) |
P | |
|---|---|---|---|---|
| インプラントの年齢 | 62.3±13.9 | 62.0±12.9 | 62.8±15.6 | .69 |
| 男性 | 214 (89.2) | 136 (88.8) | 78 (89.6) | .75 |
| 高血圧 | 126 (52.5) | 76 (49.7) | 50 (57.5) | .25 |
| 糖尿病 | 62 (26) | 41 (26.8) | 21 (24.1) | .65 |
| 慢性腎臓病 | 40 (17) | 26 (17) | 14 (16.1) | .89 |
| 心臓病 | ||||
| 虚血性 | 124 (51.7) | 80 (53) | 44 (51.8) | .86 |
| 拡張非虚血 | 73 (30.4) | 46 (30.5) | 27 (31.4) | .88 |
| Hypertrophic | 13 (5.4) | 8 (5.3) | 5 (5.9) | .85 |
| Valvular | 17 (7.1) | 13 (8.5) | 4 (4.7) | .27 |
| ARVD/C | 6 (2.5) | 4 (2.6) | 2 (2.4) | .89 |
| LVEF | 168 (70) | 107 (69.9) | 61 (70.1) | .98 |
| Atrial fibrillation at implant | 50 (20.8) | 34 (22.2) | 16 (18.4) | .59 |
| 一次予防 | 133 (55.4) | 86 (57.3) | 47 (55.35) | .76 |
| 機能クラスNYHA I-II | 157 (65.4) | 100 (65.4) | 57 (65.5) | .98 |
| シングルチャンバー ICD | 105 (43.8) | 69 (45.1) | 36 (41.4) | .58 |
| 二重部屋ICD | 66 (27.5) | 37 (24) | 29 (33.3) | .18 |
| 両室ICD | 69 (28.8) | 47 (30.7) | 22 (25.3) | .37 |
ARVD/C、不整脈原性右心室異形成/心筋症;ICD、植込み型除細動器;LVEF、左心室駆出画分;NY H A、New York H Eart Association。
データはNoと表されます。 (%)または平均±標準偏差。
植込み型除細動器のプログラミングを表2に示します。 この研究に含まれているすべてのエピソードは、ショック前に少なくとも1つのATPバーストを有していた;これらのうち、251のエピソードは、コンデンサ充電中(ATP DC)にのみ1つのATPバーストを有していたが、291のエピソードは2つのATPバーストを有していた:1BCと1DC(ATP BC/ATP DC)。 検出に必要な間隔の数は、エピソードの18/24で85.1%に設定され、2つのグループ間の違いはありませんでした。
植込み型除細動器と心室頻拍の特徴
| 合計 (n=542) |
充電中 (n=251) |
充電前/充電中 (n=291) |
P | |
|---|---|---|---|---|
| 検出する間隔の数(18/24) | 461 (85.1) | 217 (86.5) | 244 83.8) | .74 |
| ATPパルス数=8 | 521 (96.1) | 238 (94.8) | 283 (97.2) | .82 |
| ATP結合間隔=88% | 525 (96.9) | 242 (96.4) | 283 (97.2) | .86 |
| サイクル長、ms | 273±23 | 273±23 | 273±23 | .99 |
| サイクルの長さの間隔 | ||||
| ≤ 240 ms | 75 (13.8) | 35 (13.9) | 40 (13.7) | .95 |
| 241-260 ms | 124 (22.9) | 53 (21.1) | 71 (24.4) | .36 |
| 261-280 ms | 177 (32.7) | 84 (33.4) | 92 (31.6) | .64 |
| 281-300 ms | 110 (20.3) | 58 (23.1) | 53 (18.2) | .16 |
| Episode duration, s | 11 | 12 | 9 | .001 |
| Episode duration in successful ATP (s), n=395 | 10 | 11 | 8 | .001 |
| エピソードの期間(s)n=147 | 17 | 16 | 19 | .07 |
| 加速されたエピソード | 8 (1.5) | 3 (1.2) | 5 (1.7) | .43 |
ATP、抗不整脈ペーシング。
データはNoと表されます。 (%)、平均±標準偏差、または中央値。
VTエピソードの主な特徴を表2に示す。 平均VT CLは273±23msであり、2群間に差はなかった。 2つのグループ間のCL間隔の分布も表2に示されています。 いずれのCL間隔でも差は観察されなかった。
抗静脈ペーシング有効性
全体として、ATP療法の有効性は72.9%であり、VFゾーンにおけるVTの542エピソードのうち395エピソードを終了させた(表3)。
抗不整脈ペーシングとショック軽減の有効性
| 合計 (n=542) |
充電中 (n=251) |
充電前/充電中 (n=291) |
P/または | |
|---|---|---|---|---|
| 未調整のATPの有効性 | 395 (72.9) | 139 (55.4) | 256 (88) | .001 |
| 未調整の最初のATPバースト有効性 | 202 (69.4) | |||
| GEE調整有効性、%(95%CI) | 67.3 (61.7-72.5) | 60.4 (53.3-67.1) | 79.3 (71.6-85.3) | 2.5 (1.5-4.1) .001 |
| GEE調整された最初のATPバースト有効性、%(95%CI) | 63.7 (55.1-71.6) | |||
| ショックで終了したエピソード | 147 (27.1) | 112 (44.6) | 35 (12) | .001 |
| GEE-高エネルギーショック終了時に調整、%(95%CI) | 32.7 (27.5-38.3) | 39.6 (32.9-46.7) | 20.7 (14.7-28.4) | 0.4 (0.24-0.66) .001 |
| 衝撃の総数 | 174 | 133 | 41 | .001 |
| エピソードあたりの平均ショック数 | 0.32 | 0.53 | 0.14 | .001 |
| エピソードあたりの平均ショック数(ショックを伴うエピソード) | 1.18 | 1.19 | 1.17 | .43 |
| 成功したATPとエピソードで衝撃 | 20 (5.1) | 19 (13.6) | 1 (0.4) | .001 |
95%CI,95%信頼区間;ATP,抗不整脈ペーシング;GEE,一般化推定式;または,オッズ比.
特に断りのない限り、データはNoと表されます。 (%).
1ATPバーストDCで終了したエピソード数は139であり、有効性は55.4%であった(GEE調整済み、60.4%、95%CI、53.5%、95%CI、53.5%、95%CI、53.5%、95%CI3-67.1)、1または2のATPバーストBC/DCによって終了したエピソード数は256であり、88%の有効性を表していた(GEE調整、79.3%、95%CI、71.6-85.3)。 プログラムされたATP BC/ATP DCを持つエピソードのグループでは、2ATPバーストは89エピソード(30.6%)で配信されました。 この群では、最初のATPバースト(ATP BC)は202エピソードで有効であった(69.4%、GEE調整、63.7%、95%CI、55-72)。
atp BC/ATP DC群対ATP DC群に対するatp有効性の単変量GEE調整オッズ比(OR)は2.5であった(95%CI、1.5-4.1;P
)。001). 表3は、粗およびGEE調整ATP有効性のデータを示しています。
全世界で、粗ATPの有効性は、非常に高速なVT(CL≦240ms)では60%から、281~300msの間のVTでは80%までの範囲であった(表4)。 粗ATP有効性は、ATP BC/ATP DCグループ対ATP DCグループのすべてのCLにわたって一貫して高かったが、この差は281と300msの間のVTのために統計的に有意ではなかった。GEE調整された分析は、より速いVTのために同じ有意差をもたらし、より遅いCL(281-300ms)のVTのために同様の有効性をもたらした。
頻脈周期の長さによる抗徐脈ペーシングの有効性
| 合計 (n=542) |
充電中 (n=251) |
充電前/充電中 (n=291) |
P | |
|---|---|---|---|---|
| 未調整のATPの有効性 | ||||
| CL≤ 240 | 45 (60) | 10 (28.6) | 35 (87.5) | .01 |
| 241-260 | 89 (71.8) | 26 (49.1) | 63 (88.7) | .01 |
| 261-280 | 126 (71.6) | 44 (52.4) | 82 (89.1) | .01 |
| 281-300 | 89 (80.2) | 43 (74.1) | 46 (86.8) | .1 |
| 未調整の最初のATPバースト有効性 | ||||
| CL≤ 240 | 29 (72.5) | |||
| 241-260 | 49 (69.1) | |||
| 261-280 | 82 (89.1) | |||
| 281-300 | 42 (79.2) | |||
| GEE調整有効性、%(95%CI) | ||||
| CL≤ 240 | 56 (41-71) | 23 (37-53) | 57 (78-91) | .02 |
| 241-260 | 62 (51-71) | 49 (36-62) | 86 (73-93) | .01 |
| 261-280 | 65 (55-74) | 53 (41-65) | 85 (71-93) | .01 |
| 281-300 | 79 (69-86) | 75 (62-85) | 84 (69-93) | .1 |
| GEE調整された最初のATPバースト有効性、%(95%CI) | ||||
| CL≤ 240 | 73 (61-82) | |||
| 241-260 | 68 (52-80) | |||
| 261-280 | 83 (67-93) | |||
| 281-300 | 79 (65-88) | |||
95%CI、95%信頼区間、ATP、抗不整脈ペーシング; CL、サイクル長;GEE、一般化推定式。
特に断りのない限り、データはNoと表されます。 (%).
多変量GEE調整分析では、ATP有効性に有意に関連する3つの変数が示されました:atp BC/ATP DC対ATP DCのみのプログラミング(OR、2.8;95%CI、1.3-5.8;P
)。001)および非虚血性心筋症vs他の心臓疾患(OR、2.1;95%CI、1.1-4.5;P=。041)は、より高いATP有効性と関連していたが、CL≧240ms(OR、2.67;95%CI、1.15-5.8;P=。03)およびCL241-260ms(OR,2.04;95%CI,1.1-5.4;P=.03)は、低いATP有効性と関連していた(図3)。
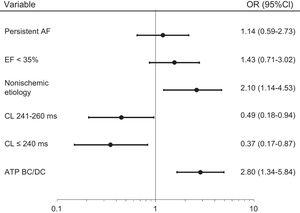
ATP有効性予測因子の多変量一般化推定式調整解析。 95%CI,95%信頼区間;AF,心房細動; ATP,抗不整脈ペーシング;BC/DC,充電前/充電中;CL,サイクル長;EF,駆出率;または,オッズ比.
高エネルギーショックの減少
必要な高エネルギーショック全体147エピソード(27.1%):ATP DCで処理したエピソード112エピソード(44.6%)対ATP BC/ATP DCで処理したエピソード35エピソード(12%)(表3)。 プログラミングATP BC/ATP DCは、高エネルギーショックの必要性の73%(66%-79%)絶対リスク低減と関連していた。
ATP BC/ATP DC群対ATP DC群のGEE調整または高エネルギーショックは0.4であった(95%CI、0.24-0.66;P
。001).
CL≦240msの非常に高速なVTを含む、すべてのCL間隔で有意な高エネルギー衝撃減少が観察された(図4)。
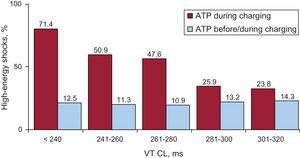
異なるVT CLに対する衝撃低減。 Vt CLとATPプログラミングによると、ショックを受けたVTエピソード。 ATP、抗徐脈ペーシング;CL、サイクル長;VT、心室頻脈。
ICDは20エピソード(5.1%)で高エネルギーショックをもたらし、ATPバーストはVTの終結に効果的であったが、そのうちの19エピソードはATP DC群で発生したのに対し、ATP BC/ATP DC群では1エピソードのみであった(P.1)。001). 終了モダリティの分析は、これらのエピソードはすべて、ATPバーストとVT終了後にいくつかの心室発作ビートを持っていたことを明らかにした。 これらの心室発作性拍動は、コンデンサ充電後に短い再検出ウィンドウに落ち、ショック送達を誘発した。
ATP DC群では総ショック数とエピソードあたりの平均ショック数が高かったが、ショックエピソードの平均ショック数は2群間で差を示さなかった。
エピソードの持続時間の中央値は11秒でした。 ATP BC/ATP DCでプログラムされたエピソードは有意に短かった(表2)。
ATPで正常に終了したエピソードのエピソード期間の中央値は、ATP DCグループでわずかに長く、これは異なる再検出アルゴリズムによって説明できます。 実際、ATP DCグループでは、icdはコンデンサの完全な充電と再検出ウィンドウの終了を待ってから、エピソードの終了を考慮してショックを中止します。 ATP BC/ATP DC群対ATP DC群では、ショックを受けたエピソードのエピソード持続時間が長くなる傾向がありました:19秒(16-22)vs16秒(14-21);P=。07.
VTの加速は両群で低かった(表2)が、ATP BC/ATP DC群の5つのVTエピソード(1.7%)に対して、ATP DC群の3つのエピソード(1.2%)で発生した(P=NS)。 注目すべきは、ATP BC/ATP DCグループの加速VTの2つのエピソードのうち5つは、第二のATPバーストで正常に処理されました。
ディスカッション主な知見
これは、vfゾーンでコンデンサ充電の前に第二のATPバーストを追加することは、充電中のみの単一のATPバーストと比較して、高エネル
抗徐脈ペーシングの有効性
抗徐脈ペーシングは、vtおよび高速VTゾーンで2つ以上のATPバーストを試験する研究によって示されるように、無害な高速VT終14,23さらに、高速VTゾーンで2つ以上のATPバーストをプログラミングすることは、VT終了に必要な高エネルギーショックの減少につながる、1ATPバーストと標準的な療法よりもグローバルATPの有効性を高めるのにより効果的であることが観察されている。20
VFゾーンでは、この検出ゾーンでのATPの有効性についての懸念と迅速な決定的な治療の必要性を考慮して、ICDは伝統的にショック送達の遅延を避ける Entrust study19は、VFゾーンで検出された高速VTに対するATP DCの有効性を決定するために設計された最初の非ランダム化試験でした。 エピソードは、送達されたATPのタイプ(ATP DCまたはATP BC)に基づいて分離されなかった。 研究に含まれるVTエピソードの数が限られているにもかかわらず(n=84)、ATP BC/ATP DCの有効性は、CL
300msのエピソードではほぼ70%であった。
私たちの集団では、コン この発見は2つの要因によって説明されるかもしれない。 まず、ATPは高速VTを終了するのに有効であることが知られているので、1つ以上のバーストを追加すると、非常に高速VTであっても、全体的なATP有効性を増 第二に、2つのATP戦略の異なるアルゴリズムが重要な役割を果たしているようです。 ATPバーストBCの投与に続いて、VTの持続性を評価する再検出アルゴリズムが実行されます。 対照的に、ATP DCのみがプログラムされている場合、ATPバーストの後、vtゾーンの5つの間隔のうち2つ以上の検出がショック送達をトリガします。 この違いは、不必要なショックを回避するという点で、ATP BCをより具体的にします。 これは、VFゾーン内のvtの重要ではない数がATPバースト後に遅延終了を示したり、過度に敏感な再検出アルゴリズムを混乱させる可能性があるいくつかの心室余分なビートが続いていることを考慮するときに特に重要である。 これはまた、ATP BC/ATP DC群対ATP DC群(69.4%対55.4%)における最初のATPバーストに対するより高い観察されたATP有効性を部分的に説明するのにも役立つ。 観察された差はGEE調整によって補正されたときにはるかに低く,残りのギャップは以前に報告されたように,異なる再検出アルゴリズムによって果たされた役割に起因する可能性がある。 方法のセクションで説明したように、我々は分析からそれらのエピソードは、彼らが主に高速VTではないので、1以上のATPバースト後に遅いVTから加速し、彼らはこの特定の設定でATPのかなり減少した有効性と可能な選択バイアスにつながる無効かつ不整脈ATPバーストから来る除外することにしました。
非虚血性心筋症は、我々の集団におけるATP有効性が有意に高いことに関連していた。 しかし、PAINFREE IIおよびADVANCE CRT-D試験によって報告されているように、それは非虚血患者にとっても非常に有効な戦略であるという証拠がある。7,24我々の結果とこれらの以前の研究に照らして、非虚血患者は、高速VTエピソードのATP終了のための良い候補であると思われる。7,24
短いCLは、多変量解析におけるATP有効性を低下させた。 この関連に関する文献は議論の余地がありますが11,20我々は、非常に速いVTにおけるATPの有効性の低下について多くのもっともらしい説明があると それにもかかわらず、このCLの範囲のより低い全体的な有効性は私達が非常に速いVTのエピソードのATP BC/ATP DCのプログラミングおよび衝撃の減少とのより高い有効性をまた記述したように1つのATPの破烈だけとの保守的なプログラミングに導くべきではない。
衝撃低減
我々は、充電前と充電中に2つのATPバーストをプログラミングすることは、単一のバーストDCの従来のプログラミングと比較して、高エネルギー衝撃の73%
我々はまた、2つのATPバーストをプログラミングすることは、ATP障害があった場合、VTエピソードのわずかな非統計的に有意な延長に関連していたことを観察した。 観察された違いは、第二のATPバーストの送達に必要な時間によるものであり、失神の発生率の増加を報告しなかった以前の出版された研究、7、25で観察さ
Icdプログラミングを最適化する際には、非常に重要な臨床的意味を持つため、ショック低減が不可欠です。
ICDショックは生活の質の低下に関連しており、心不全の悪化および死亡率の増加に関連している可能性があることが記載されている26。これらの理由から、非常に高速なVTの場合であっても、高エネルギーショックの必要性を最小限に抑える戦略が推奨される。 ATPバーストBCの追加は、不必要なショックを避けるのに役立つようです。
効果的なATPバースト後に送達されるかなりの数のショックを観察したことを強調することが重要であり、ATP DC群ではほぼのみであり、特にVT終了後に心室の余分なビートがあった場合、この群ではショックの13.6%を占める。 この発見は、良好な特異性を有する再検出ウィンドウに続いてATPバーストBCをプログラミングすることの重要性を強化する。 ATP特異性を改善するために、2つのATPバーストと2つの連続した再検出をプログラミングすることとは別に、ATPバーストDC後の新しいアルゴリズムが最近開発されており、これは不要なショック送達を減少させるようである。27最後に、ATP BCは、ATPが有効である場合に消費されるコンデンサ充電によって表されるエネルギー消費を回避し、28バッテリ寿命に影響を与えます。
私たちの研究では、エピソードのほとんどは必要な間隔の数を18/24に設定していましたが、最近の証拠では、より長い検出間隔をプログラムすると、ICD療法、特にショックを受ける可能性が低下する可能性があることが示唆されています。したがって、検出間隔が長いとかなりの数のVTが自発的に終了するため、我々の研究ではATPの有効性を過大評価している可能性があります。 それにもかかわらず、ICDがVTエピソードを検出したら、検出ウィンドウの長さに関係なく、充電前と充電中のバーストをプログラミングすることによるATPの最適化は、VTを終了して衝撃を避けるために重要であると考えられている。 最近の証拠に基づいて、有効性を最大にし、高エネルギー衝撃を減らすために延長された検出の窓およびATPの破烈BC/DCをプログラムすることは勧めら
制限
最も重要な制限は、無作為化と対照群が存在しないことにあります。 すべての患者は全国的な観察研究に登録されており、デバイスプログラミングは各センターの臨床実践に依存していた。 患者は前向きに含まれていたが、実行された分析は遡及的である。 1または2ATPバーストのプログラミングにつながった基準は、医師に依存し、本研究では調査できなかった頻脈エピソードの臨床的特徴または特徴に関
ICDプログラミングの他のいくつかの側面は、検出するために必要な間隔の数やATP投与のための最短CLなど、均質ではなかった。 最後に,このプログラミングアルゴリズムの安全性を評価するために使用される基準は間接的であり,主に高エネルギー衝撃低減とエピソード持続時間に関連している。 Syncopalイベントに関するデータを確実に収集することはできませんでした。 彼らはこの研究には含まれていませんでした。
結論
この研究は、VFゾーンで速いVTを示すICD患者における標準的なバーストATP DCに加えて1ATPバーストBCをプログラミングすることは、高エネルギーショックの有意な減少と関連していることを示唆している。 さらにこのタイプのプログラミングはエピソードの持続期間を延長しないようで、ATP DCだけの場合にはコンデンサー充満による電池の消費を避けるかも この戦略は、毎日の臨床診療におけるICDプログラミングを最適化するのに役立ちます。
利益相反
いずれも宣言されていません。
- –
VFゾーンで検出されたVTのほとんどは、高エネルギーショックを必要とせずにATPによって終了することができます。 いくつかの研究は、経験的に高速VTゾーンで1ATPバーストをプログラミングすることは、高速VTを終了するのに非常に効果的であることを示 これらの研究は、ATPが罹患率を増加させることなく高エネルギーショックの必要性を減少させることができることを示している。 Vfゾーンでのコンデンサ充電前および/またはコンデンサ充電中のATPバーストをプログラミングする可能性は,VFゾーンで無害なVT終端の可能性を維持しながらATP障害がある場合の高エネルギーショック投与の遅延を避けるために開発された。
この研究は何を追加しますか?
- –
この研究は、標準バーストDCに加えて1ATPバーストBCをプログラミングすることは、VFゾーンの高速VT患者の高エネルギーショックの有意な減少に関連して このタイプのプログラミングはエピソードの持続期間を延長しないようで、電池の消費を避けるかもしれません。 この戦略は、毎日の臨床診療におけるICDプログラミングを最適化するのに役立ちます。