efekt Jahna–Tellera, czasami znany również jako zniekształcenie Jahna-Tellera, opisuje zniekształcenia geometryczne cząsteczek i jonów, które są związane z pewnymi konfiguracjami elektronów. Ten efekt elektroniczny został nazwany na cześć Hermanna Arthura Jahna i Edwarda Tellera, którzy udowodnili, używając teorii grup, że orbitalnie zdegenerowane cząsteczki nie mogą być stabilne. Twierdzenie Jahna-Tellera zasadniczo stwierdza, że każda nieliniowa cząsteczka o przestrzennie zdegenerowanym elektronicznym stanie podstawowym ulegnie zniekształceniu geometrycznemu, które usuwa tę degenerację, ponieważ zniekształcenie obniża ogólną energię cząsteczki.
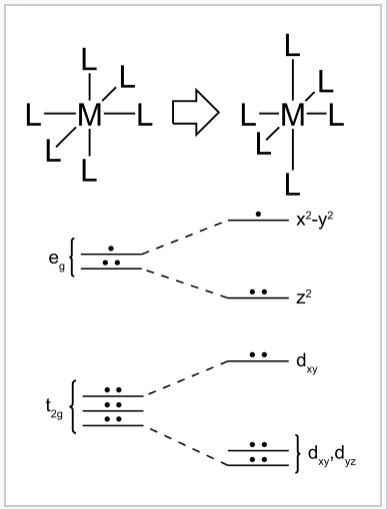
zniekształcenie Jahna-Tellera ośmiościanowego kompleksu metali przejściowych D9. Zniekształcenie tetragonalne wydłuża wiązania wzdłuż osi z, gdy wiązania w płaszczyźnie x-y stają się krótsze. Zmiana ta obniża ogólną energię, ponieważ dwa elektrony na orbitalu dz2 spadają w energię, gdy jeden elektron na orbitalu DX2-y2 idzie w górę.
możemy zrozumieć ten efekt w kontekście ośmiościanowych kompleksów metali, rozważając konfiguracje elektronów d, w których zestaw orbitalny np. zawiera jeden lub trzy elektrony. Crf2) , low spin d7 (np. Nanio2) i D9 (np. Cu2+). Jeśli kompleks może zniekształcić, aby złamać symetrię, to jeden z (dawniej) zdegenerowanych orbitali np. spadnie w energię, a drugi wzrośnie. Więcej elektronów zajmie dolny orbital niż górny, co spowoduje ogólne obniżenie energii elektronicznej. Podobne zniekształcenie może wystąpić w kompleksach czworościennych, gdy orbitale T2 są częściowo wypełnione. Takie zniekształcenia geometryczne, które obniżają energię elektroniczną, są uważane za napędzane elektronicznie. Podobne zniekształcenia elektronicznie napędzane występują w jednowymiarowych związkach łańcuchowych, gdzie nazywane są zniekształceniami Peierlsa, oraz w dwuwymiarowych arkuszach, gdzie nazywane są falami gęstości ładunku.
efekt Jahna–Tellera jest najczęściej spotykany w kompleksach ośmiościanowych, zwłaszcza w sześciokolorowych kompleksach miedzi (II). Konfiguracja elektroniczna D9 tego jonu daje trzy elektrony w dwóch zdegenerowanych orbitalach eg, co prowadzi do podwójnie zdegenerowanego elektronicznego stanu podstawowego. Takie kompleksy zniekształcają się wzdłuż jednej z cząsteczkowych osi czworokątnych (zawsze oznaczanych osią z), co powoduje usunięcie degeneracji orbitalnej i elektronowej oraz obniżenie ogólnej energii. Zniekształcenie zwykle przyjmuje formę wydłużenia wiązań do ligandów leżących wzdłuż osi z, ale czasami występuje jako skrócenie tych wiązań (twierdzenie Jahna–Tellera nie przewiduje kierunku zniekształcenia, tylko obecność niestabilnej geometrii). Gdy występuje takie wydłużenie, efektem jest obniżenie odpychania elektrostatycznego między parą elektronów na ligandzie zasadowym Lewisa a dowolnymi elektronami na orbitalach ze składową z, obniżając w ten sposób energię kompleksu. Jeśli oczekuje się, że niezakłócony kompleks będzie miał centrum inwersji, zostanie to zachowane po zniekształceniu.
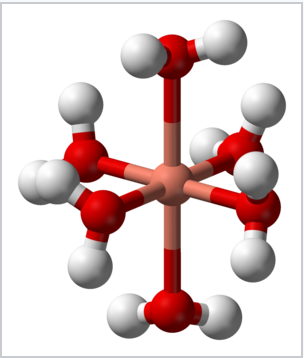
efekt Jahna-Tellera jest odpowiedzialny za tetragonalne zniekształcenie jonu kompleksowego heksaakoppera (II), 2+, który w przeciwnym razie mógłby posiadać geometrię oktaedryczną. Dwie osiowe odległości Cu-O wynoszą 2.38 Å, podczas gdy cztery równikowe odległości Cu-O wynoszą ~1,95 Å.
w kompleksach oktaedrycznych efekt Jahna–Tellera jest najbardziej wyraźny, gdy Nieparzysta liczba elektronów zajmuje np. orbitale. Sytuacja ta pojawia się w kompleksach o konfiguracjach D9, D7 o niskim spinie lub D4 o wysokim spinie, z których wszystkie mają podwójnie zdegenerowane Stany naziemne. W takich związkach np. orbitale uczestniczą w punkcie degeneracji bezpośrednio na ligandach, więc zniekształcenie może skutkować dużą stabilizacją energetyczną. Ściśle mówiąc, efekt występuje również, gdy występuje degeneracja spowodowana elektronami w orbitalach T2G (tj. konfiguracjach takich jak D1 lub d2, z których oba są potrójnie zdegenerowane). W takich przypadkach efekt jest jednak znacznie mniej zauważalny, ponieważ występuje znacznie mniejsze obniżenie odpychania przy oddalaniu ligandów od orbitali t2g, które nie wskazują bezpośrednio na ligandy (patrz tabela poniżej). To samo dotyczy kompleksów czworościanowych (np. manganian: zniekształcenie jest bardzo subtelne, ponieważ można uzyskać mniejszą stabilizację, ponieważ ligandy nie są skierowane bezpośrednio na orbitale.
oczekiwane efekty koordynacji ośmiościanowej przedstawiono w poniższej tabeli:
| liczba elektronów d | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| High / Low Spin | HS | LS | HS | LS | HS | LS | HS | LS | ||||||
| Siła efektu J – T | w | w | s | w | w | w | w | s | s | |||||
w: słaby efekt Jahna-Tellera (orbitale T2G nierównomiernie zajęte)
s: oczekiwany silny efekt Jahna–Tellera (np. orbitale nierównomiernie zajęte)
puste: oczekiwany efekt Jahna–Tellera.
efekt Jahna–Tellera przejawia się w widmach absorbancji UV-VIS niektórych związków, gdzie często powoduje rozszczepienie pasm. Jest łatwo widoczny w strukturach wielu kompleksów miedzi (II). Dodatkowe, szczegółowe informacje na temat anizotropii takich kompleksów i charakteru wiązania ligandu można uzyskać z drobnej struktury niskotemperaturowych widm elektronowego rezonansu spinowego.
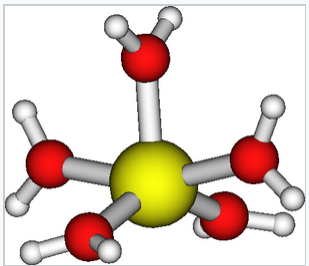
jon Cu (II) może również koordynować pięć cząsteczek wody w wydłużonej kwadratowej piramidzie z czterema wiązaniami cu-OEQ (2×1, 98 Å i 2×1, 95 Å) i długim wiązaniem Cu-OAX (2,35 Å). Cztery ligandy równikowe są zniekształcone od średniej płaszczyzny Równikowej o ± 17°.