by slcontrols,February27,2019
ALCOA+は、データの整合性を保証するフレームワークまたは一連の原則です。 米国食品医薬品局–それはによって導入され、まだFDAによって使用されています。 これは、特に医薬品の研究、製造、試験、およびサプライチェーンに関連して、分野の範囲で関連性を持っています。
コンプライアンス上の理由から不可欠であるだけでなく、ALCOA+原則はGMP(Good Manufacturing Practices)にとってますます重要になってきています。
データ整合性の重要性
データは医薬品の製造と研究において常に重要でした。 しかし、さまざまな要因があることは、データの重要性が指数関数的に高まっていることを意味します。 これを推進する要因には、消費者とエンドユーザーの進化する期待に加えて、規制要件の強化、製薬業界の競争力の強化などがあります。
しかし、データだけを持つことはできません。 代わりに、データが必要であり、そのデータの整合性を確保する必要があります。 これがあれば、使用して頼ることができるデータがあります。
ALCOAの原則は、データの整合性を保証します。 これらは、次のタイプのGMPレコードに適用されます:
- 電子的に記録–単純な機械から複雑で高度に設定可能なコンピュータ化されたシステムまでの機器を使用して記録されたデータ
- 紙ベース-手動観察または活動の紙に手動記録
- ハイブリッド–紙ベースと電子記録の両方が元の記録を構成する
- その他–これには写真、画像、クロマトグラフィプレートなどが含まれる
ALCOA Principles
alcoaは、元のデータ整合性の5つの原則の頭字語です。 これらの原則は次のとおりです:
ただし、当初のALCOA原則はALCOA+に更新されている。 元の原則は、四つの追加で残っています:
- 完全な
- 一貫性のある
- 永続的な
- 利用可能な
それぞれの原則をより詳細に見てみましょう。
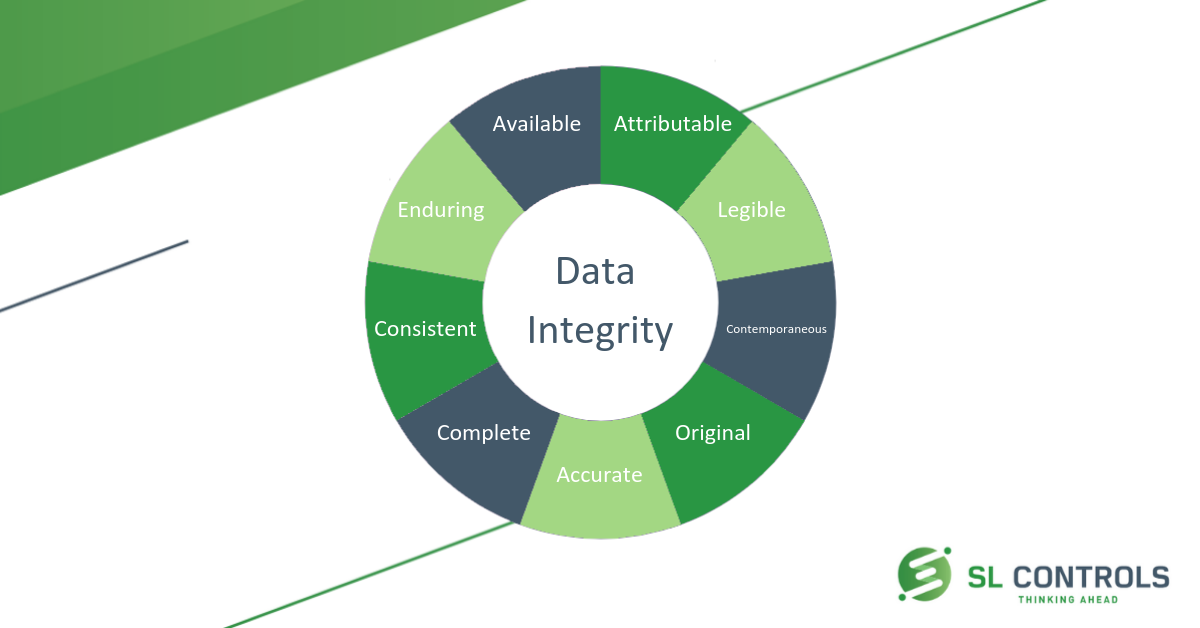
レコードを作成するときは、データを収集または生成した人またはコンピュータシステムのidを記録する必要があります。 また、コレクションまたは世代の日付を記録することも重要です。
読みやすい
データを読みやすいようにすることは、データを明確に読み取ること以上のことですが、手動でデータを記録する状況では重要です。 言葉を作ることができることは、しかし、電子データの問題のはるかに少ないです。
とはいえ、データが読みやすいようにすることは依然として関連性があります。 これは、データが記録されてから数年、さらには数十年後にデータを読み取って理解することが可能でなければならないためです。 これは、ノートブックに記録されたデータと同様に、デジタル記録されたデータとの関連性を持つことができます。
言い換えれば、データの発信者、もはや利用できなくなる可能性のある人から明確化を得ることなく、将来解読することが難しいかもしれないので、決まり文句や珍しい表現を使用することを避けることが重要です。
地域に関係なく、組織全体で一貫性のある、簡単な言語を使用することが最善のアプローチです。
同時
個人やシステムは、それが行われた時点での活動の記録を作ることが不可欠です。 電子データでは、これは通常の慣行であるため、これは手動の記録保持とより関連性のある別のポイントです。
オリジナル
レコードはコピーや転写ではなくオリジナルでなければなりません。 繰り返しになりますが、これは主に手動の記録保持に適用されます。 たとえば、後でメインレコードを完了することを意図して紙切れにレコードを書き込むべきではありません。
代わりに、データの元の記録は、その記録が紙の上にあるかデジタルシステム上にあるかにかかわらず、メインレコードにある必要があります。
正確な
すべてのレコードは、何が起こったのかの現実を反映し、エラーがないはずです。 また、元の情報を編集して、その情報が失われることはありません。
変更が必要な場合は、それらの変更を元の情報を参照できるように文書化する必要があります。 何も削除、ブロックアウト、または削除されるべきではありません。
データを電子的に記録する場合、システムには精度チェックと検証制御が組み込まれている必要があります。
Complete
記録されたすべてのデータは、削除または失われたものが何もないことを示すために監査証跡が必要です。
一貫性のある
これは主に、データが時系列であること、すなわち期待される順序にある日付とタイムスタンプを持つことを意味します。
これは以前の原則で触れられていますが、ALCOA+のこの原則は、データが記録されてから数十年後に利用可能であることを保証することに特に重点を置いています。
利用可能
この点は最後の点から続きます。 データは存在するだけでなく、アクセス可能でなければなりません。 これを達成する最も効率的な方法は、通常、データを電子的に記録することです。
データの整合性と検証
データの整合性は、医薬品および医療機器製造施設のすべての検証プロセスに不可欠です。 ALCOA+の原則に従うことは、この目標を達成するための最良の方法です。