El efecto Jahn-Teller, a veces también conocido como distorsión Jahn–Teller, describe la distorsión geométrica de moléculas e iones que está asociada con ciertas configuraciones electrónicas. Este efecto electrónico lleva el nombre de Hermann Arthur Jahn y Edward Teller, quienes demostraron, usando la teoría de grupos, que las moléculas degeneradas orbitales no pueden ser estables. El teorema de Jahn-Teller esencialmente establece que cualquier molécula no lineal con un estado fundamental electrónico espacialmente degenerado experimentará una distorsión geométrica que elimina esa degeneración, porque la distorsión reduce la energía general de la molécula.
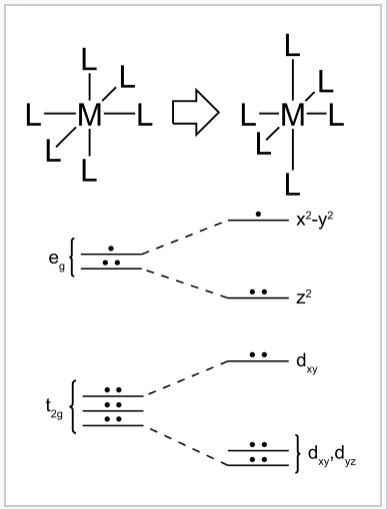
Distorsión Jahn-Teller de un complejo de metal de transición octaédrico d9. La distorsión tetragonal alarga los enlaces a lo largo del eje z a medida que los enlaces en el plano x-y se acortan. Este cambio disminuye la energía total, porque los dos electrones en el orbital dz2 bajan en energía a medida que el electrón en el orbital dx2-y2 sube.
Podemos entender este efecto en el contexto de complejos metálicos octaédricos considerando configuraciones de electrones d en las que el conjunto orbital eg contiene uno o tres electrones. Los más comunes son de alto espín d4 (por ejemplo, CrF2) , de bajo espín d7 (por ejemplo,NaNiO2) y d9 (por ejemplo, Cu2+). Si el complejo puede distorsionarse para romper la simetría, entonces uno de los orbitales (anteriormente) degenerados, por ejemplo, bajará en energía y el otro subirá. Más electrones ocuparán el orbital inferior que el superior, lo que resultará en una disminución general de la energía electrónica. Una distorsión similar puede ocurrir en complejos tetraédricos cuando los orbitales t2 están parcialmente llenos. Se dice que tales distorsiones geométricas que reducen la energía electrónica son impulsadas electrónicamente. Distorsiones similares impulsadas electrónicamente ocurren en compuestos de cadena unidimensionales, donde se denominan distorsiones Peierls, y en láminas unidas bidimensionalmente, donde se denominan ondas de densidad de carga.
El efecto Jahn-Teller se encuentra con mayor frecuencia en complejos octaédricos, especialmente complejos de cobre de seis coordenadas(II). La configuración electrónica d9 de este ion da tres electrones en los dos orbitales degenerados eg, lo que conduce a un estado fundamental electrónico doblemente degenerado. Tales complejos se distorsionan a lo largo de uno de los cuatro ejes moleculares (siempre etiquetados como eje z), lo que tiene el efecto de eliminar las degeneraciones orbitales y electrónicas y reducir la energía general. La distorsión normalmente toma la forma de alargar los enlaces a los ligandos que se encuentran a lo largo del eje z, pero ocasionalmente ocurre como un acortamiento de estos enlaces (el teorema de Jahn–Teller no predice la dirección de la distorsión, solo la presencia de una geometría inestable). Cuando se produce tal elongación, el efecto es reducir la repulsión electrostática entre el par de electrones en el ligando básico de Lewis y cualquier electrón en orbitales con un componente z, disminuyendo así la energía del complejo. Si se espera que el complejo no distorsionado tenga un centro de inversión, este se conserva después de la distorsión.
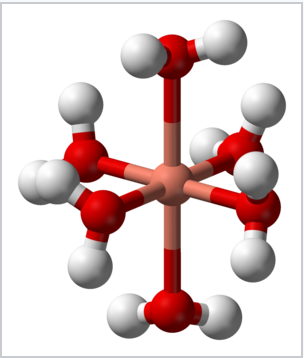
El efecto Jahn-Teller es responsable de la distorsión tetragonal del ion complejo hexaaquacopper(II), 2+, que de otro modo podría poseer geometría octaédrica. Las dos distancias axiales de Cu-O son 2.38 Å, mientras que las cuatro distancias ecuatoriales de Cu-O son ~1,95 Å.
En complejos octaédricos, el efecto Jahn-Teller es más pronunciado cuando un número impar de electrones ocupa los orbitales eg. Esta situación surge en complejos con las configuraciones d9, d7 de bajo espín o complejos d4 de alto espín, todos los cuales tienen estados fundamentales doblemente degenerados. En tales compuestos, los orbitales, por ejemplo, involucrados en la degeneración, apuntan directamente a los ligandos, por lo que la distorsión puede resultar en una gran estabilización energética. Estrictamente hablando, el efecto también ocurre cuando hay una degeneración debido a los electrones en los orbitales t2g (es decir, configuraciones como d1 o d2, ambas triplemente degeneradas). En tales casos, sin embargo, el efecto es mucho menos notable, porque hay una disminución mucho menor de la repulsión al tomar ligandos más lejos de los orbitales t2g, que no apuntan directamente a los ligandos (consulte la tabla a continuación). Lo mismo es cierto en los complejos tetraédricos (por ejemplo, manganato: la distorsión es muy sutil porque hay menos estabilización que ganar porque los ligandos no apuntan directamente a los orbitales.
Los efectos esperados para la coordinación octaédrica se presentan en la siguiente tabla:
| el Número de electrones d | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Alta/Baja Giro | HS | LS | SA | LS | SA | LS | SA | LS | ||||||
| la Fuerza de J-T Efecto | w | w | s | w | w | w | w | s | s | |||||
w: efecto Jahn–Teller débil (orbitales t2g desigualmente ocupados)
s: efecto Jahn-Teller fuerte esperado (por ejemplo, orbitales desigualmente ocupados)
en blanco: no se espera efecto Jahn–Teller.
El efecto Jahn-Teller se manifiesta en los espectros de absorbancia UV-VIS de algunos compuestos, donde a menudo causa la división de bandas. Es fácilmente evidente en las estructuras de muchos complejos de cobre(II). Se puede obtener información adicional y detallada sobre la anisotropía de tales complejos y la naturaleza de la unión del ligando a partir de la estructura fina de los espectros de resonancia de espín de electrones a baja temperatura.
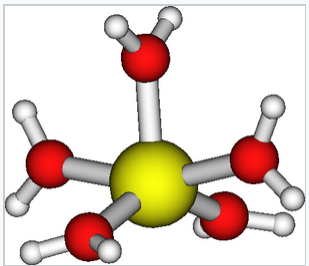
El ion Cu(II) también puede coordinar cinco moléculas de agua en una pirámide cuadrada alargada con cuatro enlaces Cu-Oeq (2×1, 98 Å y 2×1, 95 Å) y un enlace largo Cu-Oax (2,35 Å). Los cuatro ligandos ecuatoriales están distorsionados del plano ecuatorial medio en ± 17°.