nedávno jsem četl článek, který provedl off-hand odkaz na test 100% kyslíkového zkratu. Výsledky testu byly zahrnuty do analýzy dat, ale rovnice, které vědci použili, nebyly prezentovány ani na ně nebylo odkazováno, ani nebyl popsán postup. To je pravděpodobně proto, shunt frakce test a jeho rovnice jsou moc staré školy, plicní fyziologie, ale i v případě, že předmět je pravděpodobně zahrnuty v té či oné době ve fyziologii třídy mám podezření, že některé z otázek ve výpočtu nejsou tak dobře rozuměl, jak by měly být.
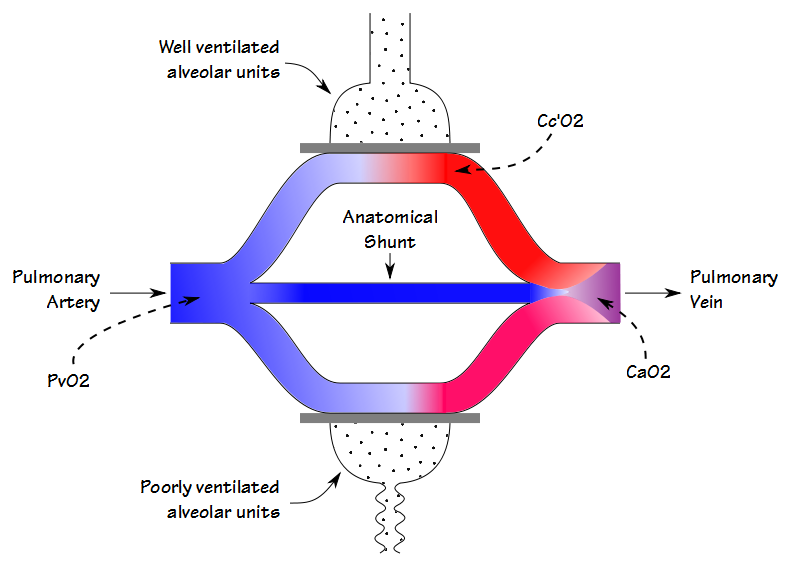
Tam jsou některé podobnosti mezi deadspace-dechový objem, poměr (Vd/Vt) a shunt frakce, ale i když jsou oba se podílejí na výměně plynů (a do jisté míry také korelují s každou další) jsou měření různých věcí. Když krev protéká do plic krev prochází dobře větraných plicních sklípků a stává se plně nasycený; krev prochází špatně větraných plicních sklípků a je pouze částečně nasycen; a někteří obchází plicní sklípky zcela. Výsledný obsah arteriálního kyslíku je součtem průměru všech těchto kompartmentů.
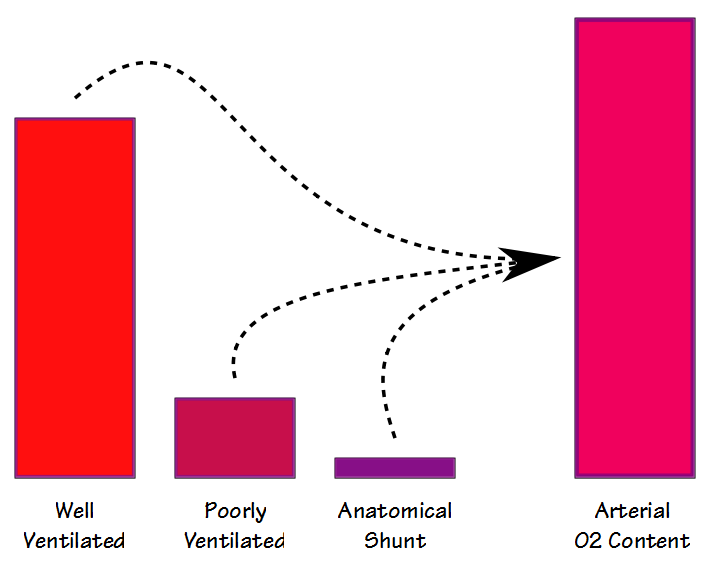
existují dva různé způsoby, jak lze měřit a vypočítat zkratovou frakci; fyziologické a anatomické. Fyziologický shunt rovnice může být provedena v každém FiO2 (ale obvykle kolem FiO2 na vzduchu v místnosti) a vyžaduje, aby arteriální a smíšené žilní krevní vzorky budou přijata více či méně současně, a pak analyzovány na PO2 a SaO2. Základní vzorec je:
kde:
Qs = průtok krve přes bočník
Qt = celkový průtok krve
Cc’O2 = plicní kapilární obsah O2
CaO2 = arteriální obsah O2
CvO2 = smíšené žilní obsah O2
je obsah Kyslíku v ml kyslíku na litr krve a je vypočtena z:
Kde:
Hb = hemoglobin (g/decaliter)
SO2 = nasycení kyslíkem (%)
PO2 = parciální tlak kyslíku
plicní kapilární obsah O2 nelze měřit přímo (a přísně vzato to je více konceptuální hodnotu než skutečný) a je obvykle odhaduje z alveolární vzduch rovnice (přestože „ideální“ plicní kapilární krve již PO2 gradientu o 1 mm Hg z alveolárního vzduchu, je to bezvýznamný, že to je obvykle ignorován).
kde:
Pb = barometrický tlak v mm Hg
FiO2 = frakční koncentrace vdechovaného kyslíku
PaCO2 = arteriální parciální tlak CO2
RER = respirační výměnný poměr
obsah kyslíku V plicních kapilár je určena podle prvního odhadu saturace kyslíku z PAO2 a to může být provedeno buď vizuálně z kyslíku, disociační křivka:
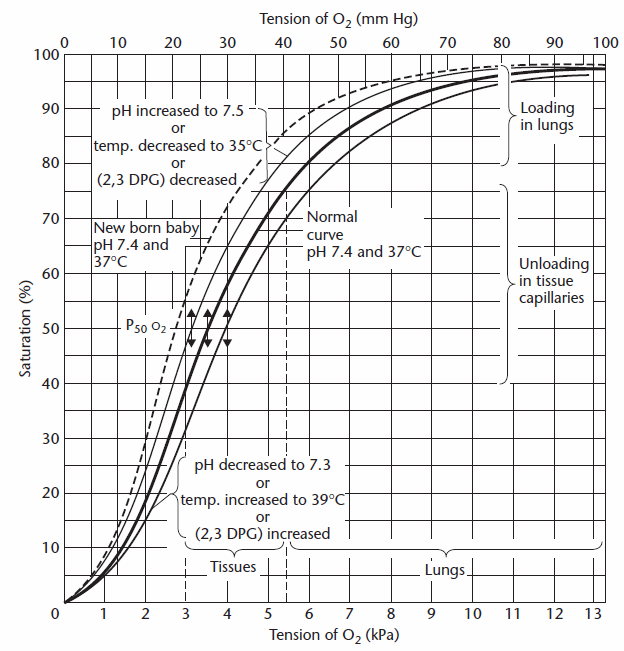
od Cotes et al, str. 260.
nebo ze Severinghausova vzorce:
a podle toho vypočítat Cc ‚ O2.
Poznámka: je Zajímavé, že ani kyslíku, disociační křivka ani Severinghaus vzorec vzít karboxyhemoglobinu (nebo methemoglobinu) v úvahu. Na to přijde, tento problém nebyl zahrnut do žádné z učebnicových diskusí shunt fraction, které jsem četl. COHb zkresluje vztah mezi PO2 a SO2 (směrem dolů, pokud pracujete z PO2 na SO2, směrem nahoru, pokud pracujete ze SO2 na PO2). Normální hladiny COHb u nekuřáků jsou 1-2 a je nepravděpodobné, že by toto množství COHb významně změnilo výpočty shunt frakce. Pokud však neexistují žádné pevné pokyny, pokud jsou přítomny vyšší hladiny COHb, měly by být pravděpodobně použity k odpovídající úpravě Cc ‚ O2.
Přičemž normální hodnoty a pracovat pozpátku, PAO2 je:
plicní kapilární nasycení kyslíkem je proto:
A plicní kapilární obsah kyslíku je:
Smíšené žilní krve nominálně má PO2 40 a saturace 75%, tak:
CaO2 se poté vypočte z individuální aktuální PaO2 a SaO2. V závislosti na konkrétních výsledcích bude shunt frakce:
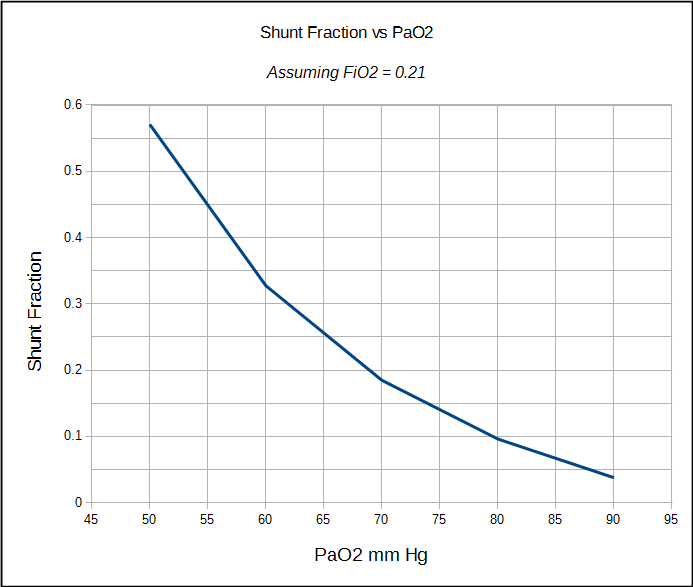
fyziologickou frakci zkratu lze vypočítat pouze tehdy, jsou-li známy jak arteriální, tak smíšená žilní PO2 a SO2. Z tohoto důvodu se nejčastěji provádí na kardiochirurgické klinice, operačním sále nebo jednotce intenzivní péče, kde jsou relativně běžné arteriální a centrální žilní linie. Výpočet fyziologického zkratu však nemůže rozlišovat mezi posunem způsobeným špatně větranými alveolárními jednotkami a anatomickým zkratem. Anatomický zkrat frakce lze vypočítat samostatným postupem však, a to je místo, kde 100% O2 test přichází do hry.
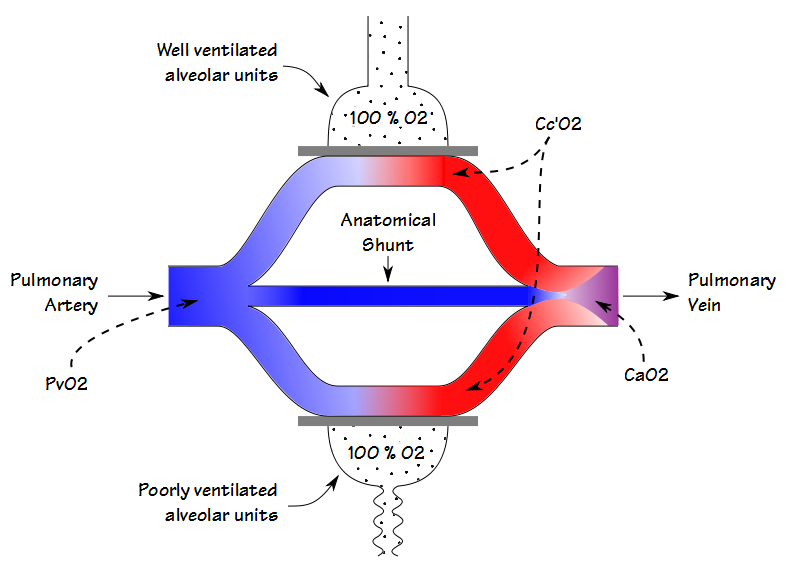
Tím, že dech pacienta 100% O2, dokud dusíku smyla z jejich plic (nominálně 20 minut), koncentrace kyslíku v i špatně větrané jednotky bude blížit 100%. To znamená, že parciální tlak a saturace krve opouštějící jak špatně, tak dobře větrané alveolární jednotky budou stejné. Z tohoto důvodu bude jakékoli snížení obsahu arteriálního kyslíku způsobeno pouze anatomickým zkratem.
Pokud má pacient zavedený centrální žilní katétr, výpočet anatomický zkrat může pokračovat stejným způsobem, jak již bylo podrobné. Pokud pouze arteriální vzorek může být získán (což je obvykle případ v PFT Lab) arteriální-venózní obsah O2 je rozdíl mezi 4.4 a 5.0 lze předpokládat, a shunt frakce odpovídajícím způsobem vypočítat.
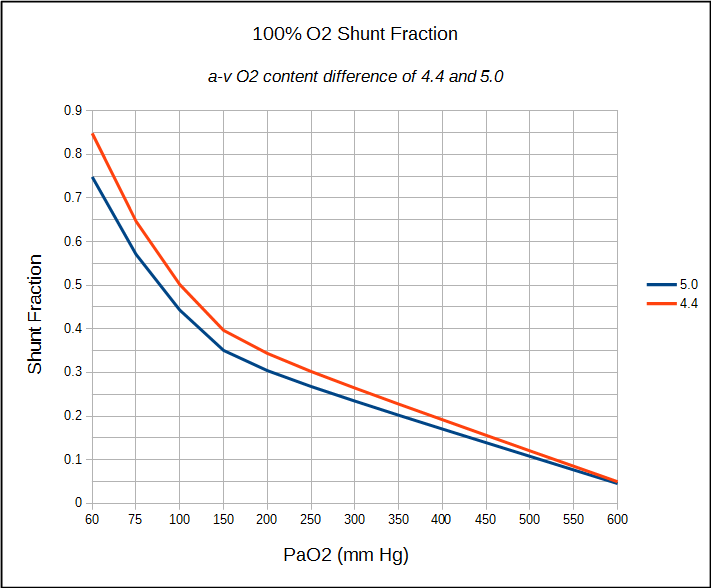
omezení shunt frakce výpočty v části s některými z předpokladů o běžných hodnot a v části s přesnost měření krevních plynů. Alveolární vzduch rovnice, například, se předpokládá, že respirační výměnný poměr (RER) je 0,8, ale jediný způsob, jak být jisti, je vlastně měření VO2 a VCO2. Přísně vzato, RER, která se liší od 0,8, pravděpodobně nebude mít významný rozdíl ve vypočtených PAO2, Sc ‚O2 a Cc‘ O2, ale stále je to předpoklad. Použití rozdílu obsahu a-v O2 4,4 až 5,0 na druhé straně je mnohem větší předpoklad. To je do jisté míry odůvodněno skutečností, že 100% test O2 se obvykle provádí v klidu a to jsou rozumné hodnoty pro jednotlivce v klidu, ale opět je to předpoklad.
Mnohem více, týkající se omezení v měření přesně PaO2 a SaO2, zejména na vyšší FiO2. Dvě různé studie ukázaly, že typ injekční stříkačky použity pro získání ABG (sklo versus plast) a jak to bylo uloženo (na ledě nebo při pokojové teplotě) udělala významný rozdíl ve vypočtené shunt frakce, i když ABG vzorky byly analyzovány rychle. Když došlo k delšímu čekání před analýzou, chyba v PaO2 by mohla způsobit, že vypočtená frakce zkratu bude dvakrát větší, než ve skutečnosti byla. Důvodem, proč k tomu dochází, je částečně difúze plastovými stříkačkami a částečně pokračující metabolismus ve vzorku krve, pokud je udržován při pokojové teplotě. Nejmenší množství změn bylo vidět, když skleněné stříkačky držely na ledu.
je zajímavé, že podobná studie se vzorky ABG odebranými při normálním FiO2 (PO2 ≈ 100) ukázala opačný účinek. Naměřený PO2 měl tendenci stoupat, opět více v plastových injekčních stříkačkách než ve skle, a opět to pravděpodobně kvůli difúzi. Zajímavé je, PO2 klesla ve skleněné injekční stříkačky uchovávány na ledu a autorů, Knowles et al, poukázat na to, že rozpustnost O2 stoupá, jak teplota klesá, a že s O2 v roztoku PO2 může snížit.
konečně jsou analyzátory krevních plynů obvykle kalibrovány pomocí koncentrací plynu v normálním fyziologickém rozmezí. Jakýkoli vzorek arteriální krve s PO2 nad 200 mm Hg je mimo tento rozsah a jsem znepokojen tím, jaký druh chybové lišty je pro PO2, které jsou ještě vyšší. Pretto et al použili tonometr krve s 95% O2 a 5% CO2, ale zajímavě nehlásili měřený PO2, ale pouze změnu PO2 v průběhu času. Smeenk et al získány vzorky krve od osob podstupujících 100% kyslíku testem jako předoperační posouzení koronárního bypassu a průměrná PO2 jejich zlatý standard vzorků (sklo, injekční stříkačky, ledový, 5 minut zpoždění) byla 590 mm Hg. To je A-a gradient kolem 80 mm Hg a může dobře být vhodné, ale také to znamená, že průměrná anatomické shunt frakce byla 10% a Cotes et al uvádí, že normální anatomické shunt pro jednotlivce ve stejném věkovém rozmezí je kolem 4%.
test shuntové frakce se běžně neprovádí v laboratořích plicních funkcí. Skutečné anatomické shunty jsou relativně vzácné a nejvhodnějším pacientem pro test 100% O2 shunt fraction by byl pacient se sníženým SaO2 v klidu, který se významně nezlepší s doplňkovým O2.
fyziologická shunt frakce by mohla být považována za zadní stranu Vd / Vt. Perfuze nehomogenity existují stejně jako větrání nehomogenity ale to může být přehlédnuty, protože vyšetření plicní funkce je orientován daleko více kolem větrání straně dýchání než perfuze straně. Ventilace a perfuzní nehomogenity jsou základními rysy mnoha plicních onemocnění. Z tohoto důvodu musí být zkrat frakce a rozdíly mezi jeho fyziologickými a anatomickými složkami součástí vzdělávání všech plicních technologů. Stejně jako Vd/VT však existují i omezení přesnosti výpočtu frakce bočníku jak z předpokladů, které mohou nebo nemusí být přiměřené, tak z přesnosti měření PO2 a SO2.
Aboab J, Louis B, Jonson B, Brochard L. Vztah mezi PaO2/FiO2 a FiO2: matematický popis. Kapitola Aplikovaná fyziologie v medicíně intenzivní péče, Pinsky MR, Brochard L, mancebo JM editoři. Springer-Verlag Heidelberg, 2006.
Conrad SA, Kinasewitz GT, George RB. Testování Plicních Funkcí. Principy a praxe. Churchill Livingston Publishing, 1984.
Cotes je, Chinn DJ, Miller Mr. Lung Function, 6th Edition. Blackwell Publishing, 2006.
Knowles TP, Mullin RA, Hunter JA, Douce FH. Účinky materiálu stříkačky, doba skladování a teplota vzorku na krevní plyny a saturace kyslíkem v arterializovaných vzorcích lidské krve. Respir Care 2006; 51 (7): 732-736.
Pretto JJ, Rochford PD. Účinky doby skladování vzorku, teploty a typu stříkačky na napětí krevních plynů ve vzorcích s vysokým tlakem kyslíku. Hrudník 1994; 49: 610-612.
Smeenk FWJM, Janssen JDJ, Arends BJ, Harff GA, van den Bosch JA, Schonberger JPAM, Postmus PE. Účinky čtyř různých metod na odběr arteriální krve a dobu skladování na napětí plynu a výpočet zkratu v testu 100% kyslíku. Eur Respir J 1997; 10: 910-913.

PFT Blog od Richarda Johnstona je licencován pod Creative Commons Attribution-NonCommercial 4.0 International License