Finegoldia magna er en strengt anaerob gram-positiv coccus som er en del av commensal flora av huden, munnhulen, mage-tarmkanalen og den kvinnelige urogenitale kanalen.1,2 vi beskriver et uvanlig tilfelle av en komplisert gluteal abscess forårsaket utelukkende av et opportunistisk patogen hos en pasient med diabetes mellitus som ikke hadde fått tidligere intramuskulære injeksjoner i det berørte området.
en 60 år gammel mann kom til akuttmottaket med intens smerte og pussdannelse i venstre rumpeballe som hadde begynt 2 uker tidligere. Pasientens tidligere historie inkluderte hypertensjon, dyslipidemi, overvekt (kroppsmasseindeks, 29), vitiligo, aktiv røyking (20 sigaretter per dag) og type 2 diabetes mellitus av 12 års varighet med god glykemisk kontroll uten tegn på metadiabetiske komplikasjoner (HbA1, 7%), selv om han rapporterte forverring av glykemisk kontroll hjemme de siste ukene, sammenfallende med den smittsomme prosessen. Pasienten rapporterte ingen tidligere gluteal intramuskulære injeksjoner. Han ble behandlet med acetylsalisylsyre (100 mg / 24 timer), atorvastatin (10 mg / 24 timer), glimepirid (2 mg/24 timer) og bisoprolol (5 mg/24 timer).
Fysisk undersøkelse viste en stor, smertefull, varm svingende hevelse på venstre bakke ledsaget av crepitus og aktiv suppuration, og et nekrotisk område på 10 cm (Fig . 1). Laboratorietester viste følgende: hemoglobin, 15 g / dL; leukocytter; 10 870 mm3; blodplater, 121 000 mm3; protrombintid, 16%; glukose, 370 mg/dL; urea, 67 mg/dL; kreatinin, 1,25 mg / dL; melkesyre 2 mmol / L; prokalsitonin, 1,19 ng / mL; C-reaktivt protein, 249 mg / L.
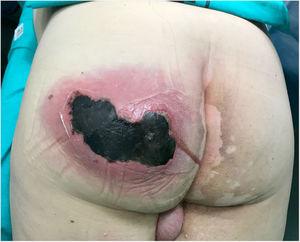
Abscess på venstre bakke med aktiv suppuration og et stort (10 cm) område av nekrose.
basert på de kliniske funnene gjennomgikk pasienten nøddrenering i operasjonen. En liter pus ble ekstrahert, prøver ble tatt for kultur, og bred eksisjon av det nekrotiske vevet ble utført. I den postoperative perioden viste pasienten et gunstig klinisk kurs, gjenopprette glykemisk kontroll og mobilitet og funksjonalitet i venstre ben.
Abscesskulturer var negative for aerobe bakterier og positive bare for strengt anaerobe gram-positive kokker, hvilken bakteriell typing identifisert Som F magna. Et antibiogram for f magna viste følsomhet overfor amoksicillin-klavulansyre, metronidazol og clindamycin, og ingen tegn på antibiotikaresistens. Pasienten ble tømt fra sykehus og foreskrevet antibiotikabehandling (metronidazol, 500 mg/8 h) og poliklinisk kirurgisk sårpleie, som han reagerte godt på.
f magna, tidligere Kjent Som Peptostreptococcus magnus, har gjennomgått flere taksonomiske endringer siden Den først ble beskrevet i 1933 Av Prevot, som brukte begrepet Diplococcus magnus.3
f magna er trolig den vanligste av alle gram-positive anaerobe kokker (GPAC) og den mest patogene formen som finnes i humane kliniske prøver. Denne mikroorganismen er en del av den normale biota og finnes hovedsakelig i huden, mage-tarmkanalen, kvinnelig genitourinary tract, og i mindre grad munnhulen.1,2 de siste årene har 2 viktige proteiner blitt identifisert som forklarer virulens og koloniseringskapasiteten Til f magna: overflateadhesjonsproteinet FAF (F magna adhesjonsfaktor) og subtilisin-lignende serinprotease SufA.2,4 I de øvre lagene av epidermis medierer FAF adhesjon ved binding til galektin-7, en keratinocyttcellemarkør. Etter at bakterier beveger seg dypere inn i huden og når basalmembranen, bryter SufA ned kollagen IV. i dermis interagerer FAF med kollagen V og fibrillin, som antagelig forklarer hvordan f magna kan nå de dypeste lagene av hudvev under infeksjon.5
f magna er en av de artene som oftest dyrkes fra abscesser i huden, bløtvev, bein og ledd, vanligvis i polymikrobielle kulturer, og i sjeldne tilfeller i rene kulturer.3 Postoperativ mediastinitt, ventilendokarditt og nekrotiserende pneumoni på Grunn Av f magna er beskrevet.6 bruken av bredspektret antibiotika som endrer hudmikrobiota, innføring av fremmede materialer (proteseklaffer, erstatningsledd, katetre) og en økning i antall pasienter behandlet med immunosuppressive stoffer favoriserer disse infeksjonene ved å skape et optimalt miljø for disse opportunistiske patogener.
Antimikrobiell resistens blant anaerobe bakterier øker over hele verden.7 De Fleste GPACs (> 90%) er følsomme for penicillin, og mange er også utsatt for andre β-laktamantibiotika,7-10, men viser økende resistens mot andre antibiotika som klindamycin, metronidazol og fluorokinoloner.8-10 Forekomst av klindamycin resistens blant GPACs varierer fra 7% til 20%, men øker i visse arter, inkludert F magna og Peptoniphilus arter.7 De Fleste GPACs er fortsatt utsatt for metronidazol, selv om noen metronidazolresistente stammer Av f magna og Parvimonas micra har blitt beskrevet.9
den foreliggende sak illustrerer hvordan commensal bakterien f magna er i stand til å produsere en avansert nekrotiserende infeksjon, og understreker viktigheten av artsnivå identifisering og bestemmelse av antimikrobiell følsomhet av anaerobe bakterier fra representative prøver når isolert i rene kulturer.
Interessekonflikter
forfatterne erklærer at de ikke har noen interessekonflikter.