10 Mai 2018, de către personalul NCI
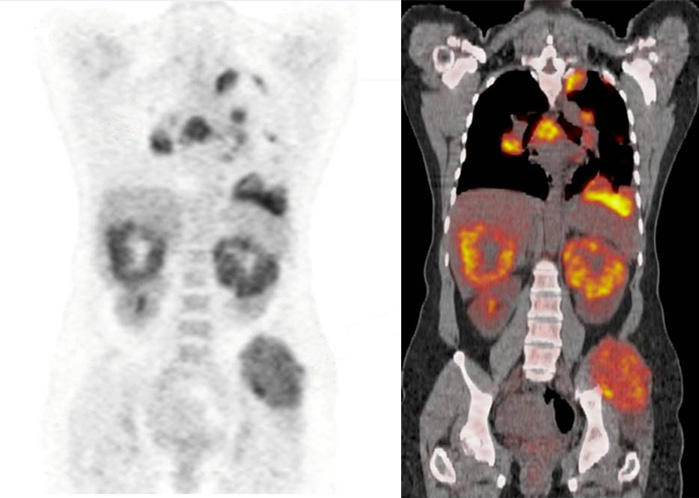
FDG PET/CT scanează de la un pacient cu carcinom renal metastatic.
pe 16 aprilie, Food and Drug Administration (FDA) a aprobat medicamentele de imunoterapie nivolumab (Opdivo) și ipilimumab (Yervoy) în combinație ca tratament inițial sau de primă linie pentru pacienții cu cancer renal avansat a căror boală are un prognostic intermediar sau slab.
acesta este primul regim de imunoterapie aprobat de FDA pentru tratamentul inițial al pacienților cu cancer renal. Nivolumab a fost aprobat anterior pentru a trata pacienții cu cancer renal avansat a căror boală s-a agravat după tratamentul cu terapie standard de primă linie.
noua aprobare s-a bazat pe rezultatele unui studiu clinic internațional de fază 3. În cadrul studiului, persoanele cu cancer renal avansat cu risc intermediar sau slab, care au primit combinația de imunoterapie, au trăit mai mult în general și au avut mai multe șanse de a – și micșora tumorile în comparație cu cei tratați cu sunitinib (Sutent). Rezultatele studiului, care a fost finanțat de Bristol-Myers Squibb și Ono Pharmaceutical, au fost raportate pe 5 Aprilie în New England Journal of Medicine (NEJM).
rezultate mai bune cu imunoterapia
studiul, numit CheckMate 214, a implicat aproape 1.100 de pacienți cu carcinom renal avansat netratat anterior (RCC), care este cel mai frecvent tip de cancer renal. (Pentru acest studiu, RCC avansat a fost definit ca cancer care nu a fost supus unei intervenții chirurgicale potențial curative sau radioterapie sau care a metastazat în alte zone ale corpului.)
participanții au fost repartizați aleatoriu pentru a primi fie nivolumab plus ipilimumab, ambele fiind inhibitori ai punctului de control imun, urmate de nivolumab în monoterapie ca terapie de întreținere, fie sunitinib, un inhibitor al angiogenezei care este un tratament standard pentru pacienții cu cancer renal avansat.
majoritatea pacienților din fiecare grup de tratament aveau boală cu risc intermediar sau slab. Oncologii folosesc factori de risc bine stabiliți pentru a clasifica pacienții cu cancer renal avansat în grupuri de risc favorabile, intermediare și slabe. Aproximativ 75% din toți pacienții cu cancer renal avansat au boală cu risc intermediar sau slab.
la 18 luni de la inițierea tratamentului, 75% dintre pacienții tratați cu combinația de imunoterapie erau încă în viață, comparativ cu 60% dintre cei tratați cu sunitinib. La o urmărire mediană de 25 de luni, supraviețuirea mediană globală pentru pacienții tratați cu combinația de imunoterapie nu a fost atinsă. Pentru pacienții tratați cu sunitinib, a fost de 26 de luni.
mai mulți pacienți cărora li s-a administrat combinația de imunoterapie decât sunitinib au prezentat un răspuns tumoral obiectiv (42% față de 27%), inclusiv răspunsuri complete (9% față de 1%), ceea ce înseamnă că cancerul lor nu mai era detectabil.
mai puțini pacienți din studiul clinic tratat cu nivolumab și ipilimumab decât cu sunitinib au prezentat reacții adverse grave (46% față de 63%). Cu toate acestea, mai mulți pacienți din grupul de imunoterapie au întrerupt tratamentul din cauza efectelor secundare (22% față de 12%). Au existat opt decese legate probabil de tratament în rândul pacienților tratați cu nivolumab și ipilimumab, au raportat cercetătorii studiului și patru în rândul pacienților tratați cu sunitinib.
în ciuda prevalenței efectelor secundare și a unui procent mai mare de pacienți care au întrerupt tratamentul, pacienții cărora li s-a administrat combinația de imunoterapie au raportat o calitate a vieții mai ridicată pe tot parcursul studiului.
pacienții cu boală cu risc favorabil s-au descurcat mai bine cu Sunitinib
îmbunătățirile ratelor de supraviețuire și răspuns tumoral observate la pacienții cu boală cu risc intermediar și slab tratați cu combinația de imunoterapie nu au fost observate la pacienții cu boală cu risc favorabil.
de fapt, în rândul pacienților cu RCC cu risc favorabil, cei tratați cu sunitinib au avut o rată de răspuns tumoral mai mare decât cei tratați cu nivolumab plus ipilimumab (52% față de 29%) și o supraviețuire mai lungă fără progresie (25,1 luni față de 15,3 luni), a remarcat Brendan D. Curti, MD., al Providence Cancer Institute, Portland, sau, într-un editorial însoțitor din NEJM.
autorii studiului au recunoscut rezultatele diferite pentru pacienții cu boală cu risc favorabil, dar au spus că rezultatele ar trebui „interpretate cu prudență din cauza naturii exploratorii a analizei, a eșantionului mic de subgrup și a imaturității datelor de supraviețuire.”Cu toate acestea, au continuat ei, rezultatele disparate” evidențiază necesitatea de a înțelege mai bine procesele biologice care stau la baza răspunsurilor la aceste două regimuri de tratament diferite.”
Eric Jonasch, MD., un oncolog genitourinar de la Universitatea din Texas MD Anderson Cancer Center, a adăugat că descoperirile la pacienții cu risc favorabil sugerează că tumorile lor pot avea o biologie diferită care ar putea fi definită de lipsa celulelor imune în micromediul tumoral.
„cred că trebuie să efectuăm studii suplimentare pentru a înțelege cu adevărat dintr-o perspectivă care sunt diferențele dintre pacienții cu risc favorabil, intermediar și slab”, a spus Dr.Jonasch, care nu a fost implicat în studiu.
trecând dincolo de blocarea alimentării cu sânge a tumorii
din 2005, FDA a aprobat numeroase medicamente precum sunitinib care vizează angiogeneza, creșterea de noi vase de sânge care hrănesc tumorile, pentru a trata cancerul renal. Spre deosebire de medicamentele antiangiogeneză, nivolumab și ipilimumab acționează prin blocarea proteinelor care descurajează sau atenuează un răspuns imun împotriva tumorilor.
noua aprobare va schimba probabil modul în care sunt tratați pacienții, a spus Dr.Jonasch. Acum, pacienții cu boală cu risc intermediar sau slab probabil vor primi nivolumab și ipilimumab ca tratament inițial, a sugerat el.
„cred că întrebarea cheie este acum care este strategia potrivită în ceea ce privește combinarea inhibitorilor punctului de control cu alți inhibitori ai punctului de control sau cu medicamente vizate precum lenvatinib sau cabozantinib și care sunt acele strategii care ne oferă răspunsuri complete și răspunsuri durabile”, a spus Dr.Jonasch.
mecanismele biologice care stau la baza motivului pentru care tumorile răspund și dezvoltă rezistență la aceste strategii de tratament trebuie studiate, astfel încât clinicienii să poată identifica mai bine persoanele care ar putea beneficia cel mai probabil de o anumită strategie, a explicat el.
atât Dr.Jonasch, cât și Dr. Curti sugerează că rata de răspuns completă observată cu combinația de imunoterapie mută bara pentru tratarea pacienților cu RCC avansat.
„rata de răspuns completă de 9% va fi probabil noul standard pe care ne vom strădui să îl depășim pe măsură ce încercăm să îmbunătățim aceste rezultate”, a spus Dr.Jonasch.