10. Mai 2018 von NCI-Mitarbeitern
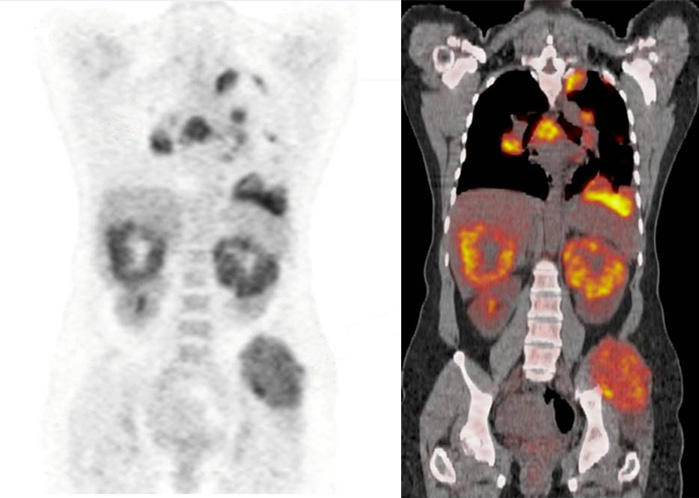
FDG PET / CT-Scans von einem Patienten mit metastasiertem Nierenzellkarzinom.
Am 16. April genehmigte die Food and Drug Administration (FDA) die Immuntherapeutika Nivolumab (Opdivo) und Ipilimumab (Yervoy) in Kombination als Erstbehandlung oder First-Line-Behandlung für Patienten mit fortgeschrittenem Nierenkrebs, deren Krankheit eine mittlere oder schlechte Prognose hat.
Dies ist das erste Immuntherapieschema, das von der FDA für die Erstbehandlung von Patienten mit Nierenkrebs zugelassen wurde. Nivolumab wurde zuvor zur Behandlung von Patienten mit fortgeschrittenem Nierenkrebs zugelassen, deren Erkrankung sich nach der Behandlung mit einer Standard-Erstlinientherapie verschlimmert hatte.
Die neue Zulassung basierte auf den Ergebnissen einer internationalen klinischen Phase-3-Studie. In der Studie lebten Menschen mit fortgeschrittenem Nierenkrebs mit mittlerem oder geringem Risiko, die die Immuntherapiekombination erhielten, insgesamt länger und schrumpften häufiger als diejenigen, die mit Sunitinib (Sutent) behandelt wurden. Die Ergebnisse der Studie, die von Bristol-Myers Squibb und Ono Pharmaceutical finanziert wurde, wurden am 5. April im New England Journal of Medicine (NEJM) veröffentlicht.
Bessere Ergebnisse mit Immuntherapie
Die Studie mit dem Namen CheckMate 214 umfasste fast 1.100 Patienten mit zuvor unbehandeltem fortgeschrittenem Nierenzellkarzinom (RCC), der häufigsten Art von Nierenkrebs. (Für diese Studie wurde fortgeschrittenes RCC als Krebs definiert, der einer potenziell kurativen Operation oder Strahlentherapie nicht zugänglich war oder der in andere Bereiche des Körpers metastasiert war.)
Die Teilnehmer erhielten nach dem Zufallsprinzip entweder Nivolumab plus Ipilimumab, beides Immun-Checkpoint-Inhibitoren, gefolgt von Nivolumab allein als Erhaltungstherapie oder Sunitinib, einem Angiogenesehemmer, der eine Standardbehandlung für Patienten mit fortgeschrittenem Nierenkrebs darstellt.
Die Mehrheit der Patienten in jeder Behandlungsgruppe hatte eine Erkrankung mit mittlerem oder geringem Risiko. Onkologen verwenden gut etablierte Risikofaktoren, um Patienten mit fortgeschrittenem Nierenkrebs in günstige, mittlere und arme Risikogruppen einzuteilen. Ungefähr 75% aller Patienten mit fortgeschrittenem Nierenkrebs haben eine Erkrankung mit mittlerem oder geringem Risiko.
18 Monate nach Beginn der Behandlung lebten noch 75% der mit der Immuntherapiekombination behandelten Patienten, verglichen mit 60% der mit Sunitinib behandelten Patienten. Bei einer medianen Nachbeobachtungszeit von 25 Monaten wurde das mediane Gesamtüberleben der mit der Immuntherapiekombination behandelten Patienten nicht erreicht. Bei Patienten, die mit Sunitinib behandelt wurden, waren es 26 Monate.
Mehr Patienten, die der Immuntherapiekombination zugeordnet wurden als Sunitinib, zeigten ein objektives Tumoransprechen (42% gegenüber 27%), einschließlich eines vollständigen Ansprechens (9% gegenüber 1%), was bedeutet, dass ihr Krebs nicht mehr nachweisbar war.
Bei weniger Patienten in der Studie, die mit Nivolumab und Ipilimumab behandelt wurden als mit Sunitinib, traten schwerwiegende Nebenwirkungen auf (46% gegenüber 63%). Mehr Patienten in der Immuntherapiegruppe brachen die Behandlung jedoch aufgrund von Nebenwirkungen ab (22% gegenüber 12%). Es gab acht Todesfälle wahrscheinlich im Zusammenhang mit der Behandlung bei Patienten, die mit nivolumab und ipilimumab, die Studie Forscher berichteten, und vier bei Patienten, die mit sunitinib.
Trotz der Prävalenz von Nebenwirkungen und eines höheren Prozentsatzes der Patienten, die die Behandlung abbrachen, berichteten Patienten, die die Immuntherapiekombination erhielten, über eine höhere Lebensqualität während der gesamten Studie.
Patienten mit günstiger Risikoerkrankung schnitten mit Sunitinib besser ab
Die Verbesserungen des Überlebens und der Tumoransprechraten bei Patienten mit intermediärer und schlechter Risikoerkrankung, die mit der Immuntherapiekombination behandelt wurden, wurden bei Patienten mit günstiger Risikoerkrankung nicht beobachtet.
Tatsächlich hatten die mit Sunitinib behandelten Patienten unter Patienten mit RCC mit günstigem Risiko eine höhere Tumoransprechrate als die mit Nivolumab plus Ipilimumab behandelten (52% gegenüber 29%) und ein längeres progressionsfreies Überleben (25, 1 Monate gegenüber 15, 3 Monate), bemerkte Brendan D. Curti, M.D., des Providence Cancer Institute, Portland, OR, in einem begleitenden Leitartikel in NEJM.
Die Autoren der Studie räumten die unterschiedlichen Ergebnisse für Patienten mit Hochrisikoerkrankungen ein, sagten jedoch, dass die Ergebnisse „aufgrund des explorativen Charakters der Analyse, der kleinen Untergruppenstichprobe und der Unreife der Überlebensdaten mit Vorsicht interpretiert werden sollten.“ Die unterschiedlichen Ergebnisse unterstreichen jedoch die Notwendigkeit, die zugrunde liegenden biologischen Prozesse, die die Reaktionen auf diese beiden verschiedenen Behandlungsschemata antreiben, besser zu verstehen.“
Dr.Eric Jonasch., ein urogenitaler Onkologe am MD Anderson Cancer Center der University of Texas, fügte hinzu, dass die Ergebnisse bei Risikopatienten darauf hindeuten, dass ihre Tumoren eine andere Biologie haben könnten, die durch einen Mangel an Immunzellen in der Tumormikroumgebung definiert werden könnte.
„Ich denke, wir müssen weitere Studien durchführen, um wirklich aus einer Perspektive zu verstehen, was die Unterschiede zwischen günstigen, mittleren und armen Risikopatienten sind“, sagte Dr. Jonasch, der nicht an der Studie beteiligt war.
Über die Blockierung der Tumorblutversorgung hinausgehen
Seit 2005 hat die FDA zahlreiche Medikamente wie Sunitinib zugelassen, die auf die Angiogenese abzielen, das Wachstum neuer Blutgefäße, die Tumore nähren, zur Behandlung von Nierenkrebs. Im Gegensatz zu Antiangiogenese-Medikamenten blockieren Nivolumab und Ipilimumab Proteine, die eine Immunantwort gegen Tumore abschrecken oder dämpfen.
Die neue Zulassung wird wahrscheinlich die Behandlung von Patienten verändern, sagte Dr. Jonasch. Jetzt, Patienten mit Intermediate-oder poor-risk-Krankheit wahrscheinlich erhalten nivolumab und ipilimumab als Ihre erste Behandlung, schlug er vor.
„Ich denke, die Schlüsselfrage ist jetzt, was die richtige Strategie in Bezug auf die Kombination von Checkpoint-Inhibitoren mit anderen Checkpoint-Inhibitoren oder mit gezielten Medikamenten wie Lenvatinib oder Cabozantinib ist und was diese Strategien uns in Bezug auf vollständige Antworten und dauerhafte Antworten geben“, sagte Dr. Jonasch.
Die zugrunde liegenden biologischen Mechanismen, warum Tumore auf diese Behandlungsstrategien ansprechen und Resistenzen entwickeln, müssen untersucht werden, damit Kliniker Personen besser identifizieren können, die am wahrscheinlichsten von einer bestimmten Strategie profitieren, erklärte er.
Sowohl Dr. Jonasch als auch Dr. Curti legen nahe, dass die vollständige Ansprechrate der Immuntherapiekombination die Messlatte für die Behandlung von Patienten mit fortgeschrittenem RCC höher legt.
„Die vollständige Ansprechrate von 9% wird wahrscheinlich der neue Standard sein, den wir übertreffen werden, wenn wir versuchen, diese Ergebnisse zu verbessern“, sagte Dr. Jonasch.