jag läste nyligen en artikel som gjorde en hänvisning till 100% syre shuntfraktionstest. Resultaten från testet inkluderades i dataanalysen men ekvationerna som forskarna använde presenterades inte heller refererades de, inte heller beskrivs proceduren. Detta beror förmodligen på att shuntfraktionstestet och dess ekvationer är mycket gamla skolan lungfysiologi men även om ämnet förmodligen är täckt vid en eller annan tidpunkt i fysiologiklasser misstänker jag att några av de frågor som är involverade i beräkningen inte är så väl förstådda som de borde vara.
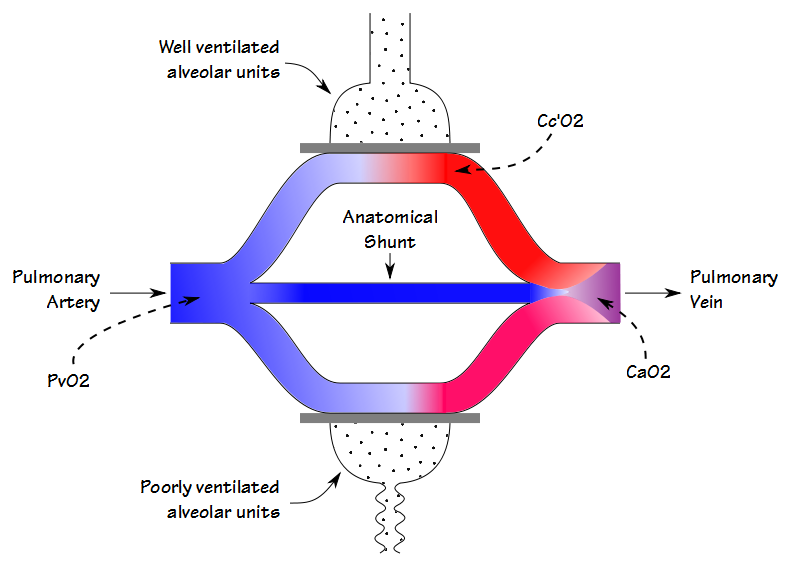
det finns vissa likheter mellan deadspace-tidal volume ratio (Vd/Vt) och shuntfraktionen men även om de båda är involverade i gasutbyte (och till viss del korrelerar de också med varandra) mäter de olika saker. När blodet flyter genom lungan passerar lite blod genom väl ventilerade alveoler och blir helt mättat; lite blod passerar genom dåligt ventilerade alveoler och är endast delvis mättat; och vissa kringgår alveolerna helt. Den resulterande arteriella syrehalten är det summerade genomsnittet av alla dessa fack.
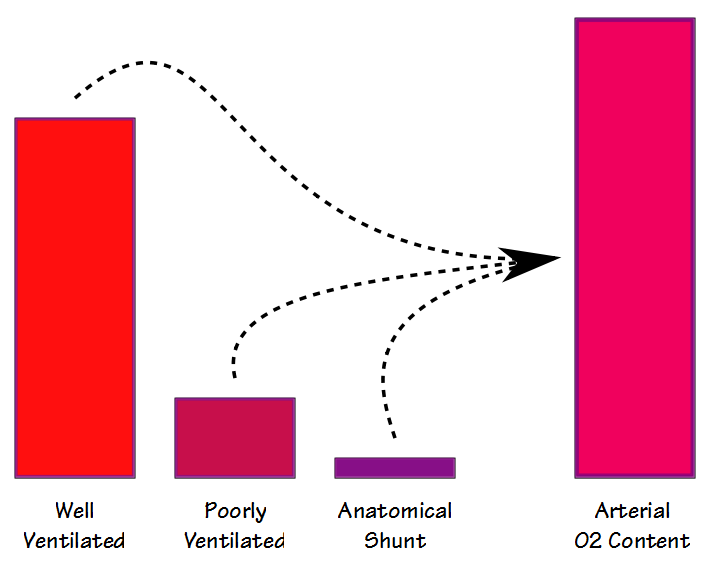
det finns två olika sätt att shuntfraktion kan mätas och beräknas; fysiologiska och anatomiska. Den fysiologiska shuntekvationen kan utföras vid vilken FiO2 som helst (men vanligtvis runt FiO2 i rumsluften) och kräver att arteriella och blandade venösa blodprover tas mer eller mindre samtidigt och sedan analyseras för PO2 och SaO2. Den grundläggande formeln är:
där:
Qs = blodflöde genom shunt
Qt = totalt blodflöde
Cc ’ O2 = pulmonell kapillär O2-innehåll
CaO2 = arteriell O2-innehåll
CvO2 = blandad venös O2-innehåll
syreinnehåll är milliliter syre per liter blod och är beräknat från:
där:
Hb = hemoglobin (gram/decaliter)
SO2 = syremättnad (%)
PO2 = syrepartialtryck
lungkapillär O2-innehållet kan inte mätas direkt (och strängt taget är det mer av ett konceptuellt värde än ett verkligt) och uppskattas vanligtvis från den alveolära luftekvationen (även om ”idealiskt” lungkapillärblod har en PO2-gradient på cirka 1 mm Hg från alveolär luft detta är obetydligt nog att det vanligtvis ignoreras).
där:
Pb = barometertryck i mm Hg
FiO2 = fraktionerad koncentration av inspirerat syre
PaCO2 = arteriellt partiellt tryck av CO2
RER = andningsutbytesförhållande
syreinnehållet i lungkapillärerna bestäms genom att först uppskatta syremättnaden från PAO2 och detta kan göras antingen visuellt från syremättnaden i lungkapillärerna dissociationskurva:
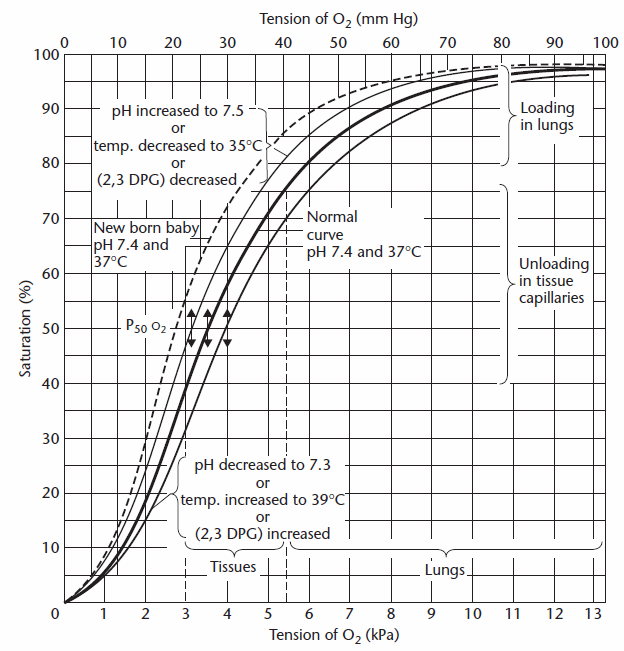
från Cotes et al, Sid. 260.
eller från Severinghaus formel:
och sedan beräkna Cc ’ O2 i enlighet därmed.
Obs: intressant tar varken syredissociationskurvan eller Severinghaus formel hänsyn till karboxihemoglobin (eller metemoglobin). För den delen har denna fråga inte inkluderats i någon av läroboksdiskussionerna om shuntfraktion som jag har läst. COHb snedvrider förhållandet mellan PO2 och SO2 (nedåt om du arbetar från PO2 till SO2, uppåt om du arbetar från SO2 till PO2). Normala COHb-nivåer hos icke-rökare är 1-2 och denna mängd COHb är osannolikt att göra en signifikant skillnad i shuntfraktionsberäkningarna. I avsaknad av några fasta riktlinjer bör de dock, när högre nivåer av COHb finns, troligen användas för att justera Cc ’ O2 i enlighet därmed.
med normala värden och arbetar bakåt är PAO2:
den lungkapillära syremättnaden är därför:
och lungkapillärsyreinnehållet är:
Blandat venöst blod har nominellt en PO2 av 40 och en syremättnad på 75%, så:
CaO2 beräknas sedan utifrån en individs faktiska PaO2 och SaO2. Beroende på de specifika resultaten kommer shuntfraktionen att vara:
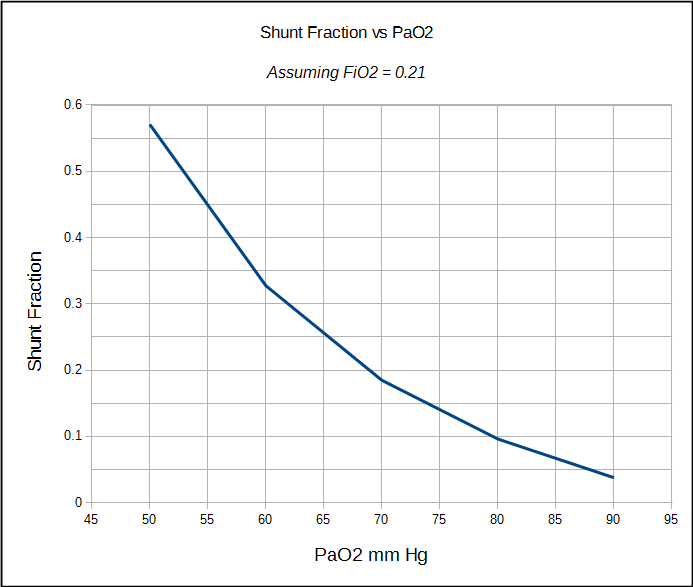
den fysiologiska shuntfraktionen kan endast beräknas när både arteriell och blandad venös PO2 och SO2 är kända. Av denna anledning är det oftast utförs i en hjärt cath lab, operationssalen eller intensivvårdsavdelning där inneboende arteriella och centrala venösa linjer är relativt vanliga. Den fysiologiska shuntberäkningen kan dock inte skilja mellan växling orsakad av dåligt ventilerade alveolära enheter och från en anatomisk shunt. Den anatomiska shuntfraktionen kan dock beräknas med ett separat förfarande, och det är här 100% O2-testet spelar in.
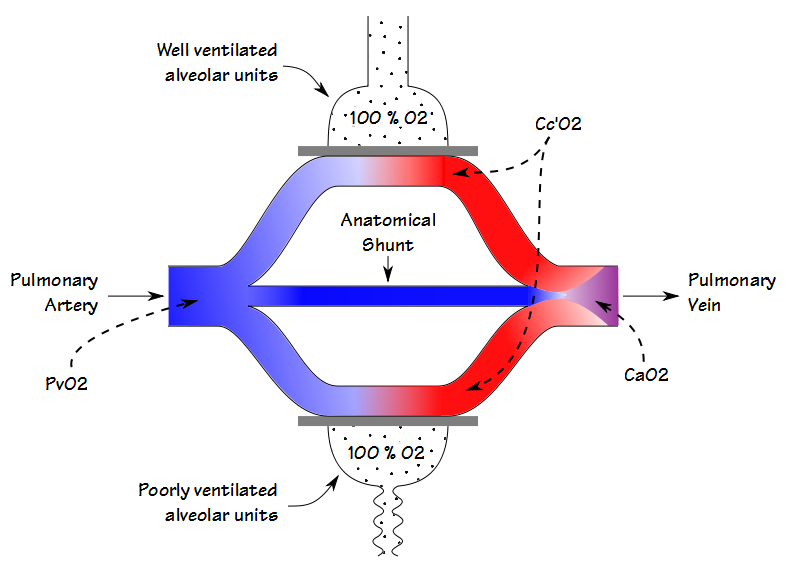
genom att patienten andas 100% O2 tills kvävet har tvättats ur lungan (nominellt 20 minuter) kommer syrekoncentrationen i även dåligt ventilerade enheter att närma sig 100%. Detta innebär att partialtrycket och mättnaden av blod som lämnar både de dåligt och de välventilerade alveolära enheterna kommer att vara desamma. Av denna anledning kommer någon minskning av arteriellt syreinnehåll enbart att bero på en anatomisk shunt.
om en patient har en inbyggd central venkateter kan beräkningen av anatomisk shunt fortsätta på samma sätt som redan detaljerad. Om endast ett arteriellt prov kan erhållas (vilket vanligtvis är fallet i ett PFT-laboratorium) kan en arteriell-venös O2-innehållsskillnad mellan 4,4 och 5,0 antas och shuntfraktionen beräknas i enlighet därmed.
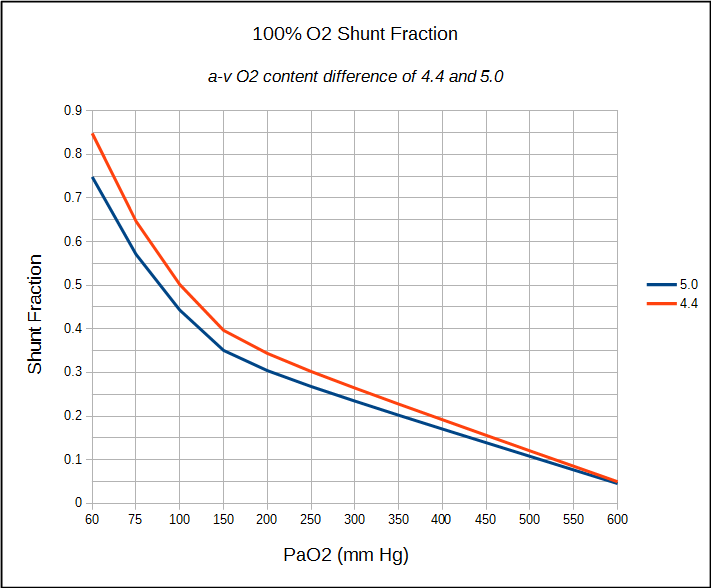
begränsningarna i shuntfraktionsberäkningarna måste delvis göras med några av antagandena om normala värden och delvis med noggrannheten i blodgasmätningar. Den alveolära luftekvationen antar till exempel att andningsutbytesrationen (RER) är 0,8 men det enda sättet att vara säker är att faktiskt mäta VO2 och VCO2. Strängt taget kommer en RER som skiljer sig från 0.8 förmodligen inte att göra någon signifikant skillnad i beräknad PAO2, Sc ’O2 och Cc’ O2, men det är fortfarande ett antagande. Att använda en A-v O2-innehållsskillnad på 4,4 till 5,0 å andra sidan är ett mycket större antagande. Det motiveras till viss del av det faktum att 100% O2-testet vanligtvis görs i vila och dessa är rimliga värden för en individ i vila men igen är det ett antagande.
långt mer om är begränsningarna i exakt mätning PaO2 och SaO2, särskilt vid högre FiO2 s. två olika studier har visat att den typ av spruta som används för att erhålla en ABG (glas kontra plast) och hur den lagrades (på is eller vid rumstemperatur) gjorde en signifikant skillnad i den beräknade shuntfraktionen även när ABG-proverna analyserades snabbt. När det var en längre väntan innan analysen kunde felet i PaO2 orsaka att den beräknade shuntfraktionen var dubbelt så stor som den verkligen var. Anledningen till att detta händer beror delvis på diffusion genom plastsprutorna och delvis på fortsatt metabolism i ett blodprov när det hålls vid rumstemperatur. Minsta förändring sågs när glassprutor hölls på is.
intressant nog visade en liknande studie med ABG-prover som tagits vid normal FiO2 (PO2 Macau 100) motsatt effekt. Den uppmätta PO2 tenderade att stiga, igen mer i plastsprutor än i glas, och igen detta troligen på grund av diffusion. Intressant, PO2 föll i glassprutor hålls på is och författarna, Knowles et al, påpeka att lösligheten av O2 stiger när temperaturen sjunker och att med mer O2 i lösning PO2 kan minska.
slutligen kalibreras blodgasanalysatorer vanligtvis med gaskoncentrationer i det normala fysiologiska området. Alla arteriella blodprov med PO2 över 200 mm Hg ligger långt utanför detta intervall och jag är oroad över vilken typ av felfält det finns för PO2 som är ännu högre. Pretto et al använde blodtonometerat med 95% O2 och 5% CO2 men intressant rapporterade de inte den uppmätta PO2 utan bara förändringen i PO2 över tiden. Smeenk et al erhöll blodprover från individer som genomgick 100% syretest som en pre-op-bedömning för koronar bypassoperation och den genomsnittliga PO2 av deras guldstandardprover (glasspruta, is, 5 minuters fördröjning) var 590 mm Hg. Detta är en a-a-gradient på cirka 80 mm Hg och kan mycket väl vara lämplig, men det betyder också att den genomsnittliga anatomiska shuntfraktionen var 10% och Cotes et al indikerar att den normala anatomiska shunten för individer i samma åldersintervall är cirka 4%.
shuntfraktionstestet utförs vanligtvis inte i lungfunktionslaboratorier. Sanna anatomiska shuntar är relativt sällsynta och den mest lämpliga patienten för 100% O2 shuntfraktionstest skulle vara en med en reducerad SaO2 i vila som inte förbättras signifikant med kompletterande O2.
den fysiologiska shuntfraktionen kan betraktas som baksidan av Vd/Vt. Perfusionsinhomogeniteter existerar lika mycket som ventilationsinhomogeniteter men detta kan förbises eftersom lungfunktionstestning är orienterad mycket mer runt ventilationssidan av andning än perfusionssidan. Ventilation och perfusionsinhomogeniteter är kärnfunktioner hos många lungsjukdomar. Av denna anledning måste shuntfraktionen och skillnaderna mellan dess fysiologiska och anatomiska komponenter vara en del av utbildningen av alla lungtekniker. Liksom Vd / Vt finns det dock också begränsningar för noggrannheten i shuntfraktionsberäkningen både från antaganden som kanske eller inte är rimliga och från mätnoggrannheten för PO2 och SO2.
Aboab J, Louis B, Jonson B, Brochard L. förhållandet mellan PaO2 / FiO2 och FiO2: en matematisk beskrivning. Kapitel i tillämpad fysiologi i intensivvård medicin, Pinsky MR, Brochard L, Mancebo JM redaktörer. Springer-Verlag Heidelberg, 2006.
Conrad SA, Kinasewitz GT, George RB. Lungfunktionstestning. Principer och praxis. Churchill Livingston Publishing, 1984.
Cotes JE, Chinn DJ, Miller Mr. lungfunktion, 6: e upplagan. Blackwell Publishing, 2006.
Knowles TP, Mullin RA, jägare JA, Douce FH. Effekter av sprutmaterial, provlagringstid och temperatur på blodgaser och syremättnad i arterialiserade humana blodprover. Respir Vård 2006; 51 (7): 732-736.
Pretto JJ, Rochford PD. Effekter av provlagringstid, temperatur och spruttyp på blodgasspänningar i prover med högt syretryck. Thorax 1994; 49: 610-612.
Smeenk FWJM, Janssen JDJ, Arends BJ, Harff GA, Van Den Bosch JA, Schonberger JPAM, Postmus PE. Effekter av fyra olika metoder på provtagning av arteriellt blod och lagringstid på gasspänningar och shuntberäkning i 100% syretest. Eur Respir J 1997; 10: 910-913.

PFT Blog av Richard Johnston är licensierad under en Creative Commons Attribution-NonCommercial 4.0 Internationell licens