INTRODUCTION
sen varhaisesta kuvauksesta lähtien vuonna 1924 Libman-Sacks-endokardiittia on pidetty systeemisen lupus erythematosuksen (SLE) tyypillisimpänä sydänhäiriönä, joskaan ei yleisimpänä.
SLE: n endokardiaalisen häiriön esiintymistiheys vaihtelee käytetyn diagnostisen tekniikan mukaan, vaikka kliininen diagnoosi on melko harvinainen. Joidenkin kirjoittajien kokemuksen mukaan vauriot ovat kliinisesti merkittäviä vain 20%: lla potilaista1 ja etenevät yleensä hitaasti sen jälkeen, kun heillä on ollut tauti monta vuotta.1,2
niissä harvoissa tapauksissa, joissa kirurginen venttiilien korjaus on tarpeen, bioprosteettisia venttiilejä ei suositella, koska ne voivat johtaa Libman-säkkeihin endokardiittiin3; tästä on kuitenkin kiistaa lääketieteellisessä kirjallisuudessa.
meillä on Libman-Sacks endokardiitti, johon liittyy mitraaliläppä ja joka etenee nopeasti vaikeaksi regurgitaatioksi, jota hoidetaan mitraalilaskennan kautta tehdyllä korjaavalla leikkauksella.
kliininen tapaus
36-vuotias nainen, jolla on diagnosoitu sidekudossairaus, jolla on puutteelliset SLE: n kliiniset kriteerit 8 vuoden ajan, pienen verisuonen vaskuliitti ja toistuvat keskenmenot, ilman aikaisempia kardiologisia oireita.
myönsi lepoon hengenahdistusta ja merkittyä veristä ysköstä; at exploration hän esitteli takypnea, lisääntynyt keskuslaskimopaine, kahdenväliset rales jopa keski keuhko kenttä, ja grade IV/VI pansystolic mitral sivuääni. Hänellä oli myös distaalisia vaskuliittivaurioita sormissa ja varpaissa. Rutiinianalyysi paljasti anemian hemoglobiinin ollessa 9,3 g / dL. Toistuva testaus fosfolipidivasta-aineiden osoittautui negatiiviseksi.
EKG: ssä todettiin sinustakykardia ilman muita siihen liittyviä anomalioita. Keuhkoröntgenissä näkyi lievä kardiomegalia ja bilateraalinen basilaarinen interstitiaalinen keuhko.
Transthorasic ja transesofageaalinen kaikukardiografia osoittivat, että molemmissa mitraaliläpissä oli 2-3 mm: n nodulaarisia nodulaarisia paksunokkeja, jotka viittasivat Libman-Sacks endokardiittiin (Kuva 1) ja vaikeaan mitraaliseen regurgitaatioon (kuva 2). Molempien kammioiden systolinen koko ja toiminta säilyivät.
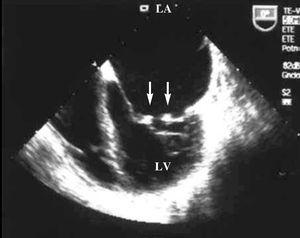
Kuva 1. Transesofageaalinen kaikukardiogrammi: apical 4-chamber projection jossa pieniä kasvupaikkoja voidaan havaita molemmissa mitraaliläpissä (nuolissa). LA osoittaa vasenta eteistä, LV vasenta kammiota.

kuva 2. Transesofageaalinen kaikukardiogrammi: 79 asteen projektio, jossa vaikea mitraalinen pulauttelu visualisoidaan. LA osoittaa vasenta eteistä, LV vasenta kammiota.
Transthorasinen kaikukardiografia tehtiin 2 vuotta aiemmin. Mitraaliläpässä havaittiin muutaman millimetrin kokoisia nodulaarisia paksunnoksia ja Libman-Sacks-endokardiitin kanssa yhteensopivaa lievää mitraalista pulauttelua.
koska epäiltiin keuhkovaltimon sisäistä verenvuotoa, pyydettiin korkean resoluution tietokonetomografiaa, joka vahvisti diagnoosin (kuvissa näkyy molemminpuolisia massoja, joissa on lasimurskaa).
evoluutio
suuriannoksisen kortikosteroidihoidon ja intensiivisen diureettihoidon jälkeen hemoptyysi eliminoitui ja huomattava sydämen vajaatoiminta saatiin hallintaan. Potilas pysyi kuitenkin toimintakykyluokassa III, minkä vuoksi läppävikaa hoidettiin 4 kuukauden kuluttua ensimmäisestä sisäänotosta kehonulkoisella leikkauksella ja mitraaliläpän korjauksella (tämän potilaan suuren verenvuotoriskin vuoksi) Carpentier-renkaalla.
venttiilin makroskooppisessa visualisoinnissa näkyi 2-3 mm granuloomaa ja patologisessa anatomiassa fragmentteja, joissa oli fibriinikerrostumia ja epäspesifisiä fokaalisia kalkkeutumia, mutta jotka olivat yhteensopivia kliinisen diagnoosin kanssa.
vuotta myöhemmin potilaalla ei ollut kardiologisia oireita; sydämen ultraäänitutkimuksessa näkyi lievä mitraalinen pulauttelu, joka oli samanlainen kuin leikkauksen jälkeisessä purkauksessa.
keskustelu
Libman-Sacks-endokardiitille on ominaista verrukoosileesiot venttiilin pinnoilla, joskin niitä voi esiintyä myös venttiilien vapailla reunoilla ja yleensä kaikilla eteisen tai kammion endokardiumin alueilla; verruca-histologia on yleensä epäspesifinen.4
doppler-kaikukardiografiaa voidaan pitää suositeltavana diagnoositekniikkana, sillä läppäsairauden esiintyvyys on 18-50%1,5,6% ja enintään 74%, jos käytetään transesofageaalista kaikukardiografiaa.7
tämä esiintyvyys on kuitenkin paljon suurempi kuin niiden lupuspotilaiden määrä, joilla on kliinisesti merkittäviä leesioita, noin 20% tapauksista.1
vaikka alkuperä läppävika leesiot SLE liittyy läheisesti läsnäolo fosfolipidivasta-aineita, 4 negatiivinen testitulokset, kuten meidän tapauksessamme, on kuvattu lääketieteellisessä kirjallisuudessa muilla potilailla SLE ja Libman-Sacks endokardiitti 8 tai jopa ei-bakteeri tromboottinen endokardiitti ilman perussairautta.9 Tämä selittynee sillä, että tällä hetkellä kaikki protromboottiset tilanteet, jotka voivat johtaa näiden vaurioiden esiintymiseen, jäävät määrittelemättömiksi.
potilaamme kaikukardiografiassa todettiin pieniä useita liikkuvia verrukoosia mitraaliläpän vapaissa reunuksissa sekä transthorasicissa että transesofageaalisen kaikukardiografian yhteydessä (kuva 1).
yleisin toiminnallinen häiriö on pulauttelu, kuten tässäkin tapauksessa. Kuitenkin, kun tauti on edennyt vain muutaman vuoden, potilas on nuori ja lupus on aktiivinen, läppävika on harvoin riittävän vakava aiheuttaa sydämen vajaatoiminta.1,2,10
meidän tapauksessamme 2 vuotta aiemmin tehty kaikukardiografinen tutkimus, joka osoitti Libman-Sacks vegetationsin ja lievän mitraalisen regurgitaation, mahdollistaa nopean etenemisen massiiviseksi mitraaliseksi regurgitaatioksi kongestiivisella sydämen vajaatoiminnalla, jonka vuoksi kirurginen toimenpide oli osoitettu. On tuskin viisikymmentä tapausta julkaistu lääketieteellisessä kirjallisuudessa mitraaliläpän korjaus johtuu SLE; prospektiivisessa tutkimuksessa osoitettiin, että 8% potilaista lopulta tarvitsevat sydänleikkauksen.1
lupukseen liittyvää valvulopatiaa sairastavien potilaiden hoitoon kuuluu endokardiitin estohoito, antiaggregantti-tai antikoagulanttihoito tietyissä tapauksissa ja läppäventtiilin vaihto, kun läppävika on vakava 11; kortikosteroidihoidon merkitys tähän valvulopatiaan ei ole selvillä.11 kiista koskee kirurgisen toimenpiteen tyyppiä. Jotkut kirjoittajat ehdottavat mekaanisten proteesien paremmuutta tämäntyyppisessä häiriössä verrattuna bioproteeseihin, mukaan lukien kryopreservoidut homograftit, koska jälkimmäinen voi johtaa lupus valvuliittiin uudessa venttiilissä.3,12-14 muut kirjoittajat15 ovat kuitenkin puoltaneet korjaavaa kirurgiaa mekaanisen proteesin haittojen välttämiseksi nuorilla potilailla, jotka tavallisesti tarvitsevat suuria annoksia kortikosteroideja ja antikoagulanttihoitoa ja joilla on suuri munuaisten vajaatoiminta.
meidän tapauksessamme 2 Viime episodia massiivisesta keuhkoverenvuodosta, johon liittyy vaikea hemoptyysi, ja tarve saada suuria annoksia kortikosteroideja taudin hillitsemiseksi ohjasivat läppäleikkauksen valintaa. Vaikka potilaan kehitystä on seurattava tulevina vuosina sarjallisten kaikukardiografisten tutkimusten kautta, 1 vuosi leikkauksen jälkeen läppävian korjaus on optimaalinen.