Le tecnologie avanzate di imaging stanno dimostrando che le ectasie corneali come il cheratocono sono più diffuse di quanto si pensasse in precedenza—fino a 265 casi ogni 100.000 persone.1 Quelli con storia familiare, sfregamento degli occhi e atopia, così come la sindrome di Down tendono ad essere più comunemente colpiti, e sono in genere diagnosticati durante la pubertà.2 Idrope corneale acuta-una grave complicanza dell’ectasia corneale-si verifica in appena il 2% e fino al 13% dei pazienti.3-5
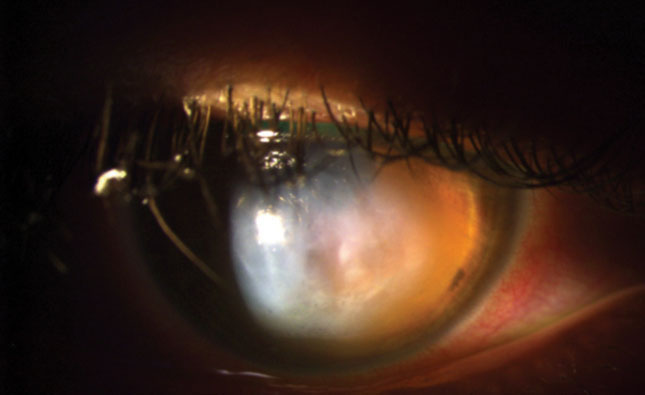
Fig. 1. L’occhio destro di questo paziente mostra l’iniezione congiuntivale globale del grado 3+, l’edema corneale del grado 3+, le micro bolle della traccia ed i difetti epiteliali.
Storia
Un maschio afroamericano di 40 anni presentava dolore improvviso all’occhio destro negli ultimi due giorni e visione sfocata associata. Ha valutato il dolore un “otto su 10” in gravità. Ha anche lamentato arrossamento e fotofobia, ma ha negato qualsiasi scarico, storia di chirurgia oculare, materiale estraneo che entra nell’occhio o trauma. Questa è stata la prima comparsa di questi sintomi. Il paziente ha tentato di usare lacrime artificiali senza sollievo. Il suo orientamento oculare era significativo, tuttavia, per il cheratocono, per il quale gli erano state prescritte lenti sclerali.
Esame
L’acuità visiva non corretta del paziente è stata di 20/800 a un piede nell’occhio destro, con un lieve miglioramento del foro stenopeico a 20/400 a due piedi. L’acuità visiva corretta nell’occhio sinistro con la lente sclerale era 20/20. Un esame esterno ha rivelato un’area di opacizzazione corneale nell’occhio destro, rendendo difficile il test della pupilla. La pupilla sinistra era rotonda, reattiva e non presentava segni di un difetto pupillare afferente. I campi visivi di confronto erano pieni di movimento a mano nell’occhio destro e pieni di conteggio delle dita nell’occhio sinistro. Il test muscolare extraoculare era normale. La biomicroscopia dell’occhio destro ha rivelato iniezione con-junctival globale di grado 3+, edema corneale di grado 3+, micro-bolle di traccia e difetti epiliali (Figura 1). La pressione intraoculare era normotensiva e l’esame del fondo dilatato era insignificante. Un segmento anteriore OCT è stato eseguito rivelando una rottura nella membrana di Descemet e nell’edema corneale (Figura 2).

Fig. 2. Questo segmento anteriore OCT mostra una rottura nella membrana di Descemet del paziente e nell’edema corneale.
Diagnosi
Le idrope corneali sono causate dalla scissione della membrana di Descemet, portando ad un afflusso di acqua nello stroma corneale con conseguente edema e foschia.6 A seconda del paziente e dell’estensione della lacrima, l’edema corneale e il dolore possono variare da relativamente asintomatici a gravi con disabilità visiva.4,6 Idrope corneale è più comune nei maschi di età compresa tra 20 e 40, ma non ha predilezione per la razza.3-6
L’idrope corneale acuta è autolimitante, con o senza trattamento, e tende a risolversi nel corso di tre o quattro mesi quando la membrana di Descemet si ri-sigilla.3 A seconda delle dimensioni della rottura e del rischio del paziente di infezione corneale o neovascolarizzazione, il tempo per completare la guarigione può essere esteso.3,4,6 Perforazione corneale, anche se rara, si verifica nel 3% dei pazienti che sviluppano idrope.3 Per prevenire complicazioni secondarie, ridurre al minimo i sintomi del paziente e limitare le cicatrici corneali, l’inizio della gestione medica è in genere garantito.
Trattamenti
Una varietà di opzioni mediche e chirurgiche sono disponibili per il trattamento di idrope corneale. Iperosmotici topici, può ridurre l’edema corneale (anche se lentamente) e migliorare l’acuità. Per gestire ulteriormente l’edema corneale riducendo anche il rischio di potenziale neo-vascolarizzazione, ODs può prescrivere steroidi topici-di solito a partire da una dose due volte al giorno.
Poiché gli steroidi hanno il potenziale per ostacolare la guarigione corneale o causare perforazione corneale, iniziare il trattamento steroideo all’inizio, o anche una volta che la membrana di Descemet guarisce, è controverso. Un agente cicloplegico, in genere dosato due volte al giorno (più se il dolore persiste), può essere aggiunto per ridurre il dolore oculare da un’uveite secondaria. Altre opzioni per alleviare il dolore includono agenti antinfiammatori non steroidei orali o topici o una lente a contatto con la benda. Tuttavia, a seconda della gravità del cheratocono del paziente, la lente potrebbe non adattarsi in modo appropriato con fluting e decentrazione significativi del bordo. Finché sono presenti difetti epiteliali, deve essere prescritto un antibiotico profilattico per ridurre il potenziale di infezione.
La ricerca mostra che la doxiciclina orale (10mg a 50mg due volte al giorno) e la vitamina C (1.000 mg al giorno)—dosata tipicamente presto nel corso di idrope acuta—possono essere utili.La doxiciclina 7,8 può anche ridurre le metalloproteinasi della matrice, che promuove la guarigione corneale.8 La vitamina C ha un ruolo nella matrice extracellulare e nella composizione corneale e può diminuire l’opacizzazione e la neovascolarizzazione.7 Altre opzioni per migliorare la guarigione corneale includono trapianti di membrana amniotica e abbondanti lacrime artificiali senza conservanti.
Gli interventi chirurgici includono l’iniezione di aria o gas, esafluoruro di zolfo (SF6) o perfluoropropano (C3F8), nella camera anteriore per chiudere meccanicamente l’apertura nella membrana di Descemet.9,10 Questi migliorano il tempo di guarigione ma non influenzano i risultati dell’acuità visiva, rendendoli controversi a causa di potenziali eventi avversi.9,10 Per ottenere il massimo effetto, queste procedure devono essere eseguite in genere entro pochi giorni dalla comparsa iniziale dei sintomi.9,10
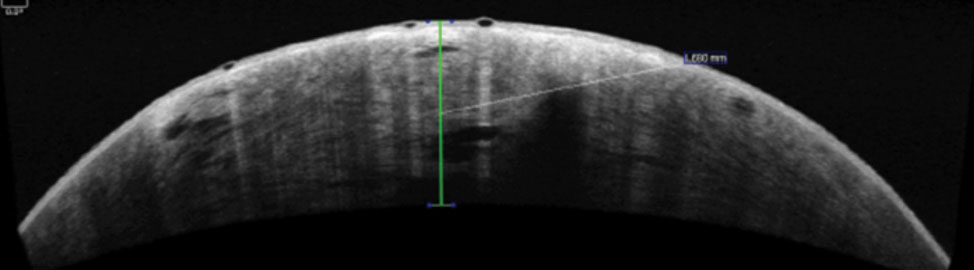
Figura 3. Questa immagine mostra lo spessore corneale del paziente tre settimane dopo il trattamento. Si era assottigliato di circa 400µm.
Recupero
Più a lungo l’idrope impiega a guarire, più è probabile che sia necessario un trapianto, a causa di cicatrici residue. Se questa cicatrice è grande, o direttamente sull’asse visivo, può essere eseguita una cheratoplastica lamellare anteriore profonda o una cheratoplastica penetrante, a seconda dell’estensione della cicatrice.3 Alcuni chirurghi sostengono un intervento precoce prima che si verifichi una neovascolarizzazione corneale, per ridurre il rischio di rigetto del trapianto. Prima di qualsiasi rinvio chirurgico, tentare un raccordo per lenti a contatto permeabili al gas consentirà di valutare la migliore acuità visiva e può ritardare l’intervento chirurgico, se il paziente può ottenere una visione funzionale.
Nel caso del nostro paziente, abbiamo prescritto un unguento iperosmotico, cicloplegico e antibiotico, insieme a doxiciclina orale e vitamina C. Entro tre settimane, il suo spessore corneale era più sottile di circa 400µm (Figura 3). Sebbene la pachimetria standard possa essere utile per monitorare la risoluzione, la pachimetria “globale” o AS-OCT sono più vantaggiose in quanto è possibile immaginare un’area più ampia della cornea e visualizzare la guarigione della membrana di Descemet. I pazienti con idrope corneale acuta devono essere monitorati ogni due o tre giorni dopo l’inizio iniziale, seguiti da una o due settimane una volta iniziata la guarigione. Tuttavia, se la cornea appare significativamente assottigliata, un follow-up più frequente è prudente per prevenire la perforazione. Si raccomanda l’uso di uno scudo di volpe. Una volta guariti, questi pazienti devono sottoporsi a un follow-up ogni tre mesi per ripetere l’imaging.
I professionisti devono sforzarsi di minimizzare i sintomi del paziente ed evitare devastanti complicazioni a lungo termine con un’adeguata gestione medica. Le apparecchiature di diagnostica per immagini possono essere utili non solo con la diagnosi iniziale, ma anche nella risoluzione del monitoraggio. Mentre gli idrope corneali sono rari, i progressi nella rilevazione e nei trattamenti del kera-tocono, con reticolazione corneale possono ridurlo o eliminarlo in futuro.
Il Dott. Morrow è un assistente professore clinico presso l’Università Statale di New York College of Optometry.
1. Godefrooij D, de Wit G, Uiterwaal C, et al. Incidenza e prevalenza specifiche per età del cheratocono: uno studio di registrazione a livello nazionale. Am J Ophthalmol. 2017;175(3):169-72.
2. Gokhale N. Epidemiologia del cheratocono. Indiano J Oph-thalmol. 2013;61(8):382-3.
3. Barsam A, Petrushlin H, Brennan M, et al. Idrope corneale acuta nel cheratocono: uno studio prospettico nazionale di inci-denza e gestione. Occhio (Lond). 2015;29(4):469-74.
4. Gokul A, Krishnan T, Emanuel P, et al. Persistendo idrope corneale acuta estrema con una fessura intrastromale gigante secondaria al cheratocono. Clin Exp Optom. 2015;98(5):483-6.
5. Thimons J. Gestione delle idrope corneali acute nel cheratocono. Rev Cornea & Cont Lens. 2015;152(3):32-3.
6. Fuentes E, Sandali O, El Sanharawi M, et al. Fattori predittivi anatomici di idrope corneale acuta nel cheratocono: uno studio di tomografia a coerenza ottica. Oftalmolo. 2015;122(8):1653-9.
7. Cho Y, Yoo W, Kim S, et al. Efficacia della supplementazione sistemica di vitamina c nel ridurre l’opacità corneale derivante dalla cheratite infettiva. Medicina (Balt). 2014;93(23):1-8.
8. Perry H, Hodes L, Seedor J, et al. Effetto della doxiciclina hyclate sulla guarigione delle ferite epiteliali corneali nel modello di ustione alcalina del coniglio. Cornea. 1993;12(5):379-82.
9. Maharana P, Sharma N, Vajpayee R. Idrope corneale acuta nel cheratocono. Indiano J Ophthalmol. 2013;61(8):461-4.
10. Shaw J. Idrope acuta: ripensare il trattamento. Rivista EyeNet. www.aao.org/eyenet/article/acute-hydrops-rethinking-treatment.Giugno 2012. Accesso al 15 ottobre 2018.