10 mei 2018, door NCI personeel
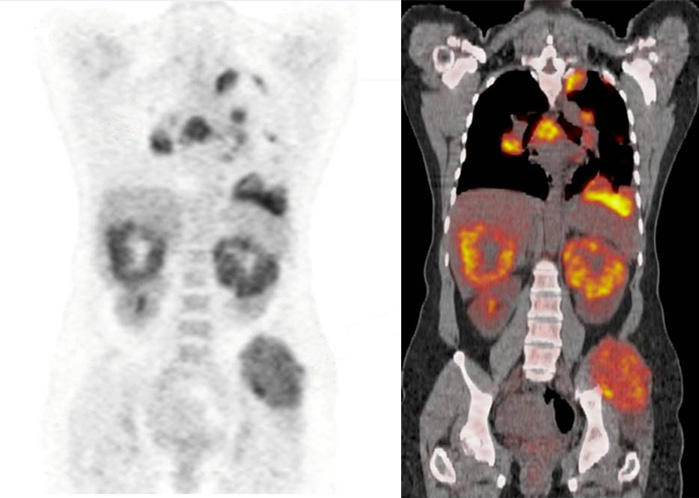
FDG PET/CT scans van een patiënt met gemetastaseerd niercelcarcinoom.
op 16 April keurde de Food and Drug Administration (FDA) de immunotherapiedrugs nivolumab (Opdivo) en ipilimumab (Yervoy) in combinatie goed als een initiële, of eerstelijnsbehandeling voor patiënten met gevorderde nierkanker bij wie de ziekte een tussenliggende of slechte prognose heeft.
dit is het eerste immunotherapieregime dat door de FDA is goedgekeurd voor de initiële behandeling van patiënten met nierkanker. Nivolumab was eerder goedgekeurd voor de behandeling van patiënten met gevorderde nierkanker bij wie de ziekte verergerd was na behandeling met standaard eerstelijnstherapie.
de nieuwe goedkeuring was gebaseerd op resultaten van een internationale fase 3 klinische studie. In het onderzoek leefden mensen met gevorderde nierkanker met een gemiddeld of laag risico die de immunotherapiecombinatie kregen over het geheel genomen langer en hadden ze meer kans om hun tumoren te laten krimpen in vergelijking met mensen die behandeld werden met sunitinib (Sutent). De resultaten van het onderzoek, dat werd gefinancierd door Bristol-Myers Squibb en Ono Pharmaceutical, werden op 5 April gemeld in het New England Journal of Medicine (NEJM).
betere resultaten met immunotherapie
het onderzoek, CheckMate 214 genoemd, betrof bijna 1.100 patiënten met niet eerder behandeld gevorderd niercelcarcinoom (RCC), het meest voorkomende type nierkanker. (Voor deze studie werd geavanceerde RCC gedefinieerd als kanker die niet vatbaar was voor potentieel curatieve chirurgie of radiotherapie of die was uitgezaaid naar andere gebieden van het lichaam.)
deelnemers werden willekeurig toegewezen aan de behandeling met nivolumab plus ipilimumab, beide immuuncheckpoint-remmers, gevolgd door nivolumab alleen als onderhoudstherapie, of sunitinib, een angiogeneseremmer die een standaardbehandeling is voor patiënten met gevorderde nierkanker.
de meerderheid van de patiënten in elke behandelingsgroep had een ziekte met een gemiddeld of een laag risico. Oncologen gebruiken gevestigde risicofactoren om patiënten met gevorderde nierkanker te categoriseren in gunstige-, intermediaire-, en slechte-risicogroepen. Ongeveer 75% van alle patiënten met gevorderde nierkanker heeft een ziekte met een gemiddeld of laag risico.18 maanden na aanvang van de behandeling was 75% van de patiënten die met de immunotherapiecombinatie werden behandeld nog in leven, vergeleken met 60% van degenen die met sunitinib werden behandeld. Bij een mediane follow-up van 25 maanden was de mediane totale overleving voor patiënten behandeld met de immunotherapiecombinatie niet bereikt. Voor patiënten die met sunitinib werden behandeld, was dit 26 maanden.
meer patiënten die de immunotherapiecombinatie kregen toegewezen dan sunitinib hadden een objectieve tumorrespons (42% versus 27%), inclusief complete responsen (9% versus 1%), Wat betekent dat hun kanker niet langer detecteerbaar was.
minder patiënten in het onderzoek die met nivolumab en ipilimumab werden behandeld dan met sunitinib hadden ernstige bijwerkingen (46% versus 63%). Echter, meer patiënten in de immunotherapiegroep stopten met de behandeling vanwege bijwerkingen (22% versus 12%). Er waren acht sterfgevallen die waarschijnlijk verband hielden met de behandeling onder patiënten die werden behandeld met nivolumab en ipilimumab, meldden de onderzoeksonderzoekers, en vier onder patiënten die werden behandeld met sunitinib.
ondanks de prevalentie van bijwerkingen en een groter percentage patiënten dat stopte met de behandeling, meldden patiënten die de immunotherapiecombinatie kregen een hogere kwaliteit van leven gedurende het hele onderzoek.
patiënten met een ziekte met een gunstig risico deden het beter met Sunitinib
de verbeteringen in overleving en tumorrespons die werden waargenomen bij patiënten met een ziekte met een gemiddeld en een laag risico die werden behandeld met de immunotherapiecombinatie, werden niet waargenomen bij patiënten met een ziekte met een gunstig risico.
bij patiënten met een gunstig risico op RCC hadden degenen die met sunitinib werden behandeld een hogere tumorrespons dan degenen die werden behandeld met nivolumab plus ipilimumab (52% versus 29%) en een langere progressievrije overleving (25,1 maanden versus 15,3 maanden), aldus Brendan D. Curti, M. D., van het Providence Cancer Institute, Portland, of, in een begeleidende editorial in NEJM.
de auteurs van het onderzoek erkenden de verschillende resultaten voor patiënten met een ziekte met een gunstig risico, maar zeiden dat de resultaten met voorzichtigheid moesten worden geïnterpreteerd vanwege de exploratieve aard van de analyse, de kleine subgroepsteekproef en de onvolwassenheid van overlevingsdata.”Echter, ze bleven, de ongelijksoortige resultaten “benadrukken de noodzaak om beter te begrijpen de onderliggende biologische processen rijden reacties op deze twee verschillende behandelingsregimes.”
Eric Jonasch, M. D., een urogenitale oncoloog aan de Universiteit van Texas MD Anderson Cancer Center, toegevoegd dat de bevindingen in gunstig-risico patiënten suggereren dat hun tumoren kunnen een andere biologie die kan worden gedefinieerd door een gebrek aan immuuncellen in de tumor micro-omgeving.
” ik denk dat we verdere studies moeten uitvoeren om echt vanuit een perspectief te begrijpen wat de verschillen zijn tussen patiënten met een gunstig, middelgroot en arm risico,” zei Dr.Jonasch, die niet betrokken was bij de studie.
naast het blokkeren van de Tumorbloedtoevoer
sinds 2005 heeft de FDA talrijke geneesmiddelen goedgekeurd zoals sunitinib die gericht zijn op angiogenese, de groei van nieuwe bloedvaten die tumoren voeden, om nierkanker te behandelen. In tegenstelling tot antiangiogenese geneesmiddelen, nivolumab en ipilimumab werken door het blokkeren van eiwitten die afschrikken of dempen een immuunrespons tegen tumoren.
de nieuwe goedkeuring zal waarschijnlijk veranderen hoe patiënten worden behandeld, zei Dr. Jonasch. Nu zullen patiënten met een ziekte met een gemiddeld of laag risico waarschijnlijk nivolumab en ipilimumab krijgen als hun initiële behandeling, stelde hij voor.”Ik denk dat de belangrijkste vraag nu is wat is de juiste strategie in termen van het combineren van checkpoint remmers met andere checkpoint remmers of met gerichte geneesmiddelen zoals lenvatinib of cabozantinib, en wat zijn die strategieën geven ons in termen van volledige responsen en duurzame responsen,” Dr.Jonasch zei.
de onderliggende biologische mechanismen van waarom tumoren reageren en resistentie ontwikkelen tegen deze behandelingsstrategieën moeten worden bestudeerd, zodat clinici beter individuen kunnen identificeren die het meest waarschijnlijk baat hebben bij een bepaalde strategie, legde hij uit.Zowel Dr. Jonasch als Dr.Curti suggereren dat het complete responspercentage dat wordt gezien met de immunotherapiecombinatie de lat verlegt voor de behandeling van patiënten met gevorderde RCC.
” de 9% complete response rate zal waarschijnlijk de nieuwe standaard zijn die we zullen proberen te overtreffen terwijl we proberen deze resultaten te verbeteren,” zei Dr.Jonasch.