- Hypophosphorous ácido Química,Propriedades,Usos, Produção
- Destaque
- propriedades químicas
- utiliza
- toxicidade
- identificação dos perigos
- método de Preparação
- método de produção
- Descrição
- Description
- Propriedades Químicas
- propriedades Físicas
- utiliza
- definição
- preparação
- Métodos de produção
- definição
- reacções
- Descrição Geral
- Ar & Reacções À Água
- perfil de reactividade
- perigo
- perigo para a saúde
- perigo de Incêndio
- Métodos de purificação
Hypophosphorous ácido Química,Propriedades,Usos, Produção
Destaque
Hypophosphorous ácido também é conhecido como “hypophosphite” é incolor de petróleo ou de liquefação de cristal , é um importante produto químico fino do produto. O principal uso é como agente redutor para revestimento eletrolítico, prevenção fosfórica descoloração de resinas, ele também pode ser usado no catalisador de reação de esterificação, o refrigerante, em particular para a produção de produto de alta pureza hipofosfito de sódio. Existem vários métodos de preparação, o método industrial comum para a produção é o método da resina de troca iônica e o método de eletrodiálise.
the chemical properties of hypophosphorous acid, uses, toxicity, and production methods are edited by andy of Chemicalbook. (2016-12-04)
propriedades químicas
é cristais deliquescentes ou óleo incolor. Ponto de fusão: 26.5℃. Densidade relativa( densidade específica): 1.439 (sólido, 19℃). É solúvel em água, etanol e éter, e pode ser misturado em qualquer proporção com água, etanol, acetona. No ar, ele facilmente deliquesce para o líquido syrupy, e a solução aquosa é ácida.
Hypophosphorous ácido é monobásico de ácido, em solução aquosa, Hypophosphorous ácido é forte o ácido, Ka = 10-2 (25℃); é relativamente estável à temperatura ambiente; disproportionation reação pode continuar a 130℃, decompor-se em fosfina e fósforo ácido:
2H3PO2=H3PO4+PH3
Ele tem uma forte redução, metal pesado solução de sal podem ser restaurados para metais, tais como Cu2 +, Hg2 +, Ag +, tais como:
4Ag+H3PO2+2H2) = 4Ag+H3PO4+4H +
é um oxidante fraco, pode ser reduzido à fosfina, fosfina quando encontra um forte agente redutor.
utiliza
1. O ácido hipofosfórico é utilizado como agente redutor para revestimento electrolítico;
2. Pode ser utilizado para prevenir a descoloração da resina de ácido fosfórico;
3. É usado como catalisador de esterificação, o refrigerante;
4. É usado para produzir hipofosfito, sais de sódio, sais de manganês, sais de ferro são geralmente usados como substâncias nutritivas;
5. O ácido hipofosfórico é usado em medicina e como agente redutor, a determinação de arsênico, telúrio e separação de tântalo, nióbio e outros reagentes.
6. É um forte agente redutor, pode ser usado para a preparação de hipofosfito de sódio, fosfato de cálcio e outros hipofosfitos.
7. Pode ser usado para o banho de revestimento. Medicamento. agente redutor. reagentes gerais.
8. É um forte agente redutor, pode ser usado na produção de hipofosfito de sódio, fosfato de cálcio e outros hipofosfitos.
9. Este produto é amplamente utilizado como agente redutor, Ag, Cu, Ni, Hg e outros metais são reduzidos correspondentes do metal, para a verificação de Como, Nb, Ta e outros reagentes, ele pode ser usado para a preparação de Na, K, Ca, Mn, Fe e outros tipos de hypophosphite.
toxicidade
é incombustível. Mas quando contactar com o agente hole H, vai causar fogo. Quando se encontra com um agente oxidante, a reação violenta e combustão pode prosseguir. Quando é aquecido a alta, pode decompor-se em gás fosfina altamente tóxico, ou mesmo explodir. É corrosivo. O ácido hipofosfórico é frequentemente adicionado em refrigerantes, e porque não é absorvido. Então o risco é pequeno, mas particularmente forte hipofosfito dói gastrintestinal. Acidentalmente salpica nos olhos ou contacto com a pele, muita água é usada para lavar. Os operadores de produção devem usar vestuário de protecção e outro vestuário de protecção. O equipamento de produção deve ser selado, a oficina deve ser bem ventilada.
identificação dos perigos
Advertência de perigo:
Provoca queimaduras graves da pele e lesões oculares.
Provoca lesões oculares graves
recomendações de prudência:
não respirar poeiras/fumos/gases/névoa/vapores / pulverização.Lave cuidadosamente após o manuseamento.
usar luvas de protecção e protecção ocular / facial.Em caso de ingestão, lavar a boca . Não induzir vómitos.Se estiver na pele (ou no cabelo): retirar/retirar imediatamente todas as roupas contaminadas. Lavar a pele com água/chuveiro.Se nos olhos: lavar cuidadosamente com água durante vários minutos. Remover as lentes de contacto, se
estiverem presentes e forem fáceis de fazer. Continua a enxaguar.Em caso de INALAÇÃO: retirar a vítima do ar fresco e manter em repouso numa posição confortável para respirar.Contacte imediatamente um centro de envenenamento ou um médico/médico.Conservar trancado.
elimine este material e o seu recipiente para um ponto de recolha de resíduos perigosos ou especiais.
método de Preparação
1. O fósforo e o hidróxido de bário solução é aquecida, sal de bário, Ba (H2PO2) 2 • 2H2O pode gerar, o ácido sulfúrico é adicionado na hypophosphorous ácido de bário em solução, Ba2+ pode precipitar:
Ba(H2PO2)2+H2SO4=BaSO4+2H3PO2
Hypophosphorous ácido pode ser obtido por evaporação sob pressão reduzida e baixa temperatura de cristalização. Devido a este processo, a solubilidade do sal de bário é pequena, de modo que a concentração de ácido Hipofosfórico obtido não é elevada, produto industrial deve ser purificado por recristalização.
2. o óxido de bário (ou cal) e a solução de fósforo branco são aquecidos em conjunto para formar fosfato de bário secundário (ou cálcio) e, em seguida, reage com ácido sulfúrico, é filtrado, concentrado para obter o produto, ou a solução de hipofosfito de sódio processa resina de permuta iónica do tipo H pode derivar o produto. Este método requer uma grande quantidade de resina, e regeneração de resina e passo de lavagem é pesado, geralmente custa mais de US $ 7 por libra, é apenas adequado para a produção de pequenos lotes, e não adequado para aplicações industriais em grande escala.
3. Hypophosphorous ácido é preparado por electrodiálise método, no qual a electrodiálise célula se divide em três partes, que são o ânodo da câmara, a matéria-prima da câmara e do cátodo câmara, o intermediário é separado por uma membrana aniônica e catiônica de membrana, entre duas membranas de sódio hypophosphite solução é colocado (concentração de 100g/L~500g/L), ânodo de uma câmara de solução diluída de Hypophosphorous ácido 5g/L, o ânodo da câmara é diluir a solução de hidróxido de sódio ( 5g /L), entre os pólos DC (3V~36V) é passado, ânodo libera o oxigênio, e gera um produto secundário da Hypophosphorous ácido; o cátodo emite hidrogênio, e gera produto secundário de hidróxido de sódio, o tempo de reação é de 3~21h. As reações de ânodo câmara e do cátodo câmara, são como segue:
ânodo câmara:
H2O==H++OH-
2OH-==O2+2H2O+4e
H++H2PO2-==H3PO2
cátodo câmara:
H2O==H++OH-
2H++2e==H2
Nd++OH-==NaOH
Electrodiálise método de preparação Hypophosphorous ácido é simples e o investimento em equipamentos é pequeno, ele é adequado para produção em massa.
4. A partir do hipofosfito de sódio de qualidade industrial, Cl-, SO42-aniões que afetam os indicadores de qualidade do ácido Hipofosfórico são removidos por precipitação, íons de metal pesado são removidos da solução formando sulfeto, e, em seguida, usando Forte Resina de troca de catião ácido para obter fosfato secundário de sódio, produto de alta pureza pode obter. O processo pode produzir fosfato secundário de alta qualidade, tecnicamente é viável, o processo é simples, operação fácil, boa qualidade do produto, pode atender às necessidades da indústria eletrônica, indústria de defesa e outros campos de alta tecnologia.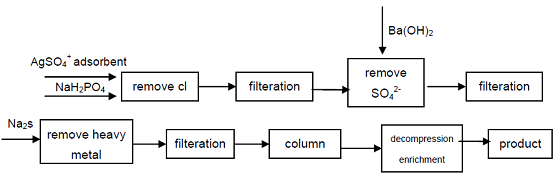
Figura 1 Processo de produção de ácido Hipofosfórico a partir de hipofosfito de Sódio Industrial.
5. De troca iônica em resina método: cerca de 70g de resina de troca catiônica humedecido com água é embalado em um tubo de vidro com 5 mol/L de ácido clorídrico de circulação cerca de 15min, depois de bem lavadas com água de alta pureza, sódio aquoso hypophosphite solução aquosa (15 g/60 ml de H2O) flui através dele, a resina coluna é o primeiro lavados com 50 ml, em seguida, com 25 rnl água destilada. O ácido e a lavagem dos efluentes são combinados, concentrando-se por evaporação em banho-maria. O ácido concentrado é colocado em alto vácuo com secador de P205 para desidratação, resfriamento e cristalização, filtração, recristalização, para obter Produto de ácido hipofosfórico.
método de produção
método de permuta iónica: colocar cerca de 70 g de resinas de permuta catiónica solúvel em água para encher um tubo de vidro. Circular com ácido clorídrico 5 mol/L durante cerca de 15 minutos e lavar suficientemente com água. Ter uma solução aquosa elevada de hipofosfito de sódio (15 g/60 ml de H2O) para fluir através da coluna de resina, seguida de lavagem com 50 ml de água e de lavagem com 25 rnl de água destilada. O ácido do efluente e as lavagens foram combinados e concentrados por evaporação num banho de água. O ácido concentrado é enviado para o altamente vácuo, secador P205 para desidratação, seguido de cristalização de arrefecimento, filtração e recristalização para obter o produto acabado do ácido hipofosfórico.
Descrição
o ácido Hipofosfórico é um potente agente redutor com uma fórmula molecular de H3PO2. Quimiistsrefere inorgânico para o ácido livre por este nome, embora o seu IUPACname seja dihidridohidroxidooxidofosforus, ou o nome aceitável do ácido fosfínico. É um composto de fusão incolor, que é solúvel em água,dioxano e álcoois. A fórmula para hipofosforousacid é geralmente escrita H3PO2, mas uma apresentação mais descritiva é HOP(o)H2, que eleva o seu caráter monoprotico. Sais derivados deste ácido chamados fosfinatos (hipofosfitos).
Description
This acid has the general formula ofH4P2O6 and differs from the other oxy-phosphorous acids. Tem muitos peculiarities.It é formado juntamente com fósforo e fosforicácidos, quando o fósforo é oxidado pelo ar húmido.Se o fósforo branco for exposto ao ar, e o acetato de sódio for adicionado ao liquido que se forma, o hipofosfato de na2h2p2o6·6h2oseparados. No entanto, o hipofosfato de sódio mono-hidratado é verisolúvel e deliquescente a uma dose de 98,7 g/100 ml.
Propriedades Químicas
incolor líquido
propriedades Físicas
Incolor deliquescente, cristais ou oleoso; odor azedo; densidade 1.493 g/cm3;derrete em 26.5°C; ferve a 130°C; muito solúvel em água, álcool e éter; densidade de 50% de solução aquosa é de 1,13 g/mL.
utiliza
preparação de hipofosfitos, electroplatinídeos.
definição
ChEBI: um oxoacídeo de fósforo que consiste num único fósforo pentavalente ligado covalentemente através de ligações únicas a dois hidrogénios e um grupo hidroxi e através de uma ligação dupla a um oxigénio. O progenitor da classe dos ácidos fosfínicos.
preparação
ácido Hipofosfórico pode ser preparado por vários métodos:
1. Fósforo branco em ebulição com hidróxido de cálcio:
P4 + 4Ca(OH)2 + 8H2O → 4CA(H2PO2)2 + 4H2
o sal de cálcio é solúvel em água. O tratamento com ácido sulfúrico produz o ácido organofosforoso:
(H2PO2)2Ca + H2SO4 → 2H3PO2 + CaSO4
a mistura do produto é filtrada para remover o CaSO4 insolúvel. A solução aquosa de ácido hipofosfórico está concentrada sob pressão reduzida.A água baryta concentrada pode ser utilizada em vez de hidróxido de cálcio.2. Ao tratar hipofosfito de sódio, Nah2po2 com uma resina permutadora de iões.O sal de sódio pode ser produzido por ebulição de fósforo branco com uma solução de hidróxido de sódio, uma reação similar a (1) acima.
PH3 + 2I2 + 2H2O → H3PO2 + 4HI
o método acima pode ser considerado mais seguro do que o que envolve o aquecimento de fósforo branco com álcali.O ácido Hipofosfórico deve ser conservado a uma temperatura inferior a 50 ° C. É vendido comercialmente como solução aquosa a várias concentrações.
Métodos de produção
o ácido Hipofosfórico é formado por reação de hipofosfito de bário e ácido sulfúrico, e filtragem de sulfato de bário. Por evaporação da solução no vácuo a 80 °C, e depois arrefecimento a 0°C, O ácido hipofosfórico cristaliza.
definição
um sólido cristalino de cor branca. É um Ácido monobásico que forma o anião H2PO2-em água. O sal de sódio, e portanto o ácido, pode ser preparado aquecendo fósforo amarelo com solução de hidróxido de sódio. O ácido livre e seus sais são agentes redutores poderosos.
reacções
ácido Hipofosfórico é miscível com água em todas as proporções e uma força comercial é de 30% H3PO2. Hipofosfitos são usados em medicina. Hypophosphorous ácido é um poderoso agente redutor, por exemplo, com o cobre sulfato de formas cuproso de hidreto de Cu2H2, marrom precipitado, que evolui de gás hidrogênio e folhas de cobre no aquecimento; com nitrato de prata produz finamente dividido prata; com sulfurosa ácido produz enxofre e alguns sulfeto de hidrogênio; com ácido sulfúrico produz sulfurosa ácido, que reage como acima; formas manganous imediatamente com permanganato.
Descrição Geral
cristais oleosos ou deliquescentes incolor com odor azedo. Densidade 1.439 g / cm3. Ponto de fusão 26.5°C. A inalação de vapores irrita ou queima o aparelho respiratório. Líquido e vapores podem irritar ou queimar os olhos e a pele.
Ar & Reacções À Água
Deliquescente. Solúvel em água.
perfil de reactividade
o ácido HIPOFOSFÓRICO decompõe-se quando aquecido em ácido fosfórico e fosfina espontaneamente inflamável. É oxidado pelo ácido sulfúrico com libertação de dióxido de enxofre e enxofre. Reage explosivamente com óxido de mercúrio(II). Reage violentamente com nitrato de mercúrio(II). Neutraliza bases em reacções exotérmicas.
perigo
risco de incêndio e explosão em contacto com agentes oxidantes.
perigo para a saúde
tóxico; por inalação, ingestão ou contacto com a pele com material pode causar lesões graves ou morte. O contacto com a substância fundida pode causar queimaduras graves na pele e nos olhos. Evite qualquer contacto com a pele. Os efeitos de contacto ou inalação podem ser retardados. O fogo pode produzir gases irritantes, corrosivos e / ou tóxicos. O escoamento da água de controlo de incêndios ou de diluição pode ser corrosivo e/ou tóxico e causar poluição.
perigo de Incêndio
não combustível, a substância em si não queima, mas pode decompor-se após aquecimento para produzir fumos corrosivos e/ou tóxicos. Alguns são oxidantes e podem inflamar combustíveis (madeira, papel, óleo, vestuário, etc.). O contacto com metais pode provocar a formação de um gás de hidrogénio inflamável. Os recipientes podem explodir quando aquecidos.
Métodos de purificação
o ácido fosforoso é um contaminante comum do ácido hipofosforoso comercial a 50%. Jenkins e Jones purificaram esta matéria evaporando cerca de 600 ml num frasco de 1L a 40o, sob pressão reduzida (em N2), para um volume de cerca de 300 ml. Depois de arrefecida, a solução foi transferida para um Erlenmeyer de boca larga, que foi rolado e deixado num banho de gelo seco/acetona durante várias horas para congelar (se necessário, com arranhões da parede). Quando o frasco foi então deixado em cerca de 5o durante 12 horas, cerca de 30-40% dele liquefeito, e foi novamente filtrado. Este processo foi repetido, então o sólido foi armazenado sobre Mg (ClO4) 2 em um dessecador de vácuo no frio. Cristalizações subsequentes a partir de n-butanol dissolvendo-o à temperatura ambiente e depois arrefecendo num banho de sal de gelo a-20o não parecem purificá-lo mais. O ácido livre forma cristais deliquescentes m 26,5 o e é solúvel em H2O e EtOH. O sal NaH2PO2 pode ser purificado através de uma resina de troca de aniões