aromaattisen renkaan saattaminen nukleofiilien hyökkäyksen kohteeksi
useimmissa näkemissämme aromaattisten yhdisteiden valmisteissa (kuten elektrofiilisessa aromaattisessa substituutiossa sekä edellisessä jaksossa käsitellyssä Suzuki-reaktiossa) aromaattinen rengas on nukleofiili ja reagoi elektrofiilisen reagenssin kanssa. Nukleofiilinen aromaattinen substituutio (17.1.) liittyy nukleofiilisiin reagensseihin, mutta se rajoittuu renkaisiin, joissa on voimakkaita elektroneja vetäytyviä ryhmiä Orto tai para lähtevään ryhmään. Monipuolisin tapa saada aromaattisia renkaita nukleofiiliseen hyökkäykseen on valmistaa Arenediatsoniumsuoloja, jotka sisältävät ArN2+ – ionin. Alla olevassa kaaviossa on esitetty erilaisia mahdollisia reaktioita arenediatsoniumsuolojen kanssa.

Arenediatsoniumsuoloja valmistetaan helposti aryyliamiineista (aniliineista) diatsotisaatioksi kutsutulla menetelmällä. Prosessissa amiini liuotetaan sopivaan happoon, jäähdytetään jääkylvyssä 0-5 oC: iin ja lisätään sitten natriumnitriittiliuosta (NaNO2). Happo reagoi NaNO2: n kanssa muodostaen typpihappoa (HNO2), joka sitten reagoi aryyliamiinin kanssa muodostaen arenediatsoniumsuolan. Yleisin näissä reaktioissa käytettävä suola on kloridi (valmistettu käyttämällä HCl: ää happona), jotka ovat melko liukoisia mutta hajoavat nopeasti huoneenlämmössä. Joissakin reaktioissa (kuten fenolin muodostumisessa) kloridi-ioni voi kuitenkin häiritä ja korvata CL: n, joten näissä tapauksissa käytetään sulfaattia (valmistettu käyttämällä H2SO4: ää). Diatsoniumsulfaatit ovat hieman stabiilimpia kuin kloridit, mutta ne ovat myös yleensä vähemmän liukenevia ja siten hankalampia käyttää. Diatsoniumtetrafluoriboraatit valmistetaan klorideista lisäämällä HBF4: ää; ne ovat yleensä täysin liukenemattomia, jolloin ne voidaan suodattaa pois, minkä jälkeen ne kuivataan hajoamista varten ilman vettä, jolloin renkaaseen tulee fluoria. Tätä menetelmää fluorin lisäämiseksi aromaattiseen renkaaseen kutsutaan Balz-Schiemann-reaktioksi.
Arenediatsoniumsuolat ovat hyödyllisiä välituotteita, ja ne menettävät helposti typpeä reagoidessaan erilaisten nukleofiilien kanssa, kuten yllä olevasta kaaviosta käy ilmi. Koska typpi on hyvin stabiili ja häviää kaasuna, tämä antaa voimakkaan käyttövoiman näille reaktioille. Veden tai jodidi-ionin tapauksessa nukleofiili reagoi ilman tarvetta katalyysille. Monia diatsoniumsuolojen reaktioita katalysoi kuitenkin kupari (I), jolloin reaktiota kutsutaan Sandmeyer-reaktioksi.
yhdessä reaktiossa, jossa nämä kaksi typpeä säilyvät, kytketään toinen (elektronirikas) aromaattinen rengas, kuten reaktiosysteemin vasemmasta osasta käy ilmi. Tämä on hyvin tärkeää keinotekoisessa väriaineteollisuudessa, joka perustettiin pääasiassa näiden ”atsovärien” valmistamisen avulla Perkinin mauven löytymisen jälkeen vuonna 1856.
käyttö synteesissä
diatsoniumsuolan kemia, joka perustuu nukleofiilisiin reagensseihin, joita käytetään elektrofiilisen aromaattisen renkaan kanssa, täydentää elektrofiilista aromaattista substituutiota (Eas, jossa käytetään elektrofiilisia reagensseja). Diatsoniumsuoloja valmistetaan helposti aromaattisista aineista kolmivaiheisen synteesin avulla:

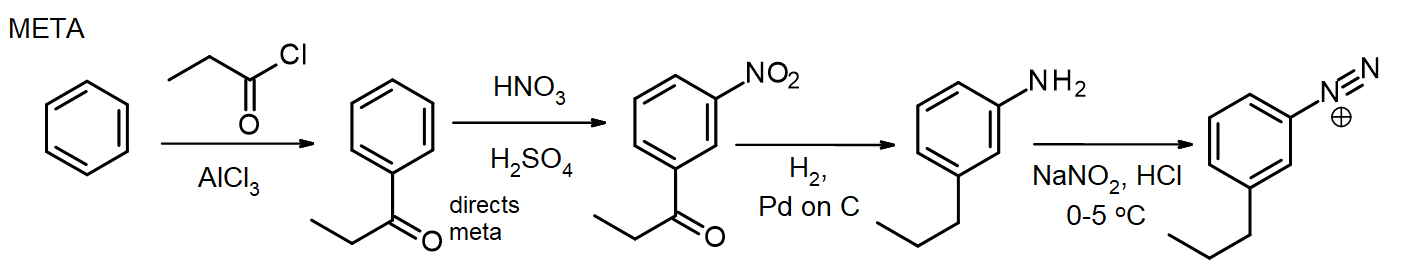
jos tarvitaan muita substituentteja, niitä voidaan lisätä synteesin aikana. Jos tarvitaan meta-substituentti, substituentti otetaan käyttöön nitrovaiheessa tai sitä ennen; Orto/para-substituenteille tämä voidaan tehdä NH2-vaiheessa. Aryyliamiinin aminoryhmä (aniliini) on erittäin voimakas aktivaattori, joten monet aryyliamiinien Eas – reaktiot tuovat nopeasti 2 tai 3 substituenttia, ellei NH2-ryhmän reaktiivisuutta hillitä muodostamalla amidi-recall tämä menetelmä amiinien suojelemiseksi asetylaatiolla, ryhmästä 16. Joissakin tapauksissa Uusi substituentti voi myös pelkistyä nitroryhmän pelkistyessä, kuten tässä metapropyylibentseenidiatsoniumkloridin synteesissä bentseenistä:
para-isomeerin synteesissä aryyliamiini asetyloidaan ennen Friedel-Crafts-reaktiota, minkä jälkeen se deasetyloidaan kuumentamalla ylimääräisellä aq: lla. HCl juuri ennen diatsotisointia.

tämä para-isomeerisynteesi osoittaa asetyyliryhmän käytön aminoryhmän reaktiivisuuden säätelyyn. (Vaihtoehtoisella synteesillä tämä voitaisiin välttää lisäämällä propyyliryhmä ensin, ennen nitrausta.) Vaikka nämä syntetisaattorit vaikuttavat pitkiltä, ne sisältävät synteettisiä askeleita, jotka ovat luotettavia ja toistettavissa, ja ne noudattavat vakiomallia. Myös se, että erilaisia substituentteja voidaan ottaa käyttöön valituissa asennoissa matkan varrella, tekee tästä lähestymistavasta erittäin arvokkaan synteettisen sekvenssin.