Explication
Le benzène agit avec des halogènes (anciens sels) comme le chlore et le brome et ces réactions sont appelées réaction de substitution électrophile en présence d’un catalyseur d’acide de Lewis comme le chlorure d’aluminium, le dichlorure de soufre, le chlorure de fer ou le fer. Le bromure d’aluminium est utilisé lors de la réaction du bromure de benzène.Le fer n’est pas un catalyseur car il réagit avec une petite quantité de chlore ou de bromine et forme du chlorure de fer (III) FeCl3 ou du bromideFeBr3 de fer (III).
2Fe + 3Cl2→ 2FeCl3
2Fe + 3Br2→2FeBr3
Réaction avec le chlore
Le Benzèneagit avec le chlore en présence de chlorure d’aluminium ou de fer pour préparer le chlorobenzène.
C6H6 + Cl2 → C6H5Cl + HCl
Réaction avec le brome
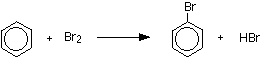
Le Benzèneagit avec le brome en présence de bromure d’aluminium ou de fer pour produire du bromobenzène. Le fer est utilisé car il est facilement disponible et moins cher.
C6H6 + Br2 → C6H5Br + HBr
Réaction d’addition
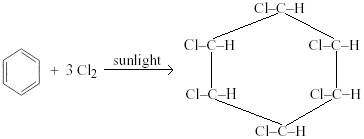
Additionla réaction du benzène chaud subit en présence de lumière ultraviolette avecchlorine ou brome. L’atome de chlore ou de brome s’ajoute à l’atome de carbone et la géolocalisation des anneaux est brisée en permanence.
Par exemple: le 1,2,3,4,5,6-hexachlorocyclohexane est produit lorsque le gaz de chlore à bulles à travers le benzène chaud est exposé à la lumière UV pendant une heure.
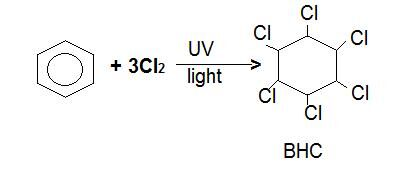
Le brome agirait de la même manière, le chlore et l’hydrogène fabriquent des nombres d’isomères en collant de haut en bas à une position aléatoire du cycle. La double liaison carbone-carbone est rompue et incapable de tourner. Un autre isomère est couramment utilisé comme insecticide appelé BCH, HCH et Gammexane. Aussi appelé hydrocarbures chlorés, il est très nocif pour l’environnement..
L’halogénation du méthylbenzène
Réaction de substitution
La réaction de substitution entre le méthylbenzène et le chlore ou le brome se déroule en deux jours:
- Substitution Dans le cycle
- Substitution dans le groupe méthyle
Substitution dans le cycle
Cette réaction est réalisée à température ambiante en présence de chlorure d’aluminium ou de fer et en absence de lumière UV. Les groupes méthyle sont fixés en position 2 ou 4 sur le cycle et le nouveau groupe est fixé sur le cycle à côté du groupe éthyle. La réaction de substitution avec le chlore produit deux produits2-chlorométhylbenzène et 4-chlorométhylbenzène.
C6H5CH3 + Cl2 → C6H4CH3Cl + HCl
Substitution en groupe méthyle
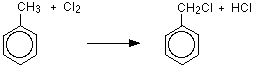
Substitutionréaction du chlore ou du brome dans le groupe méthyle plutôt que dans le cycle avec le méthylbenzène bouillant en présence de lumière UV et en l’absence de catalyseur.
Le produit formé est du (chlorométhyl) benzène, le nom écrit entre parenthèses montre quechlorine attachée au groupe méthyle et non au cycle.
Les atomes d’hydrogène sont remplacés dans le groupe méthyle par un atome de chlore, les trois atomes d’hydrogène du groupe méthyle sont remplacés par un atome de chlore. Les nouveaux produits sont le (dichlorométhyl)benzène et le (trichlorométhyl) benzène car l’atome d’hydrogène est remplacé un à la fois.
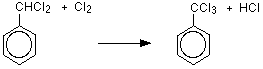
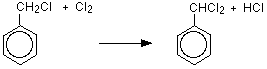
Formation de l’électrophile
La délocalisation de l’électron dans le cycle repousse la liaison chlore-chlore, de sorte que la molécule de chlore se rapproche du cycle benzénique.
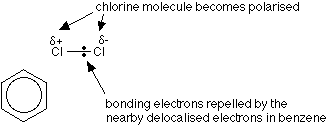
Le chlorure d’aluminium aide à la polarisation, l’extrémité positive de la molécule de chlore agit comme l’électrophile.
Mécanisme de substitution électrophile
Première étape
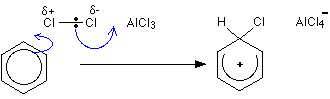
Deuxième étape
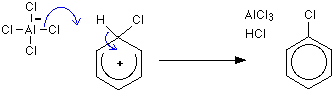
L’hydrogène du premier étage est éliminé par l’ion AlCl-4, maisau deuxième étage, le chlorure d’aluminium est régénéré.
Mécanisme de chloration du benzène
Première étape:
Formation d’ions chloronium, le chlore réagit avec l’acide de Lewis pour former un complexe qui rend le chlore plus électrophile.
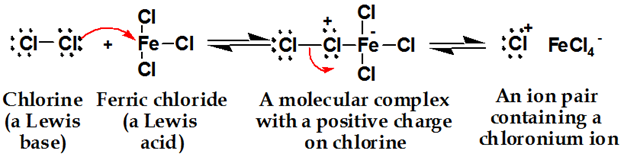
Deuxième étape :
Attaque d’ions chloronium sur l’anneau. Les électrons à double liaison du C = C aromatique agissent comme un nucléophile, attaquant le Cl électrophile, et une délocalisation a lieu.
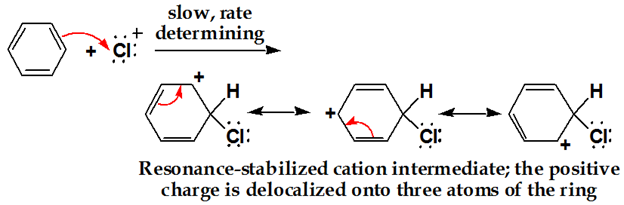
Troisième étape :
Le transfert de protons régénère le caractère aromatique du cycle.
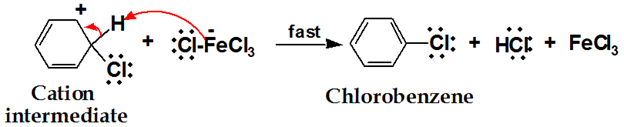
Le chlorobenzène utilise
- Ilest utilisé dans la production de pesticide DDT à l’aide de la réaction avecchloral en présence d’acide sulfurique.
- Il est utilisé comme intermédiaire dans la préparation de produits tels que les herbicides, les colorants et le caoutchouc.
- Ilest également utilisé comme solvant à ébullition élevée pour la préparation d’adhésifs, de peintures, de décapants, de vernis, de colorants et de médicaments.
- Ilest également utilisé pour la préparation d’isolant en polyuréthane.
Problèmes de santé
La personne exposée à un niveau élevé éprouve des maux de tête, un engourdissement, une somnolence, des nausées et des vomissements. Le chlorobenzène affecte également la dépression de la fonction de nombreuses parties du système nerveux. Chez les animaux, une exposition légère à sévère affecte le cerveau, le foie etle rein. Provoquent également des malformations congénitales.