10 de mayo de 2018, por Personal del NCI
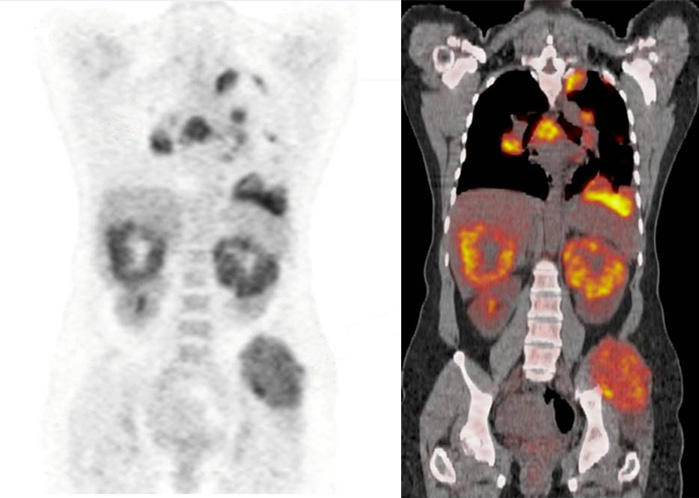
TEP/TC con FDG de un paciente con carcinoma metastásico de células renales.
El 16 de abril, la Administración de Alimentos y Medicamentos (FDA) aprobó los medicamentos de inmunoterapia nivolumab (Opdivo) e ipilimumab (Yervoy) en combinación como tratamiento inicial o de primera línea para pacientes con cáncer de riñón avanzado cuya enfermedad tiene un pronóstico intermedio o precario.
Este es el primer régimen de inmunoterapia aprobado por la FDA para el tratamiento inicial de pacientes con cáncer de riñón. Nivolumab fue aprobado previamente para tratar pacientes con cáncer de riñón avanzado cuya enfermedad había empeorado después del tratamiento con terapia de primera línea estándar.
La nueva aprobación se basó en los resultados de un ensayo clínico internacional de fase 3. En el ensayo, las personas con cáncer de riñón avanzado de riesgo intermedio o precario que recibieron la combinación de inmunoterapia vivieron más tiempo en general y tuvieron más probabilidades de que sus tumores se encogieran en comparación con aquellos tratados con sunitinib (Sutent). Los resultados del ensayo, que fue financiado por Bristol-Myers Squibb y Pharmaceutical Pharmaceutical, se informaron el 5 de abril en el New England Journal of Medicine (NEJM).
Mejores resultados con inmunoterapia
En el ensayo, llamado Jaque Mate 214, participaron casi 1100 pacientes con carcinoma avanzado de células renales (CCR) no tratado previamente, que es el tipo más común de cáncer de riñón. (Para este estudio, el CCR avanzado se definió como cáncer que no se prestaba a cirugía o radioterapia potencialmente curativas o que había hecho metástasis en otras áreas del cuerpo.)
Los participantes se asignaron al azar para recibir nivolumab más ipilimumab, ambos inhibidores de puntos de control inmunitario, seguidos de nivolumab solo como terapia de mantenimiento, o sunitinib, un inhibidor de la angiogénesis que es un tratamiento estándar para pacientes de cáncer de riñón avanzado.
La mayoría de los pacientes de cada grupo de tratamiento tenían enfermedad de riesgo intermedio o bajo. Los oncólogos utilizan factores de riesgo bien establecidos para clasificar a los pacientes con cáncer de riñón avanzado en grupos de riesgo favorable, intermedio y precario. Aproximadamente 75% de todos los pacientes de cáncer de riñón avanzado tienen enfermedad de riesgo intermedio o precario.
A los 18 meses de iniciar el tratamiento, el 75% de los pacientes tratados con la combinación de inmunoterapia seguían vivos, en comparación con el 60% de los tratados con sunitinib. A una mediana de seguimiento de 25 meses, no se había alcanzado la mediana de supervivencia global de los pacientes tratados con la combinación de inmunoterapia. Para los pacientes tratados con sunitinib, fue de 26 meses.
Más pacientes asignados a la combinación de inmunoterapia que a sunitinib experimentaron una respuesta tumoral objetiva (42% frente a 27%), incluidas respuestas completas (9% frente a 1%), lo que significa que su cáncer ya no era detectable.
Menos pacientes en el ensayo tratados con nivolumab e ipilimumab que con sunitinib experimentaron efectos adversos graves (46% frente a 63%). Sin embargo, más pacientes del grupo de inmunoterapia interrumpieron el tratamiento debido a los efectos secundarios (22% frente a 12%). Según informaron los investigadores del estudio, hubo ocho muertes probablemente relacionadas con el tratamiento entre los pacientes tratados con nivolumab e ipilimumab, y cuatro entre los pacientes tratados con sunitinib.
A pesar de la prevalencia de efectos secundarios y de un mayor porcentaje de pacientes que interrumpieron el tratamiento, los pacientes que recibieron la combinación de inmunoterapia notificaron una mayor calidad de vida a lo largo del estudio.
Los pacientes con Enfermedad de Riesgo Favorable obtuvieron mejores resultados con Sunitinib
Las mejoras en la supervivencia y las tasas de respuesta tumoral observadas en los pacientes con enfermedad de riesgo intermedio y de riesgo precario tratados con la combinación de inmunoterapia no se observaron en los pacientes con enfermedad de riesgo favorable.
De hecho, entre los pacientes con CCR de riesgo favorable, los tratados con sunitinib tuvieron una tasa de respuesta tumoral más alta que los tratados con nivolumab más ipilimumab (52% versus 29%) y una supervivencia sin progresión más larga (25,1 meses versus 15,3 meses), observó el Dr. Brendan D. Curti., del Providence Cancer Institute, Portland, OR, en un editorial adjunto en NEJM.
Los autores del estudio reconocieron los diferentes resultados para los pacientes con enfermedad de riesgo favorable, pero dijeron que los resultados deben «interpretarse con precaución debido a la naturaleza exploratoria del análisis, la muestra de subgrupos pequeños y la inmadurez de los datos de supervivencia.»Sin embargo, continuaron, los resultados dispares» destacan la necesidad de comprender mejor los procesos biológicos subyacentes que impulsan las respuestas a estos dos regímenes de tratamiento diferentes.»
Eric Jonasch, M. D., un oncólogo genitourinario del MD Anderson Cancer Center de la Universidad de Texas, agregó que los hallazgos en pacientes de riesgo favorable sugieren que sus tumores pueden tener una biología diferente que podría definirse por la falta de células inmunitarias en el microambiente tumoral.
«Creo que necesitamos realizar más estudios para entender realmente, desde una perspectiva, cuáles son las diferencias entre los pacientes favorables, intermedios y de bajo riesgo», dijo el Dr. Jonasch, quien no participó en el estudio.
Yendo más allá de Bloquear el Suministro de Sangre Tumoral
Desde 2005, la FDA ha aprobado numerosos medicamentos como sunitinib que se dirigen a la angiogénesis, el crecimiento de vasos sanguíneos nuevos que nutren tumores, para tratar el cáncer de riñón. A diferencia de los fármacos antiangiogénicos, el nivolumab y el ipilimumab actúan bloqueando proteínas que disuaden o amortiguan una respuesta inmunitaria contra los tumores.
La nueva aprobación probablemente cambiará la forma en que se trata a los pacientes, dijo el Dr. Jonasch. Ahora, los pacientes con enfermedad de riesgo intermedio o bajo probablemente recibirán nivolumab e ipilimumab como su tratamiento inicial, sugirió.
«Creo que la pregunta clave ahora es cuál es la estrategia correcta en términos de combinar inhibidores de puntos de control con otros inhibidores de puntos de control o con medicamentos dirigidos como lenvatinib o cabozantinib, y cuáles son esas estrategias que nos brindan respuestas completas y respuestas duraderas», dijo el Dr. Jonasch.
Los mecanismos biológicos subyacentes de por qué los tumores responden y desarrollan resistencia a estas estrategias de tratamiento deben estudiarse para que los médicos puedan identificar mejor a las personas que tienen más probabilidades de beneficiarse de una estrategia en particular, explicó.
Tanto el Dr. Jonasch como el Dr. Curti sugieren que la tasa de respuesta completa observada con la combinación de inmunoterapia mueve el listón para el tratamiento de pacientes con CCR avanzado.
» La tasa de respuesta completa del 9% probablemente será el nuevo estándar que nos esforzaremos por superar al tratar de mejorar estos resultados», dijo el Dr. Jonasch.