Maj 10, 2018, av NCI personal
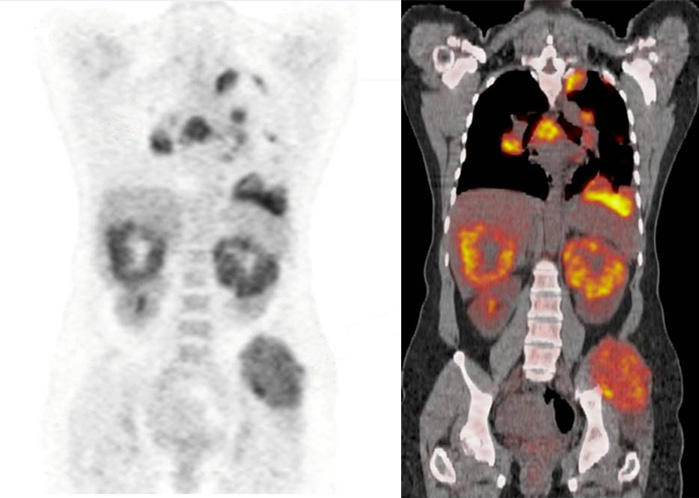
FDG PET / CT-skanningar från en patient med metastatisk njurcellscancer.
den 16 April godkände Food and Drug Administration (FDA) immunterapidrogen nivolumab (Opdivo) och ipilimumab (Yervoy) i kombination som en initial eller första linjens behandling för patienter med avancerad njurecancer vars sjukdom har en mellanliggande eller dålig prognos.
detta är den första immunterapiregimen som godkänts av FDA för initial behandling av patienter med njurcancer. Nivolumab godkändes tidigare för att behandla patienter med avancerad njurecancer vars sjukdom hade förvärrats efter behandling med standard första linjens behandling.
det nya godkännandet baserades på resultat från en internationell klinisk fas 3-studie. I försöket levde personer med mellanliggande eller dålig risk avancerad njurcancer som fick immunterapikombinationen längre totalt sett och var mer benägna att få sina tumörer att krympa jämfört med de som behandlades med sunitinib (Sutent). Resultat från försöket, som finansierades av Bristol-Myers Squibb och Ono Pharmaceutical, rapporterades den 5 April i New England Journal of Medicine (NEJM).
bättre resultat med immunterapi
studien, kallad CheckMate 214, involverade nästan 1 100 patienter med tidigare obehandlat avancerat njurcellscancer (RCC), vilket är den vanligaste typen av njurcancer. (För denna studie definierades avancerad RCC som cancer som inte var mottaglig för potentiellt botande kirurgi eller strålbehandling eller som hade metastaserat till andra delar av kroppen.)
deltagarna tilldelades slumpmässigt att få antingen nivolumab plus ipilimumab, vilka båda är immunkontrollinhibitorer, följt av nivolumab enbart som underhållsbehandling, eller sunitinib, en angiogeneshämmare som är en standardbehandling för patienter med avancerad njurcancer.
majoriteten av patienterna i varje behandlingsgrupp hade medel-eller lågrisksjukdom. Onkologer använder väletablerade riskfaktorer för att kategorisera patienter med avancerad njurcancer i gynnsamma, mellanliggande och fattiga riskgrupper. Cirka 75% av alla patienter med avancerad njurecancer har mellanliggande eller dålig risksjukdom.
18 månader efter påbörjad behandling levde 75% av patienterna som behandlades med immunterapikombinationen fortfarande, jämfört med 60% av de som behandlades med sunitinib. Vid en medianuppföljning på 25 månader hade medianöverlevnaden för patienter som behandlats med immunterapikombinationen inte uppnåtts. För patienter som behandlades med sunitinib var det 26 månader.
fler patienter som tilldelats immunterapikombinationen än sunitinib upplevde ett objektivt tumörrespons (42% mot 27%), inklusive fullständiga svar (9% mot 1%), vilket innebär att deras cancer inte längre kunde detekteras.
färre patienter i studien behandlade med nivolumab och ipilimumab än med sunitinib upplevde allvarliga biverkningar (46% mot 63%). Fler patienter i immunterapigruppen avbröt dock behandlingen på grund av biverkningar (22% mot 12%). Det fanns åtta dödsfall som sannolikt var relaterade till behandling bland patienter som behandlades med nivolumab och ipilimumab, rapporterade studieforskarna och fyra bland patienter som behandlades med sunitinib.
trots förekomsten av biverkningar och större andel patienter som stoppade behandlingen rapporterade patienter som fick immunterapikombinationen högre livskvalitet under hela studien.
patienter med gynnsam Risksjukdom gick bättre med Sunitinib
förbättringarna i överlevnad och tumörresponsfrekvens som ses hos patienter med mellanliggande och dålig risksjukdom behandlad med immunterapikombinationen sågs inte hos patienter med gynnsam risksjukdom.
faktum är att bland patienter med gynnsam risk RCC hade de som behandlades med sunitinib en högre tumörresponsfrekvens än de som behandlades med nivolumab plus ipilimumab (52% mot 29%) och längre progressionsfri överlevnad (25, 1 månader mot 15, 3 månader), noterade Brendan D. Curti, MD., av Providence Cancer Institute, Portland, eller, i en medföljande ledare i NEJM.
studieförfattarna erkände de olika resultaten för patienter med gynnsam risksjukdom, men sa att resultaten bör ”tolkas med försiktighet på grund av analysens undersökande karaktär, det lilla undergruppsprovet och omogenheten av överlevnadsdata.”Men de fortsatte, de olika resultaten” belyser behovet av att bättre förstå de underliggande biologiska processerna som driver svar på dessa två olika behandlingsregimer.”
Eric Jonasch, M. D., en genitourinary onkolog vid University of Texas MD Anderson Cancer Center, tillade att resultaten i gynnsamma riskpatienter tyder på att deras tumörer kan ha en annan biologi som kan definieras av brist på immunceller i tumörmikromiljön.
”jag tror att vi måste utföra ytterligare studier för att verkligen förstå ur ett perspektiv vad skillnaderna är mellan gynnsamma, mellanliggande och fattiga riskpatienter”, säger Dr.Jonasch, som inte var inblandad i studien.
flytta bortom att blockera Tumörblodtillförseln
sedan 2005 har FDA godkänt många läkemedel som sunitinib som riktar sig mot angiogenes, tillväxten av nya blodkärl som ger näring till tumörer, för att behandla njurcancer. Till skillnad från antiangiogenesläkemedel fungerar nivolumab och ipilimumab genom att blockera proteiner som avskräcker eller dämpar ett immunsvar mot tumörer.
det nya godkännandet kommer sannolikt att förändra hur patienter behandlas, säger Dr. Jonasch. Nu kommer patienter med mellanliggande eller dålig risksjukdom sannolikt att få nivolumab och ipilimumab som sin första behandling, föreslog han.
”jag tror att nyckelfrågan nu är vad som är rätt strategi när det gäller att kombinera kontrollpunktshämmare med andra kontrollpunktshämmare eller med riktade läkemedel som lenvatinib eller cabozantinib, och vad är de strategier som ger oss när det gäller fullständiga svar och varaktiga svar”, säger Dr.Jonasch.
de underliggande biologiska mekanismerna för varför tumörer svarar och utvecklar resistens mot dessa behandlingsstrategier måste studeras så att kliniker bättre kan identifiera individer som mest sannolikt kan dra nytta av en viss strategi, förklarade han.
både Dr. Jonasch och Dr.Curti föreslår att den fullständiga svarsfrekvensen som ses med immunterapikombinationen flyttar baren för behandling av patienter med avancerad RCC.
”9% komplett svarsfrekvens kommer förmodligen att vara den nya standarden som vi kommer att sträva efter att överträffa när vi försöker förbättra dessa resultat”, säger Dr.Jonasch.