Tento návod popisuje základní aspekty hmotnostní spektrometrie, které budou užitečné pro vás při rozhodování o tom, na správné techniky a měření pro své výzkumné soubory.
- co je hmotnostní spektrometrie?
- Hmotnostní Spektrometr
- Ionizační Metody
- Electron Impact Ionizace
- Chemické Ionizace
- Matricí Asistované Laserové Desorpce
- Atmosférického Tlaku Chemická Ionizace
- Ionizace Elektrosprejem
- Analýza Iontů
- Tandemové Hmotnostní Spektrometrie
- Separační Metody pro spojení s hmotnostním Spektrometrem
Co je Hmotnostní Spektrometrie?
Hmotnostní spektrometrie je analytická technika, která zahrnuje studium v plynné fázi ionizovaných molekul s cílem jeden nebo více z následujících:
- Molekulární hmotnosti
- Strukturní charakterizaci
- plynné fázi studie reaktivity
- Kvalitativní a kvantitativní analýzy složek ve směsi.
hmotnostní spektrometrie sestává v podstatě z vážení iontů v plynné fázi. Použitý nástroj lze považovat za sofistikovanou rovnováhu, která s vysokou přesností určuje hmotnosti jednotlivých atomů a molekul. V závislosti na chemických a fyzikálních vlastnostech vzorků lze použít různé ionizační techniky. Jedním z hlavních faktorů při výběru techniky ionizace, která má být použita, je termolabilita. U vzorků, které nejsoumolabilní a relativně těkavé, lze účinně použít ionizaci, jako je dopad elektronů a/nebo chemická ionizace. U vzorků, které jsou termolabilní, jako jsou peptidy, proteiny a další vzorky biologického zájmu, je třeba zvážit techniky měkké ionizace. Mezi nejpoužívanější techniky měkké ionizace patří Electrospray (ESI) a Matrix Assisted Laser desorpce (MALDI). Název dané konkrétní technice hmotnostní SPECIFIKACE obvykle ukazuje na použitou metodu ionizace.
atomové a molekulové hmotnosti jsou přiřazeny vzhledem k hmotnosti izotopu uhlíku, 12C, jehož atomová hmotnost je definována jako přesně 12. Skutečná hmotnost 12C je 12 daltonů, přičemž jeden dalton se rovná 1.661 10-24 g. hmotnost molekuly nebo iontu může být prezentována v daltonech (Da) nebo kilodaltonech (kDa).
hmotnostní spektrometr
hmotnostní spektrometrie používá přístroj zvaný hmotnostní spektrometr. Hlavní složky hmotnostního spektrometru jsou:
- Vstupní systém (LC, GC, přímá sonda atd…)
- zdroj iontů (EI, CI, ESI, APCI, MALDI atd…)
- Hmotnost analyzátoru (Kvadrupól, TOF, Iontová Past, Magnetický Sektor)
- Detektor (Elektronový Násobič, Micro Channel Desky Mcp)
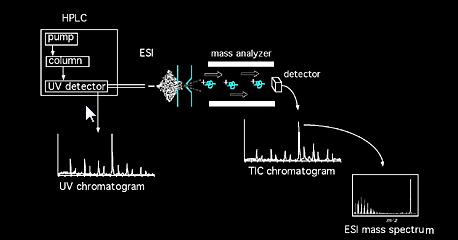
Vzorky mohou být zavedeny do hmotnostního spektrometru přímo přes pevné sondy, nebo v případě směsí, prostřednictvím chromatografie zařízení (např. Plynová chromatografie, kapalinová chromatografie, Kapilární elektroforéza, atd…). Jakmile jsou ve zdroji, molekuly vzorku jsou podrobeny ionizaci. Ionty vytvořené ve zdroji (molekulární a fragmentové ionty) získávají určitou kinetickou energii a opouštějí zdroj. Kalibrovaný analyzátor pak analyzuje procházející ionty jako funkci jejich poměrů hmotnosti a náboje. Mohou být použity různé druhy analyzátorů, magnetické, Kvadrulpole, iontové pasti, Fourierova transformace, doba letu atd…Poté je detekován iontový paprsek opouštějící sestavu analyzátoru a signál je registrován. Běžné ionizační metoda zkratky patří:
- EI=Dopad Elektronů;
- CI=Chemická Ionizace;
- SIMS=Sekundárních Iontů Hmotnostní Spektrometr;
- FAB=Fast Atom Bombardování;
- LDMS=Laserové Desorpční Hmotnostní Spektrometr;
- PDMS=Plazma Desorpční Hmotnostní Spektrometr;
- TS=Thermospray;
- =Aerospray;
- ESMS=Elektrosprejem Hmotnostní Spektrometr.
Společné hmotnostní analyzátor zkratky patří:
- EB=Elektrostatický-Magnetické;
- =iontová past;
- Q=Kvadrupól;
- TOF=Time of Flight.
Ionizační Metody
Výběr správné ionizační metoda pro analýzu vašeho vzorku je velmi důležité. I když můžeme nabídnout návrhy, je vaší odpovědností pochopit a vybrat metodu(y) vhodnou pro vaše výzkumné sloučeniny.
- Dopad Elektronů EI Ionizace
- Chemická Ionizace CI
- Negativní Ion Chemická Ionizace
- Ionizace Elektrosprejem Techniky
- Matrix Assisted Lazer Desorpce (není nabízena v našem zařízení, ale k dispozici elswhere na akademické půdě)
- Atmosférického Tlaku Chemická Ionizace APCI
Electron Impact Ionizace
M + e-(70eV) —–> M+. + 2e –
ei ionizační metoda je vhodná pro netermolabilní sloučeniny. Je vyžadována volatilita vzorku. Vzorky molekul ve stavu par jsou bombardovány rychle se pohybujícími elektrony, konvenčně 70 eV energie. To má za následek tvorbu iontů. Jeden elektron z nejvyšší orbitální energie se uvolní a v důsledku toho se vytvoří molekulární ionty. Některé z těchto molekulárních iontů se rozkládají a vytvářejí se fragmentové ionty. Fragmentace daného iontu je způsobena přebytkem energie, kterou vyžaduje v rámci ionizace. Fragmentové ionty mohou být lichý elektron nebo sudý elektron. Molekulární ionty vytvořené při ionizaci elektronů jsou liché elektronové ionty. Ionty lichých elektronových fragmentů jsou tvořeny přímým štěpením (např. přímé štěpení vazby C-C). I ionty elektronových fragmentů jsou často tvořeny přeskupením (např. Vzorek může být zaveden do EI zdroj pomocí plynové chromatografie zařízení, například v případě směsí, nebo přímo přes pevné sondy zařízení. Množství potřebná pro experiment je obvykle menší než mikrogram materiálu.
hmotnostní spektra EI ve většině případů obsahují intenzivní vrcholy fragmentových iontů a mnohem méně intenzivní vrchol molekulárních iontů. Když vrchol molekulárních iontů není pozorován v hmotnostním spektru, může být použita chemická ionizace za účelem získání informací o molekulárních iontech. Jedním z užitečných pravidel pro určení, zda je iont molekulárním iontem, je pravidlo dusíku.
dusíkové pravidlo: jak je uvedeno výše, molekulární ionty vytvořené při ionizaci EI jsou liché elektronové ionty. Pokud je jejich pozorovaný poměr hmotnosti k náboji lichý, zkoumaná molekula obsahuje lichý počet atomů dusíku. Pokud je tento poměr hmotnosti k náboji sudé číslo, tato molekula neobsahuje žádné nebo dokonce atomy dusíku.
Chemické Ionizace
Pro organické chemiky, Chemická Ionizace (CI) je zvláště užitečná technika při žádné molekulární ion je pozorován v EI hmotnostní spektrum, a to i v případě potvrzení hmotnost účtovat poměr molekulární ion. Chemická ionizační technika používá prakticky stejné zařízení iontového zdroje jako při dopadu elektronů, s výjimkou, CI používá těsný iontový zdroj, a reagenční plyn. Reakční plyn (např. amoniak) je nejprve vystaven působení elektronů. Vzorkové ionty jsou tvořeny interakcí iontů reakčního plynu a molekul vzorku. Tento jev se nazývá reakce iontových molekul. Molekuly reakčního plynu jsou přítomny v poměru asi 100: 1 Vzhledem k molekulám vzorku. V procesu CI se vytvářejí pozitivní ionty a negativní ionty. V závislosti na nastavení přístroje (zdrojové napětí, detektor atd…) zaznamenávají se pouze kladné ionty nebo pouze záporné ionty.
v CI dochází k reakcím molekul iontů mezi molekulami ionizovaného činidla (G) a neutrálními molekulami těkavého analytu (M) za vzniku iontů analytu. Často jsou pozorovány pseudomolekulární ionty MH+ (režim pozitivních iontů) nebo-(režim negativních iontů). Na rozdíl od molekulárních iontů získaných metodou EI dochází k detekci MH+ a – ve vysokém výtěžku a pozoruje se méně fragmentových iontů.
Kladný iont režimu:
GH+ + M ——> MH+ + G
Negativní ion režimu:
– + M ——> – + G
Tyto jednoduché reakce přenosu protonu jsou pravdivé plynu-fáze acidobazické procesy v Bronsted-Lowrey smysl. „Těsný“ iontový zdroj (tlak = 0,1-2 torr) se používá k maximalizaci kolizí, což má za následek zvýšení citlivosti. K uskutečnění těchto reakcí molekul iontů musí být exotermní. Přenos protonů je jedním z jednoduchých procesů pozorovaných v pozitivním CI:
RH+ + M – – – – > MH+ + R
jedním z rozhodujících parametrů v této reakci je afinita protonů. Aby došlo k reakci, musí být protonová afinita molekuly M vyšší než afinita molekuly plynu. Hlavní reakční plyny používané v CI jsou: amoniak, metan a isobutan. Vzniklé převažující reaktantové ionty jsou uvedeny v níže uvedených mechanismech. Volba reakčního plynu ovlivňuje rozsah fragmentace kvazimolekulárního iontu.
metan (pozitivní iontová chemická ionizace):
- CH4 + e —–> CH4+. + 2e ——> CH3+ + H.
- CH4+. + CH4 —–> CH5+ +CH3.
- CH4+. + CH4 —–> C2H5+ + H2 + H.
Isobutane (positive ion chemical ionization):
- i-C4H10 + e —–> i-C4H10+. + 2e
- i-C4H10+. + i-C4H10 ——> i-C4H9+ + C4H9 +H2
Ammonia (positive ion chemical ionization):
- NH3 + e —–> NH3+. + 2e
- NH3+. + NH3 ——> NH4+ + NH2.
- NH4+ + NH3 ———>N2H7+
V metanu pozitivní ion režim chemické ionizace relevantní vzorek vrcholy pozorované jsou MH+, +,+;, ale především MH+. To odpovídá hmotnostem M+1, M + 29 A M + 41.
v chemickém ionizačním režimu s pozitivním iontem isobutanu je hlavním pozorovaným vrcholem MH+.
v chemickém ionizačním režimu s pozitivním iontem amoniaku jsou hlavními pozorovanými vrcholy MH+ a +. Pokud je přítomno více než jedno protonační místo, mohou být vidět další NH3 addukty odpovídající +. To odpovídá hmotnostem M+1, M + 18 A M + 35.
V některých případech, protonované dimery nebo jiné adukty může být viděn; ztráta H2O následuje protonaci nebo adduct ion tvorbě je vidět, pro některé třídy sloučenin. Pokud se zdá, že spektrum, které pozorujete, nevykazuje správné ionty aduktu nebo vykazuje rozsáhlou fragmentaci, buďte opatrní při pokusu o interpretaci výsledků. V literatuře je k dispozici množství údajů o mechanismech chemické ionizace použitelných pro konkrétní třídy sloučenin.
dva faktory určují volbu použitého reakčního plynu:
- Proton affinity PA
- přenos Energie
NH3 (čpavek) je nejpoužívanější činidla plynu v CI, protože nízký přenos energie NH4+ porovnání s CH5+ například. U NH3 jako reakčního plynu jsou obvykle pozorovány MH+ a MNH4+ (rozdíl 17 hmotnostních jednotek).
Negativní Ion Chemická Ionizace
Tři mechanismy mohou být zdůrazněno,:
- Elektronový záchyt reakce, z důvodu dosažení pomalých, nízké energie „termalizovaného“ elektrony, které mohou být převedeny více efektivně, aby vzorek molekul.
- přenos Elektronů z ionizované činidla plynu (např. NH2 – může přenášet elektron na molekulu mají větší elektronovou afinitu než NH2).
- reakční plynné ionty se účastní skutečných CI reakcí (např. abstrakce protonů podle relativní acidity).
molekulární ionty pozorované v hmotnostních spektrech záporných iontů jsou obvykle M-nebo -.
electrospray ionizační metoda
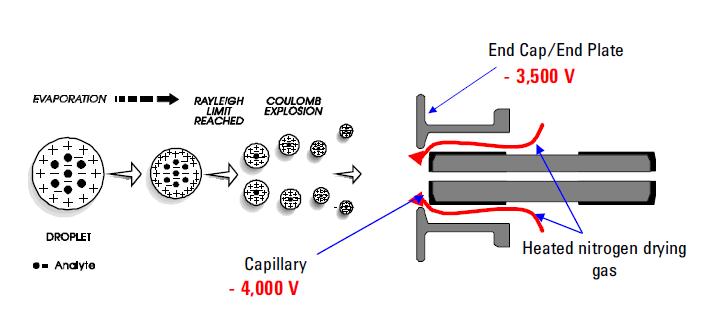
mezi nejpoužívanější techniky ionizace postřikem patří ionizace Elektrosprejem (ESI). Tato technika je i nadále metodou volby pro analýzu termolabilních chemikálií. Jeho schopnosti jsou dobře zdokumentovány. Používá elektrické napětí mezi výstupem sondy ESI (např. kapilárou) a protielektrodou, která je umístěna několik milimetrů od sondy. Výsledkem procesu je generování vysoce nabitých kapiček přímo z infuzního roztoku. Násobit a / nebo jednotlivě nabité molekuly analytu desorbují ze stříkaných kapiček a vzorkují se zbytkem hmotnostního spektrometru. ESI byl význačný pro jeho schopnost produkovat násobit nabité molekulární ionty z velkého množství polymerů, jako jsou bílkoviny a DNA fragmenty; umožňuje také citlivou detekci jednotlivě nabitá nízkomolekulární polární druhy, jako jsou drogy a drogové metabolity. Tvorba kladných nebo záporných iontů (v závislosti na znaku aplikovaného elektrického pole) nastává ve vysokém výtěžku. V režimu kladných iontů protonovaných a / nebo alkalických molekul aduktu analytu obecně pozorovaných v hmotnostních spektrech. V režimu záporných iontů jsou pozorovány provozní vrcholy odpovídající deprotonovaným molekulám analytu. ESI je popisován jako velmi „měkké“ ionizační technika, kde okolní vana plynu má zmírňující účinek na vnitřní a translační energie desorbované ionty.
Výhody ESI:
- Měkké ionizační proces, takže neporušené molekulární ionty jsou pozorovány
- ESI umožňuje výrobu vícenásobně nabité ionty. To má za následek schopnost analyzovat druhy s velmi vysokou molekulovou hmotností Pomocí nejvíce dostupných analyzátorů hmotnosti (např.
- ESI je proces atmosférického tlaku. Díky tomu je snadné použití a snadné rozhraní s technikami separace HPLC a CE.
Matricí Asistovaná Laserová Desorpce (MALDI)
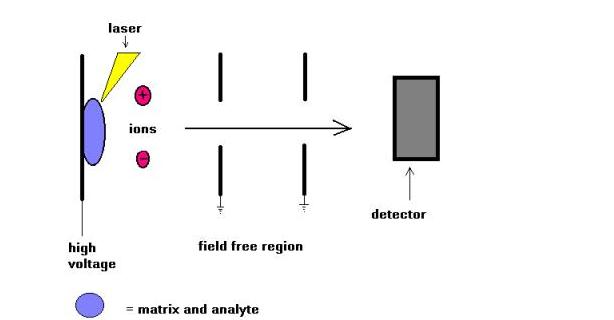
Matricí Asistovaná Laserová Desorpce (MALDI) – hmotnostní spektrometrie technikou byl představen Karas a Hillkamp v roce 1988 pro ionizaci peptidů a proteinů. Brzy poté, co tato technika byla schopna analyzovat jiný typ biomolekul, jako jsou oligosacharidy, glykolipidy, nukleotidy a syntetické polymery. V této technice jsou vzorky kokrystalizovány látkou absorbující UV záření zvanou matrice. Například pro proteiny je matricí volby často kyselina sinapinová. Nejčastěji se používá záření 337 nm z dusíkového laseru. Laser pomáhá zavádět energii do molekulárního systému tak, aby zabránil tepelnému rozkladu.
MALDI je často používán s time-of-lety hmotnostní spektrometr ( TOF ) v důsledku pulzující přírody, techniky a hmotnostní rozsah schopností. Molekulová hmotnost až několik stovek daltonů by mohla být měřena. V posledních několika letech bylo provedeno srovnání ionizačních technik MALDI a ESI. Podle mého názoru tyto dvě techniky nejsou konkurenceschopné, ale komplementární. Abychom jmenovali alespoň některé, u druhů s vysokou molekulovou hmotností vede MALDI k tvorbě jednotlivě nabitých molekulárních iontů, zatímco ESI umožňuje tvorbu násobně nabitých molekulárních iontů.
praktické úvahy:
- konečný molární poměr vzorek / matrice je asi nebo kolem 1/5000.
- Konečné koncentrace vzorku je 1 až 10 pmol/ul
- Naše zkušenosti s MALDI poukazují na dynamický rozsah 100 fmol/ul několika stovek pmol/ul
- MALDI je poměrně robustní ionizační technika, která toleruje používání soli a povrchově aktivních látek a pufrů. I když je nejlepší je odstranit pro lepší výkon.
Peptidové a Proteinové Standardy pro MALDI:
- Angiotenzin II (lidské) MW: 1046.2
- Substance P (lidské) MW: 1347.7
- Inzulínu (skotu) MW: 5733.6
- Cytochrom c (koní) MW: 12,360.1
- RNase A (skotu) MW: 13,682.2
- Apo-Myoglobin (koní) MW: 16,951.5
- Trypsinogen (skotu) MW: 23,980.9
Atmosférického Tlaku Chemická Ionizace
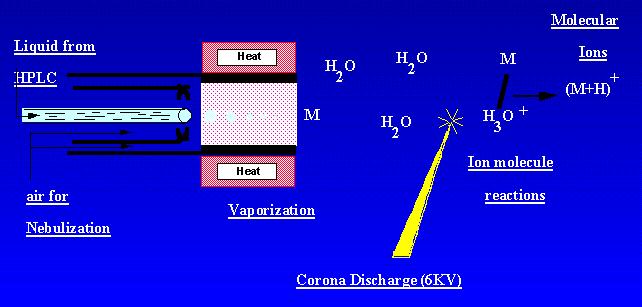
APCI je technika, která vytváří ionty za atmosférického tlaku. Roztok vzorku protéká vyhřívaná trubice, kde je volatilized v mlze a stříká do korónového výboje s pomocí dusíku rozprašování. Molekulární vzorky jsou ionizovány reakcemi iontových molekul z výbojových iontů ambiant corona. Ionty jsou produkovány ve výboji a extrahovány do hmotnostního spektrometru. APCI je nejvhodnější pro relativně polární, polotěkavé vzorky. Hmotnostní spektrum APCI obvykle obsahovalo kvazimolekulární iont, – nebo +.
analýza iontů
k dosažení hmotnostní separace je možné použít několik různých fyzikálních parametrů. Běžné typy analyzátorů hmotnosti jsou popsány níže. Každý z nich má své výhody a nevýhody. V našem zařízení máme v současné době kvadrupólové, iontové pasti, hmotnostní spektrometry amd Time-of-Flight (TOF).
Magnetické Sektoru Hmotnostní Spektrometr
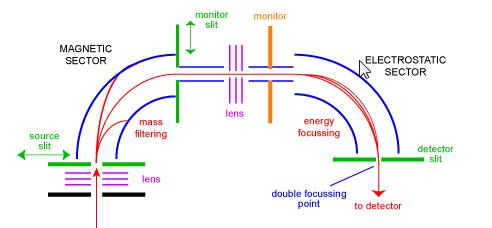
odvětví hmotnostní spektrometr byl jeden z nejčastějších typů hmotnostní analyzátor a pravděpodobně nejvíce známý pro každodenní vědec. V roce 1950 byly první komerční hmotnostní spektrometry sektorové nástroje. Skládají se z nějaké kombinace velkého elektromagnetického a nějakého druhu elektrostatického zaostřovacího zařízení. Různí výrobci používají různé geometrie. Obrázek 1 znázorňuje schéma standardního dvojitého zaostřovacího nástroje s geometrií „BE“. Konfigurace BE se také nazývá hmotnostní spektrometr sektoru reverzní geometrie – to je nástroj s duálním sektorem sestávající z magnetického sektoru následovaného elektrostatickým sektorem.
ionty vstupují do přístroje ze zdroje (vlevo dole), kde jsou zpočátku zaostřeny. Vstupují do magnetického sektoru přes zdrojovou štěrbinu, kde jsou vychýleny podle pravidla levé ruky. Ionty s vyšší hmotností jsou vychýleny méně než ionty s nižší hmotností. Skenování magnetu umožňuje zaostření iontů různých hmot na štěrbinu monitoru. V této fázi byly ionty odděleny pouze jejich hmotami. Chcete-li získat spektrum dobrého rozlišení, kde všechny ionty se stejným m/z jeví shodné jako jeden vrchol ve spektru, ionty musí být filtrovány jejich kinetickou energií. Po další fázi se zaměřením na ionty vstupují do elektrostatického sektoru, kde ionty o stejném m/z mají své energetické rozvody opraveny a jsou zaměřené na double zaměří bod na detektoru štěrbina.
sektorové nástroje měly v 1950 a 1960 obrovské obchodní úspěchy, protože byly jediným praktickým způsobem získávání dat s vysokým rozlišením. V posledních zhruba 20 letech klesají s klesajícími cenami FTMS a vývojem alternativ s vysokým rozlišením (například Q-Tof) sektorové nástroje.
Time-of-Flight Hmotnostní Spektrometrie (TOF-MS)
time-of-flight hmotnostní spektrometr používá rozdíly v tranzitní čas pomocí drift regionu oddělit ionty o různé hmotnosti. Pracuje v pulzním režimu, takže ionty musí být produkovány nebo extrahovány v impulsech. Elektrické pole urychluje všechny ionty do oblasti driftu bez pole s kinetickou energií qV, kde q je iontový náboj a V je aplikované napětí. Protože iontová kinetická energie je 0, 5mv2, lehčí ionty mají vyšší rychlost než těžší ionty a dosáhnou detektoru na konci driftové oblasti dříve.
Teorie:
- K. E. = qV
- 1/2 mv2 = qV
- v = (2qV/m)1/2
tranzitní čas (t) přes drift tube L/v kde L je délka driftové trubice
- t=L / (2V/m/q)1/2
Schéma lineárního TOF-MS

Toto schéma ukazuje, ablace iontů z objemového vzorku s pulzním laserem. Reflectron je řada prstenců nebo mřížek, které fungují jako iontové zrcadlo. Toto zrcadlo kompenzuje šíření kinetických energií iontů při vstupu do driftové oblasti a zlepšuje rozlišení nástroje. Výstup iontového detektoru je zobrazen na osciloskopu jako funkce času pro výrobu hmotnostního spektra.
Iontová Past
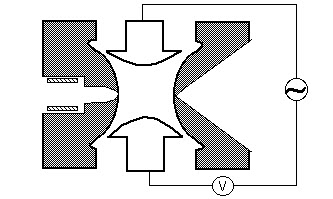
Ionty vytvořené elektronovým nárazem (EI), elektrosprejem (ESI), nebo matricí asistovaná laserová desorpce (MALDI) a ionizace jsou zaměřeny pomocí elektrostatického čočkování systému do iontové pasti. Elektrostatická iontová brána pulzuje otevřená (- V) a uzavřená (+V), aby vstřikovala ionty do iontové pasti. Pulzování iontové brány odlišuje iontové pasti od“ paprskových “ nástrojů, jako jsou kvadrupoly, kde ionty neustále vstupují do hmotnostního analyzátoru. Doba, po kterou jsou ionty povoleny do pasti, nazývá se „doba ionizace“, je nastavena tak, aby maximalizovala signál při minimalizaci efektů náboje prostoru. Space-charge výsledky z příliš mnoho iontů v pasti, které způsobují narušení elektrického pole, což vede k celkovému snížení výkonu. Iontový lapač je obvykle naplněn heliem na tlak asi 1 mtorr. Kolize s heliem tlumí kinetickou energii iontů a slouží k rychlému smlouvy trajektorie směrem ke středu iontové pasti umožňující odchyt vstřikované ionty. Pasti ionty jsou dále zaměřeny směrem ke středu pasti pomocí oscilační potenciál, nazývá základní rf , aplikovaná do ringu elektrody. Ion bude stabilně v pasti v závislosti na hodnot pro hmotnost a náboj iontu, velikost iontová past (r), oscilační frekvence základní rf ( w), a amplituda napětí na kroužek elektrody ( V). Závislost iontové pohybu na těchto parametrů je popsán pomocí bezrozměrného parametru qz, qz = 4eV/mr2w2
Kvadrupól
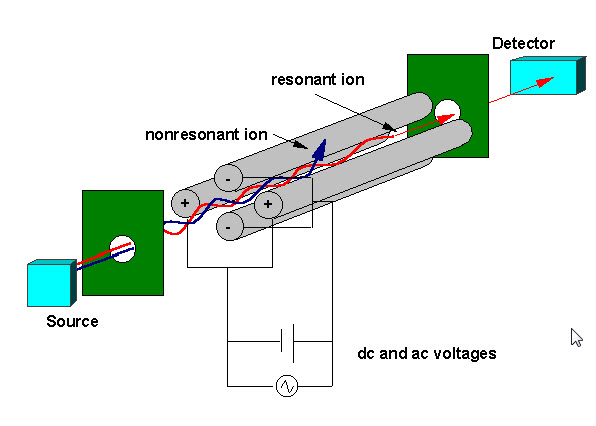
Je kvadrupólový hmotnostní filtr se skládá ze čtyř paralelních kovových tyčí uspořádány jako na obrázku níže. Dvě protilehlé tyče mají aplikovaný potenciál (U+Vcos(wt)) a další dvě tyče mají potenciál -(U+Vcos(wt)), kde U je stejnosměrné napětí a Vcos (wt) je střídavé napětí. Aplikovaná napětí ovlivňují trajektorii iontů cestujících po dráze letu se středem mezi čtyřmi tyčemi. Pro dané stejnosměrné a střídavé napětí procházejí kvadrupólovým filtrem pouze ionty určitého poměru hmotnosti k náboji a všechny ostatní ionty jsou vyhozeny ze své původní dráhy. Hmotnostní spektrum se získá sledováním iontů procházejících kvadrupólovým filtrem, protože napětí na tyčích se mění. Existují dvě metody: různé w a drží U a V konstantní, nebo různé U a V (U/V) pevné pro konstantní w.
kvadrupólový hmotnostní filtr se skládá ze čtyř paralelních kovových tyčí uspořádány jako na obrázku níže. Dvě protilehlé tyče ha
tandemová hmotnostní spektrometrie:
tandemová hmotnostní spektrometrie, obvykle označovaná jako MS/MS, zahrnuje použití 2 nebo více analyzátorů hmotnosti. Často se používá k analýze jednotlivých složek ve směsi. Tato technika přidává specifičnost k dané analýze. Ačkoli tandemová hmotnostní spektrometrie může být označována MS/ MS, MS / MS / MS atd… v této prezentaci budu popisovat pouze MS/MS
základní myšlenkou MS/MS je výběr z m/z daného iontu tvoří v iontovým zdrojem a předmětem tohoto iontu k roztříštěnosti, obvykle srážkou s inertní plyn (např. Argon). Potom se detekují ionty produktu. Jedná se o silný způsob, jak potvrdit identitu určitých sloučenin a určit strukturu neznámých druhů. MS / MS je tedy proces, který zahrnuje 3 kroky: ionizaci, výběr hmoty,analýzu hmotnosti.
MS / MS lze provádět na nástrojích, jako je trojitý kvadrupól (QQQ), iontová past, doba letu, Fourierova transformace atd… Trojitý kvadrupol je nejčastěji používaným hmotnostním spektrometrem pro MS / MS, možná kvůli nákladům a snadnému použití mimo jiné faktory.
Separační Metody pro spojení s hmotnostním Spektrometrem
- GC-MS: Směsi vzorků se přímo odpařují a vstupují do pojených tavených křemičitých kolon. Složky směsi jsou odděleny na základě jejich afinitního rozdílu s vázanou fází. Oddělené sloučeniny opouštějí kolonu a vstupují do vakuového systému hmotnostního spektrometru. Molekuly vzorku jsou ionizovány (EI nebo CI) a akcelerovány do prekalibrovaného hmotnostního analyzátoru (např…). Zaznamenávají se retenční časy, molekulární hmotnosti a fragmentační vzorce. Jedním z nejdůležitějších considirations GC / MS je, že vzorek(y) musí být non termolable význam tepelně stabilní.
- LC-MS: pro sloučeniny, které jsou tepelně nestabilní, se zvažuje metoda LC / ms. Separace je založena na rozdílu afinity vzorků se stacionární fází a mobilní fází. např. hydrofobnost v případě RP chromatografie.
- CZE-MS: Tato metoda je založena na odchylkám z elektroforetické mobility vzorků, kdy kolona z křemenného skla je pod potenciální rozdíl mezi injekce straně a detektor straně.
- CIEF-MS: Jedná se o variantu cze. Je založen na rozdílech v izoelektrických bodech analytů.