このチュートリアルでは、あなたの研究サンプルのための適切な技術と測定を決定する際に役立つ質量分析の基本的な側面について説明します。
- 質量分析とは何ですか?
- 質量分析計
- イオン化方法
- 電子衝撃イオン化
- 化学イオン化
- マトリックス支援レーザー脱着
- 大気圧化学イオン化
- エレクトロスプレイイ
- イオンの分析
- タンデム質量分析
- 質量分析とのカップリングのための分離方法
質量分析とは何ですか?
質量分析は、イオン化分子の気相を以下のいずれかまたは複数の目的で研究する分析技術です:
- 分子量測定
- 構造特性評価
- 気相反応性研究
- 混合物中の成分の定性的および定量的分析。
質量分析は、基本的に気相中のイオンの重量を量ることから構成されています。 使用される器械は高精度と個々の原子および分子の固まりを定める洗練されたバランスとして考慮できる。 試料の化学的および物理的性質に応じて、異なるイオン化技術を使用することができる。 どのイオン化技術を使用するかを選択する主な要因の一つは、熱溶解性である。 揮発性ではなく、比較的揮発性でない試料については、電子衝撃および/または化学イオン化のようなイオン化を効果的に使用することができる。 ペプチド、タンパク質、および生物学的関心のある他のサンプルのような熱安定性のあるサンプルについては、軟質イオン化技術が考慮されるべきで 最も使用されているソフトイオン化技術の中には、エレクトロスプレー(ESI)とマトリックス支援レーザー脱着(MALDI)があります。 特定の質量仕様技術に与えられた名前は、通常、使用されているイオン化方法を指しています。
原子量と分子量は、炭素同位体12Cの質量に対して割り当てられ、その原子量は正確に12と定義されています。 12Cの実際の質量は12ダルトンであり、1ダルトンは1に等しい。分子またはイオンの質量は、ダルトン(D A)またはキロダルトン(KD A)で表すことができる。
質量分析計
質量分析計は、質量分析計と呼ばれる機器を使用しています。 質量分析計の主な構成要素は次のとおりです:
- 入口システム(LC、GC、直接調査等。..イオン源(EI、CI、ESI、APCI、MALDIなど)..)
- 質量分析計(四重極、TOF、イオントラップ、磁気セクター)
- 検出器(電子乗数、マイクロチャネルプレートMcp)
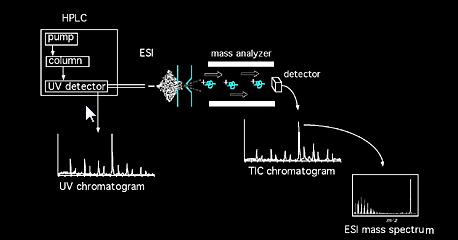
サンプルは、固体プローブを介して直接質量分析計に導入することができ、または混合物の場合には、クロマトグラフィー装置(例えば、ガスクロマトグラフィー、液体クロマトグラフィー、キャピラリー電気泳動など)の仲介によって導入することができる。..). ソースに入ると、サンプル分子はイオン化にさらされます。 源に形成されたイオン(分子イオンおよび断片イオン)は、いくらかの運動エネルギーを獲得し、源を離れる。 較正された分析器は、通過するイオンを質量と電荷の比の関数として分析します。 別の種類の検光子は磁気、Quadrulpole、イオントラップ、フーリエ変換、飛行時間、等使用することができます。..アナライザアセンブリから出るイオンビームが検出され、信号が登録されます。 一般的なイオン化法の略語は次のとおりです:
- EI=電子衝撃;
- CI=化学イオン化;
- SIMS=二次イオン質量Spec;
- FAB=高速原子衝撃;
- LDMS=レーザー脱着質量Spec;
- PDMS=プラズマ脱着質量Spec;
- TS=Thermospray;
- AS=Aerospray;
- ESMS=エレクトロスプレー質量仕様。
一般的な質量分析器の頭字語は次のとおりです:
- EB=静電-磁気;
- IT=イオントラップ;
- Q=四重極;
- TOF=飛行時間。
イオン化方法
サンプルの分析に適したイオン化方法の選択は非常に重要です。 私たちは提案を提供することができますが、あなたの研究化合物に適した方法を理解し、選択することはあなたの責任です。
- 電子衝撃EIイオン化
- 化学イオン化CI
- マイナスイオン化学イオン化
- エレクトロスプレイイオン化技術
- マトリックス支援レーザー脱離(私たちの施設では提供されていませんが、キャンパス内では利用可能です)
- 大気圧化学イオン化APCI
電子衝撃イオン化
M+E-(70ev)—–>M+. +2e-
EIイオン化法は、非熱安定性化合物に適しています。 サンプルのボラティリティが必要です。 蒸気状態のサンプル分子は、従来70eVのエネルギーである高速移動電子によって衝撃される。 これはイオン形成で起因する。 最も高い軌道エネルギーからの1つの電子が取り除かれ、結果として分子イオンが形成される。 この分子イオンのいくつかは分解し、フラグメントイオンが形成される。 与えられたイオンの断片化は、それがイオン化内で必要とするエネルギーの過剰によるものである。 フラグメントイオンは奇数電子または偶数電子であり得る。 電子衝突イオン化で形成される分子イオンは奇数電子イオンである。 奇数電子フラグメントイオンは、直接開裂によって形成される(例えば、 C−C結合の直接開裂)。 電子フラグメントイオンでさえ、転位(例えばプロトン移動)によって形成されることが多い。 試料は、ガスクロマトグラフィー装置を介して、例えば混合物の場合には、または固体プローブ装置を介して直接EI源に導入することができる。 実験に必要な量は、通常、材料のマイクログラムよりも少ないです。
EI質量スペクトルは、ほとんどの場合、強烈なフラグメントイオンピークとはるかに少ない強烈な分子イオンピークを含んでいます。 質量スペクトルで分子イオンピークが観測されない場合,分子イオン情報を得るために化学イオン化を用いることができる。 イオンが分子イオンであるかどうかを決定するための有用なルールの1つは、窒素ルールです。
窒素則:上記のように、EIイオン化で形成される分子イオンは奇数電子イオンである。 それらの観測された質量対電荷比が奇数である場合、調査中の分子は奇数の窒素原子を含む。 その質量対電荷比が偶数である場合、その分子には窒素原子が含まれていないか、または窒素原子さえも含まれていない。
化学イオン化
有機化学者にとって、化学イオン化(CI)は、EI質量スペクトルで分子イオンが観察されない場合や、分子イオンの質量対電荷比を確認する場合に特に有用な技術である。 化学イオン化の技術は電子影響のと事実上同じイオン源装置を、除いて使用します、CIは堅いイオン源および試薬ガスを使用します。 試薬ガス(例えばアンモニア)は、最初に電子衝撃を受ける。 試料イオンは、試薬ガスイオンと試料分子との相互作用によって形成される。 この現象はイオン分子反応と呼ばれます。 試薬ガス分子は、試料分子に対して約1 0 0:1の比で存在する。 CIプロセスでは、正イオンと負イオンが形成されます。 機器の設定(ソース電圧、検出器など)に応じて、次の手順を実行します。..)正イオンのみまたは負イオンのみが記録されます。
CIでは、イオン化された試薬ガス分子(G)と揮発性分析物中性分子(M)との間でイオン分子反応が起こり、分析物イオンを生成する。 擬似分子イオンM h+(正イオンモード)または-(負イオンモード)がしばしば観察される。 EI法で得られた分子イオンとは異なり,MH+および-検出は高収率で起こり,フラグメントイオンは少ない。正イオンモード:
GH++M——>MH++G
負イオンモード:
-+M——> – + G
これらの単純なプロトン移動反応は、ブロンステッド-ローリーの意味での真の気相酸-塩基プロセスである。 「堅い」イオン源(圧力=0.1-2torr)が増加する感受性で起因する衝突を最大にするのに使用されています。 これらのイオン分子反応を起こすには発熱性でなければならない。 プロトン移動は、陽性CIで観察される単純なプロセスの一つである:
RH++M—–>MH++R
この反応における決定的なパラメータの一つは、プロトン親和性である。 反応が起こるためには、分子Mのプロトン親和性は、ガス分子のものよりも高くなければならない。 CIで使用される主な試薬ガスは、アンモニア、メタン、イソブタンです。 形成される主な反応物イオンは、以下に示すメカニズムで与えられる。 試薬ガスの選択は準分子イオンの断片化の程度に影響する。
:
- CH4 + e —–> CH4+. + 2e ——> CH3+ + H.
- CH4+. + CH4 —–> CH5+ +CH3.
- CH4+. + CH4 —–> C2H5+ + H2 + H.
Isobutane (positive ion chemical ionization):
- i-C4H10 + e —–> i-C4H10+. + 2e
- i-C4H10+. + i-C4H10 ——> i-C4H9+ + C4H9 +H2
Ammonia (positive ion chemical ionization):
- NH3 + e —–> NH3+. + 2e
- NH3+. + NH3 ——> NH4+ + NH2.
- NH4++NH3———>N2H7+
メタン正イオンモードの化学イオン化では,観測された関連する試料ピークはM h+,+,+であるが,主にM h+である。 これは質量M+1、M+29、およびM+41に対応します。
イソブタン正イオンモード化学イオン化では、観測される主なピークはMH+である。
アンモニア正イオンモードの化学イオン化では、観測される主なピークはMH+、および+である。 複数のプロトン化部位が存在する場合、追加のNH3付加体は+に対応することが見られるかもしれない。 これは質量M+1、M+18、およびM+35に対応します。
場合によっては、プロトン化された二量体または他の付加体が見られることがあり、h2Oの損失に続いてプロトン化または付加体イオン形成が見 あなたが観察するスペクトルが適切な付加物イオンを示さないように見えるか、または広範な断片化を示す場合は、結果を解釈しようとするときに 化合物の特定のクラスに適用可能な化学イオン化機構を議論する文献で利用可能なデータの豊富さがあります。
二つの要因が使用されるレーガントガスの選択を決定します:
- プロトン親和性PA
- エネルギー移動
NH3(アンモニア)は、例えばCH5+と比較してNH4+のエネルギー移動が低いため、CIで最も使用されている試薬ガ 試薬ガスとしてNH3を用いると、通常MH+およびMNH4+(17の質量単位の相違)が観察されます。
マイナスイオン化学イオン化
三つのメカニズムに下線を付けることができます:
- サンプル分子により効率的に転送することができる低速移動、低エネルギー”熱化”電子の達成に起因する電子捕獲反応。
- イオン化試薬ガスからの電子移動(例えば、NH2-NH2よりも大きな電子親和性を有する分子に電子を移動させることができる)。
- 試薬ガスイオンは真のCI反応に関与する(例えば、プロトンの引抜き、相対酸性度による)。
負イオン化学イオン化質量スペクトルで観測される分子イオンは、通常M-または-である。
エレクトロスプレイイオン化法
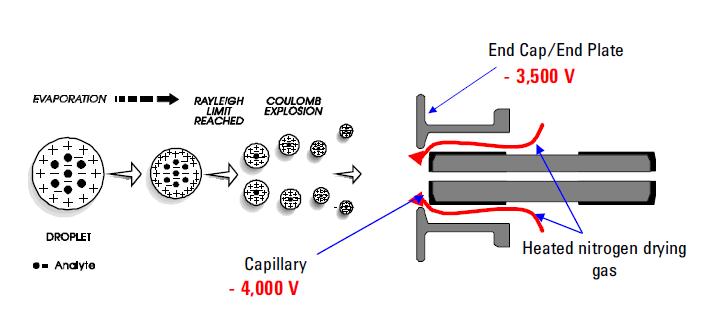
最も使用されているスプレーイオン化技術の中には、エレクトロスプレイイオン化(ESI)があります。 この技術は、熱不安定性化学物質を分析するための選択の方法であり続けています。 その機能は十分に文書化されています。 それはESIの調査の出口(例えば毛管)と調査からの数ミリメートルにある反対電極間の電気圧力を使用する。 このプロセスは、注入された溶液から直接高度に帯電した液滴を生成する。 噴霧された液滴から多重および/または単独に帯電した分析物分子を脱着させ、質量分析計の残りの部分を介してサンプリングする。 ESIは蛋白質およびDNAの片のようなポリマーの大きい変化から荷電分子イオンを増加する作り出す機能のために区別されました;それは薬剤および 正または負のイオンの形成(印加された電場の符号に依存する)は、高収率で起こる。 正イオンモードではプロトン化および/またはアルカリ付加物分析物分子が質量スペクトルで一般に観察された。 負イオンモードでは,脱プロトン化された分析物分子に対応するピークが観察された。 ESIは,周囲の浴ガスが脱離イオンの内部および並進エネルギーに対して緩和効果を有する非常に”柔らかい”イオン化技術として記述されている。
ESIの利点:
- 柔らかいイオン化プロセスので、無傷の分子イオンが観察される
- ESIは、乗算荷電イオンの生成を可能にする。 これは最も利用できる多くの検光子(例えば四重極)を使用して非常に高分子量種を分析する能力で起因する。
- ESIは大気圧プロセスです。 これにより、使いやすく、HPLCおよびCE分離技術とのインターフェイスが容易になります。
マトリックスアシストレーザー脱着(MALDI)
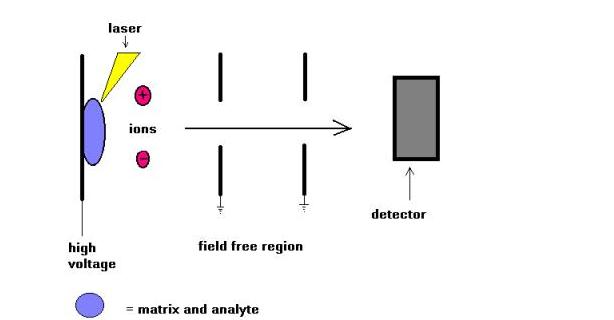
マトリックス支援レーザー脱離(MALDI)質量分析技術は、ペプチドとタンパク質のイオン化のために1988年にKarasとHillkampによって導入されました。 すぐにそこにこの技術は、オリゴ糖、糖脂質、ヌクレオチド、および合成ポリマーなどの生体分子の他のタイプを、分析することができた後。 この技術では、サンプルはマトリックスと呼ばれる紫外線吸収物質と共結晶化されます。 例えば蛋白質のために、選択のマトリックスは頻繁にsinapinic酸です。 窒素レーザーからの337nmの放射が最も一般的に使用されます。 レーザーは熱分解を防ぐような方法で分子システムにエネルギーを導入するのを助ける。
MALDIは、この技術のパルス性と質量範囲能力のために、飛行時間質量分析計(TOF)でよく使用されます。 数百のダルトンまでの分子量を測定することができた。 ここ数年,MALDIとESIイオン化技術の比較を試みた。 私の意見では、これら二つの技術は競争力が、補完的ではありません。 いくつかの例を挙げると、高分子量種の場合、MALDIは単独で荷電した分子イオンの形成をもたらし、ESIは乗算荷電した分子イオンの形成を可能にする。
:
- 最終的なモル比のサンプル/マトリックスは約1/5000またはその周りです。
- サンプルの最終濃度は1-10pmol/ul
- MALDIの経験は、100fmol/ulから数百pmol/ulのダイナミックレンジを指しています
- MALDIは、塩および界面活性剤および緩衝剤の使 それはより良いパフォーマンスのためにそれらを削除するのが最善ですが。
MALDIのペプチドおよびタンパク質標準:
- アンギオテンシンII(ヒト)MW:1046.2
- Substance P(ヒト)MW:1347.7
- Insulin(ウシ)MW:5733.6
- Cytochrom c(ウマ)MW:12,360.1
- RNase A(ウシ)MW: 13,682.2
- アポミオグロビン(馬): 16,951.5
- トリプシノーゲン(ウシ): 23,980.9
大気圧化学イオン化
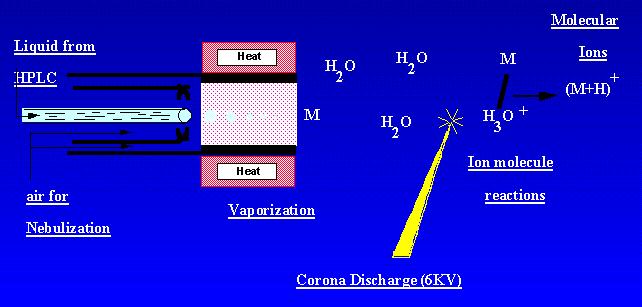
APCIは、大気圧でイオンを生成する技術です。 サンプル解決は霧で揮発し、窒素のnebulizationの援助とのコロナ放電に吹きかかる熱くする管を通って流れます。 試料分子はアンビエントコロナ放電イオンからのイオン分子反応によってイオン化される。 イオンは放電中に生成され、質量分析計に抽出される。 APCIは、比較的極性の半揮発性のサンプルに最適です。 APCI質量スペクトルは通常,準分子イオン,-または+を含んでいた。
イオンの分析
質量分離を達成するために、いくつかの異なる物理パラメータを使用することが可能です。 一般的なタイプの質量分析器については、以下で説明します。 それぞれに長所と短所があります。 私達の設備で私達は現在四重極、イオントラップ、amd飛行時間(TOF)の質量分析計を有する。
磁気セクター質量分析計
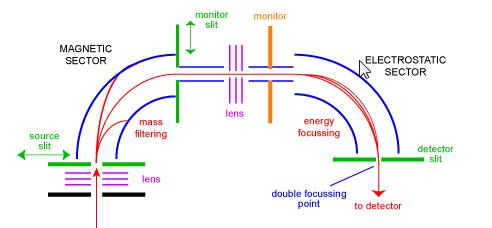
セクター質量分析計は、質量分析器の最も一般的なタイプの一つであり、おそらく日常の科学者に最もよく知られていました。 1950年代には、最初の商業的な質量分析計はセクターの器械だった。 それらは、大きな電磁気とある種の静電集束装置のいくつかの組み合わせで構成されています。 異なった製造します使用相違の幾何学を。 図1は、標準的な”BE”ジオメトリの二重焦点測定器の概略図を示しています。 BE構成はまた逆の幾何学のセクターの質量分析計と呼ばれる-すなわち、静電気のセクターに先行している磁気セクターから成っている二重セクターの器械。
イオンは、最初に焦点が当てられているソース(左下)から機器に入ります。 それらは左の規則に従って逸らされる源スリットを通して磁気セクターに入る。 高質量イオンは、低質量イオンよりも偏向されない。 磁石をスキャンすることは異なった固まりのイオンがモニタースリットに集中されることを可能にする。 この段階では、イオンはその質量によってのみ分離されている。 同じm/zを持つすべてのイオンがスペクトル内の一つのピークと一致するように見える良好な分解能のスペクトルを得るためには、イオンはその運動エネルギーによってフィルタリングされなければならない。 イオンを集束させる別の段階の後、同じm/zのイオンがエネルギー分布を補正し、検出器スリット上の二重集束点に集束される静電セクターに入る。
セクター機器は、高解像度データを取得する唯一の実用的な方法であったため、1950年代と1960年代に大きな商業的成功を収めました。 最後の20年かそこらでは、FTMの価格の低下と高解像度の代替(例えばQ-Tof)セクターの機器の開発では減少しています。
飛行時間質量分析(TOF-MS)
飛行時間質量分析装置は、異なる質量のイオンを分離するためにドリフト領域を通過する通過時間の差を使用します。 それは脈打ったモードで作動する従ってイオンは脈拍で作り出されるか、または得られなければならない。 電場はすべてのイオンを運動エネルギーがqvの無磁場ドリフト領域に加速し,qはイオン電荷,Vは印加電圧である。 イオン運動エネルギーは0.5mv2であるため、軽いイオンは重いイオンよりも高い速度を持ち、ドリフト領域の終わりに早く検出器に到達する。
:
- K.E. =qV
- 1/2mv2=qV
- v=(2qv/m)1/2
ドリフトチューブを通る通過時間(t)はL/vであり、Lはドリフトチューブの長さである
- t=L/(2V/m/q)1/2
リニアTOF-MSの回路図

この回路図は、パルスレーザーによる固体試料からのイオンのアブレーションを示しています。 反射鏡は、イオンミラーとして機能する一連のリングまたはグリッドです。 このミラーはイオンがドリフト領域に入るときの運動エネルギーの広がりを補償し,測定器の分解能を改善した。 イオン検出器の出力は、質量スペクトルを生成するために時間の関数としてオシロスコープに表示されます。
イオントラップ
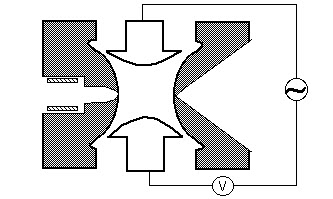
電子衝撃(E i),エレクトロスプレー(ESI),またはマトリックス支援レーザ脱着(MALDI)イオン化によって生成されたイオンは,静電レンズシステムを用いてイオントラップに集束される。 静電イオンゲートパルスはイオントラップにイオンを注入するために開いた(-V)および閉じた(+V)。 イオンゲートの脈打つことはイオンが質量分析器に絶えず入る四重極のような”ビーム”の器械からのイオントラップを区別する。 “イオン化持続時間”と呼ばれるイオンがトラップに入る時間は、空間電荷効果を最小限に抑えながら信号を最大化するように設定されています。 空間電荷は、トラップ内のイオンが多すぎるため、電界の歪みが発生し、性能が全体的に低下します。 イオントラップは、典型的には約1mtorrの圧力までヘリウムで満たされている。 ヘリウムとの衝突はイオンの運動エネルギーを減衰させ、イオントラップの中心に向かって軌道を迅速に収縮させ、注入されたイオンのトラップを可能にする。 トラップされたイオンは、リング電極に印加される基本rfと呼ばれる振動電位を使用することにより、トラップの中心に向かってさらに集束され イオンは、イオンの質量と電荷、イオントラップの大きさ(r)、基本rfの振動周波数(w)、リング電極上の電圧の振幅(V)の値に応じて安定にトラップされます。 これらのパラメータに対するイオン運動の依存性は、無次元パラメータqz、qz=4ev/mr2w2
四重極によって記述されます
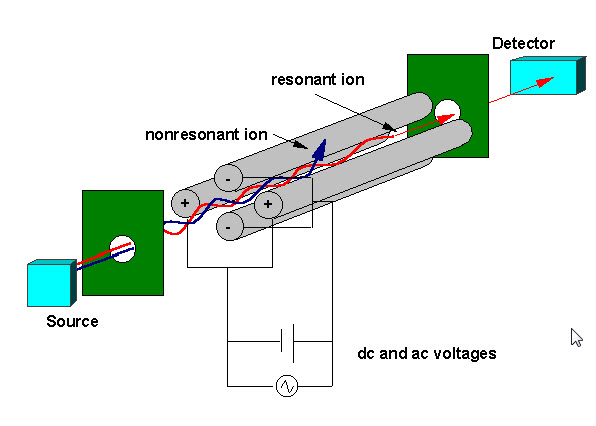
四重極質量フィルタは、下の図のように配置された四つの平行な金属棒で構成されています。 対向する2つのロッドは、印加電位(U+Vcos(w t))を有し、他の2つのロッドは、−(U+Vcos(w t))の電位を有し、ここで、Uは、dc電圧であり、Vcos(w t)は、a c電圧である。 印加された電圧は,四つの棒の間を中心とする飛行経路を通過するイオンの軌道に影響を与える。 与えられたdc電圧とac電圧では、ある質量電荷比のイオンのみが四重極フィルタを通過し、他のすべてのイオンは元の経路から投げ出されます。 ロッド上の電圧が変化するときに四重極フィルタを通過するイオンを監視することによって質量スペクトルを得た。 Wを変化させてUとVを一定に保持する方法と、定数wに対してuとV(U/V)を固定する方法があります。
四重極質量フィルタは、下の図のように配置された四つの平行な金属棒で構成されています。 ハ
タンデム質量分析:
タンデム質量分析は、通常MS/MSと呼ばれ、2つ以上の質量分析装置を使用する。 これは、混合物中の個々の成分を分析するためによく使用されます。 この手法は、特定の分析に特異性を追加します。 タンデム質量分析法は、MS/MS、MS/MS/MSなどと呼ぶことができるが、ms/MS/MSなどと呼ぶことができる。.. MS/MSの基本的な考え方は、イオン源に形成された所与のイオンのm/zの選択であり、通常は不活性ガスとの衝突によって、このイオンを断片化させる(例: アルゴン)。 その後、生成物イオンが検出される。 これは、特定の化合物の同一性を確認し、未知の種の構造を決定する強力な方法です。 したがって、MS/MSは、イオン化、質量選択、質量分析の3つのステップを含むプロセスです。
MS/MSは、三重四重極(QQQ)、イオントラップ、飛行時間、フーリエ変換などの機器で実行できます。.. 三重の四重極は他の要因間の費用そして使い易さのためにMS/MSのための最も頻繁に使用された質量分析計、多分である。
質量仕様
- GC-MSとの結合のための分離方法: 試料混合物は直接気化し、結合石英ガラスカラムに入ります。 混合物の成分は、結合相との親和性の差に基づいて分離される。 分離された化合物はカラムを出て、質量分析計の真空システムに入る。 サンプル分子はイオン化され(EI、かCI)、precalibrated質量分析装置(例えばQ、イオントラップ、TOF、FTMS等)に加速されます。..). 保持時間、分子量、および断片化パターンが記録されます。 GC/MSの最も重要な考察の一つは、サンプル(複数可)は、熱的に安定な意味非熱安定でなければならないということです。
- LC-MS:熱的に不安定な化合物については、LC/MS法を検討します。 分離は静止相および移動相との試料の親和性の相違に基づいている。 例えば、RPクロマトグラフィーの場合の疎水性。
- CZE-MS:この方法は、石英ガラスカラムが注入側と検出器側の電位差の下にあるときの試料の電気泳動移動度の回折に基づいています。
- CIEF-MS:これはCZEの変種です。 それはanalytesの等電点のdiffrerencesに基づいています。