Questo tutorial discute gli aspetti di base della spettrometria di massa che ti saranno utili per decidere le tecniche e le misurazioni corrette per i tuoi campioni di ricerca.
- Che cos’è la spettrometria di massa?
- Lo Spettrometro Di Massa
- Metodi Di Ionizzazione
- Impatto Di Elettroni Di Ionizzazione
- Ionizzazione Chimica
- Matrix Assisted Laser Desorption
- Ionizzazione Chimica A Pressione Atmosferica
- Ionizzazione Electrospray
- Analisi di Ioni
- Spettrometria di Massa Tandem
- Metodi di Separazione per l’Accoppiamento con i Mass Spec
che Cosa è la Spettrometria di Massa?
spettrometria di Massa è una tecnica analitica che prevede lo studio in fase gas di molecole ionizzate con l’obiettivo di uno o più dei seguenti:
- determinazione del peso Molecolare
- caratterizzazione Strutturale
- Gas fase di studio di reattività
- analisi Qualitativa e quantitativa dei componenti di una miscela.
La spettrometria di massa consiste essenzialmente nel pesare gli ioni nella fase gassosa. Lo strumento utilizzato potrebbe essere considerato come un sofisticato equilibrio che determina con alta precisione le masse dei singoli atomi e molecole. A seconda delle proprietà chimiche e fisiche dei campioni, è possibile utilizzare diverse tecniche di ionizzazione. Uno dei fattori principali nella scelta della tecnica di ionizzazione da utilizzare è la termolabilità. Per i campioni che non sono themolable e relativamente volatile, la ionizzazione quale impatto dell’elettrone e/o la ionizzazione chimica può efficacemente essere usata. Per campioni che sono termolabili come peptidi, proteine e altri campioni di interesse biologico, sono da considerare tecniche di ionizzazione morbida. Tra le tecniche di ionizzazione soft più utilizzate ci sono Electrospray (ESI) e Matrix Assisted Laser Desorption (MALDI). Il nome dato a una particolare tecnica di spec di massa di solito punta al metodo di ionizzazione utilizzato.
Le masse atomiche e molecolari sono assegnate rispetto alla massa dell’isotopo del carbonio, 12C, il cui peso atomico è definito esattamente come 12. La massa effettiva di 12C è 12 dalton, con un dalton è uguale a 1.661 10-24 g. La massa di una molecola o di uno ion può essere presentata in dalton (Da) o kilodaltons (kDa).
Lo spettrometro di massa
Spettrometria di massa utilizza uno strumento chiamato spettrometro di massa. I componenti principali di uno spettrometro di massa sono:
- Sistema dell’entrata (LC, GC, sonda diretta ecc…)
- Sorgente ionica (EI, CI, ESI, APCI, MALDI, ecc…)
- analizzatore di Massa (Quadrupolo, TOF, Trappola Ionica, a Settore Magnetico)
- Rilevatore (Electron Multiplier, Micro Piastre Canale MCPs)
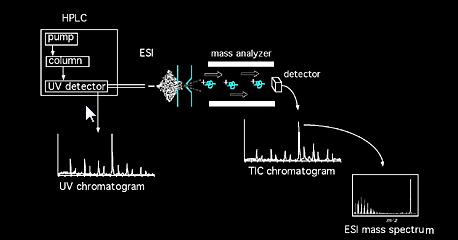
i Campioni possono essere introdotte per lo spettrometro di massa direttamente via solidi sonda, o, nel caso di miscele, dall’intermediario di cromatografia dispositivo (ad esempio, Gas-cromatografia, cromatografia Liquida, elettroforesi Capillare, etc…). Una volta nella fonte, le molecole del campione sono sottoposte a ionizzazione. Gli ioni formati nella sorgente (ioni molecolari e frammenti) acquisiscono una certa energia cinetica e lasciano la sorgente. Un analizzatore calibrato analizza quindi gli ioni che passano in funzione del loro rapporto massa / carica. Possono essere utilizzati diversi tipi di analizzatori, magnetici, quadrulpoli, trappola ionica, trasformata di Fourier, tempo di volo, ecc…Il fascio ionico che esce dal gruppo analizzatore viene quindi rilevato e il segnale viene registrato. Gli acronimi comuni del metodo di ionizzazione includono:
- EI = Electron Impact;
- CI = Ionizzazione chimica;
- SIMS = Ioni secondari Mass Spec;
- FAB=Bombardamento atomico veloce;
- LDMS=Laser Desorption Mass Spec;
- PDMS = Plasma Desorption Mass Spec;
- TS = Thermospray;
- AS=Aerospray;
- ESMS=Spec.di massa dell’elettrospray.
Gli acronimi comuni dell’analizzatore di massa includono:
- EB = Elettrostatico-magnetico;
- IT=trappola ionica;
- Q=Quadrupolo;
- TOF=Tempo di volo.
Metodi di ionizzazione
La selezione del metodo di ionizzazione corretto per l’analisi del campione è estremamente importante. Anche se siamo in grado di offrire suggerimenti, è vostra responsabilità di comprendere e selezionare il metodo(s) appropriato per i composti di ricerca.
- Impatto di Elettroni di Ionizzazione EI
- Ionizzazione Chimica a CI
- Ioni Negativi Ionizzazione Chimica
- Tecniche di Ionizzazione Electrospray
- Matrix Assisted Laser Desorbimento (non disponibile nella nostra struttura, ma disponibili altrove sul campus)
- Ionizzazione Chimica a Pressione Atmosferica APCI
Impatto di Elettroni di Ionizzazione
M + e-(70eV) —–> M+. + 2e –
Il metodo di ionizzazione EI è adatto per composti non termolabili. È richiesta la volatilità del campione. Molecole campione in stato di vapore sono bombardati da elettroni in rapido movimento, convenzionalmente 70 energia eV. Ciò si traduce in formazione di ioni. Un elettrone dalla più alta energia orbitale viene spostato e di conseguenza si formano ioni molecolari. Alcuni di questi ioni molecolari si decompongono e si formano ioni frammenti. La frammentazione di un dato ion è dovuta all’eccesso di energia che richiede all’interno della ionizzazione. Gli ioni frammenti possono essere elettrone dispari o addirittura elettrone. Gli ioni molecolari formati nella ionizzazione a impatto elettronico sono ioni elettronici dispari. Gli ioni dispari del frammento dell’elettrone sono formati dalla scissione diretta(per esempio scissione diretta di un legame C-C). Anche gli ioni di frammenti di elettroni sono spesso formati da riarrangiamento (ad esempio trasferimento di protoni). Il campione può essere introdotto alla sorgente EI tramite un dispositivo di gascromatografia, ad esempio nel caso di miscele, o direttamente tramite un dispositivo di sonda solidi. Le quantità necessarie per un esperimento sono solitamente inferiori a un microgramma di materiale.
Gli spettri di massa EI, nella maggior parte dei casi, contengono picchi di ioni di frammenti intensi e picchi di ioni molecolari molto meno intensi. Quando il picco di ioni molecolari non viene osservato nello spettro di massa, è possibile utilizzare la ionizzazione chimica per ottenere informazioni sugli ioni molecolari. Una regola utile per determinare se uno ion è uno ion molecolare è la regola dell’azoto.
Regola dell’azoto :come indicato sopra, gli ioni molecolari formati nella ionizzazione EI sono ioni elettronici dispari. Se il loro rapporto massa / carica osservato è dispari, la molecola in esame contiene un numero dispari di atomi di azoto. Se quel rapporto massa-carica è un numero pari, quella molecola non contiene atomi di azoto o addirittura.
Ionizzazione chimica
Per i chimici organici, la ionizzazione chimica (CI) è una tecnica particolarmente utile quando non si osserva uno ion molecolare nello spettro di massa EI e anche nel caso di conferma del rapporto massa / carica dello ion molecolare. Tecnica di ionizzazione chimica utilizza praticamente lo stesso dispositivo sorgente di ioni come in impatto elettronico, tranne, CI utilizza sorgente di ioni stretto, e gas reagente. Il gas reagente (ad esempio ammoniaca) viene prima sottoposto all’impatto degli elettroni. Gli ioni campione sono formati dall’interazione di ioni gas reagenti e molecole campione. Questo fenomeno è chiamato reazioni ion-molecole. Le molecole di gas reagente sono presenti nel rapporto di circa 100: 1 rispetto alle molecole del campione. Ioni positivi e ioni negativi si formano nel processo CI. A seconda della configurazione dello strumento(tensioni di sorgente, rivelatore, ecc…) vengono registrati solo ioni positivi o solo ioni negativi.
In CI, le reazioni della molecola dello ion accadono fra le molecole ionizzate del gas del reagente (G) e le molecole neutrali volatili dell’analita (M) per produrre gli ioni dell’analita. Spesso si osservano ioni pseudo-molecolari MH+ (modalità ioni positivi) o – (modalità ioni negativi). A differenza degli ioni molecolari ottenuti nel metodo EI, il rilevamento MH+ e-avviene in alta resa e si osservano meno ioni di frammenti.
Modalità di ioni positivi:
GH + + M – – – – – – > MH+ + G
Modalità di ioni negativi:
– + M ——> – + G
Queste semplici reazioni di trasferimento di protoni sono veri processi acido-Base in fase gassosa nel senso di Bronsted-Lowrey. Una sorgente di ioni “stretta” (pressione=0,1-2 torr) viene utilizzata per massimizzare le collisioni che si traducono in un aumento della sensibilità. Per avere luogo queste reazioni di molecole ioniche devono essere esotermiche. Il trasferimento di protoni è uno dei semplici processi osservati in CI positivo:
RH+ + M —–> MH+ + R
Uno dei parametri decisivi in questa reazione è l’affinità del protone. Perché la reazione si verifichi, l’affinità protonica della molecola M deve essere superiore a quella della molecola del gas. I principali gas reagenti utilizzati nell’IC sono: Ammoniaca, metano e isobutano. Gli ioni reagenti predominanti formati sono indicati nei meccanismi mostrati di seguito. La scelta del gas reagente influisce sull’entità della frammentazione dello ion quasi-molecolare.
Metano (ionizzazione chimica a ioni positivi):
- CH4 + e —–> CH4+. + 2e ——> CH3+ + H.
- CH4+. + CH4 —–> CH5+ +CH3.
- CH4+. + CH4 —–> C2H5+ + H2 + H.
Isobutane (positive ion chemical ionization):
- i-C4H10 + e —–> i-C4H10+. + 2e
- i-C4H10+. + i-C4H10 ——> i-C4H9+ + C4H9 +H2
Ammonia (positive ion chemical ionization):
- NH3 + e —–> NH3+. + 2e
- NH3+. + NH3 ——> NH4+ + NH2.
- NH4+ + NH3 ———>N2H7+
Nella ionizzazione chimica del modo dello methane positivo del metano i picchi rilevanti del campione osservati sono MH+, + e +; ma pricipalmente MH+. Ciò corrisponde alle masse M + 1, M + 29 e M + 41.
Nella ionizzazione chimica del modo dello ion positivo dell’isobutano il picco principale osservato è MH+.
Nella ionizzazione chimica del modo dello ammonia positivo dell’ammoniaca i picchi principali osservati sono MH+ e +. Se è presente più di un sito di protonazione, possono essere osservati addotti aggiuntivi di NH3 corrispondenti a +. Ciò corrisponde alle masse M + 1, M + 18 e M + 35.
In alcuni casi, dimeri protonati o altri addotti potrebbero essere visti; perdita di H2O seguita da protonazione o formazione di ioni addotti è visto per alcune classi di composti. Se lo spettro che osservi non sembra mostrare gli ioni addotti appropriati, o mostra un’ampia frammentazione, fai attenzione quando cerchi di interpretare i risultati. C’è un’abbondanza di dati disponibili nella letteratura che discute i meccanismi di ionizzazione chimica applicabili a classi specifiche di composti.
Due fattori determinano la scelta del gas reagente da utilizzare:
- Proton affinity PA
- Trasferimento di energia
NH3 (ammoniaca) è il gas reagente più utilizzato in CI a causa del basso trasferimento di energia di NH4+ confronta con CH5+ per esempio. Con NH3 come gas reagente, di solito si osservano MH+ e MNH4+ (differenza di 17 unità di massa).
Ionizzazione chimica di ioni negativi
Tre meccanismi possono essere sottolineati:
- Reazione di cattura elettronica dovuta al raggiungimento di elettroni “termalizzati” a bassa energia che possono essere trasferiti in modo più efficiente alle molecole del campione.
- Trasferimento di elettroni dal gas reagente ionizzato (ad esempio NH2 – può trasferire un elettrone a una molecola con una maggiore affinità elettronica rispetto a NH2).
- Gli ioni gas reagenti partecipano alle vere reazioni dell’IC (ad es. astrazione di protoni, in base alle acidità relative).
Gli ioni molecolari osservati negli spettri di massa di ionizzazione chimica degli ioni negativi sono solitamente M – o -.
Metodo di ionizzazione Elettrospray
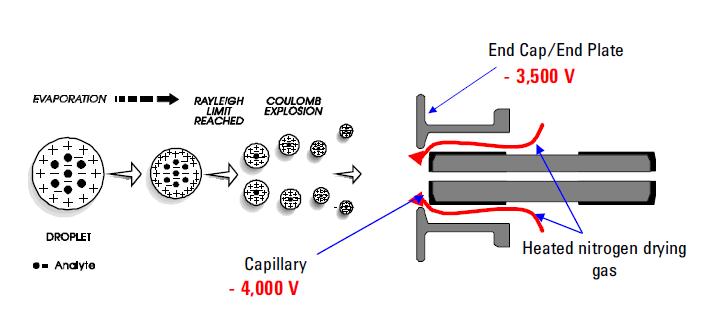
Tra le tecniche di ionizzazione a spruzzo più utilizzate c’è la ionizzazione Elettrospray (ESI). Questa tecnica continua ad essere il metodo di scelta per l’analisi di sostanze chimiche termolabili. Le sue capacità sono ben documentate. Utilizza una sollecitazione elettrica tra l’uscita della sonda ESI (ad esempio capillare) e il contatore elettrodo, che si trova a pochi millimetri dalla sonda. Il processo si traduce nella generazione di goccioline altamente cariche direttamente dalla soluzione infusa. Moltiplicare e / o molecole di analita singolarmente cariche desorbe dalle goccioline spruzzate e campionate attraverso il resto dello spettrometro di massa. ESI si è distinto per la sua capacità di produrre ioni molecolari carichi moltiplicati da una grande varietà di polimeri come proteine e frammenti di DNA; consente anche il rilevamento sensibile di specie polari a basso peso molecolare caricate singolarmente come farmaci e metaboliti di farmaci. La formazione di ioni positivi o negativi (a seconda del segno del campo elettrico applicato) avviene in alta resa. In modo ionico positivo protonato e/o alcali addotto molecole analita generalmente osservati negli spettri di massa. Nella modalità di ioni negativi si osservano picchi di funzionamento corrispondenti a molecole di analita deprotonato. L’ESI è descritto come una tecnica di ionizzazione molto “morbida” in cui il gas del bagno circostante ha un effetto moderatore sulle energie interne e traslazionali degli ioni desorbiti.
Vantaggi di ESI:
- Processo di ionizzazione morbido così si osservano ioni molecolari intatti
- ESI consente la produzione di ioni carichi moltiplicati. Ciò si traduce nella capacità di analizzare specie ad altissimo peso molecolare utilizzando gli analizzatori di massa più disponibili (ad esempio quadrupoli).
- ESI è un processo a pressione atmosferica. Questo lo rende facile da usare e facile da interfacciare con tecniche di separazione HPLC e CE.
Desorbimento laser assistito da matrice (MALDI)
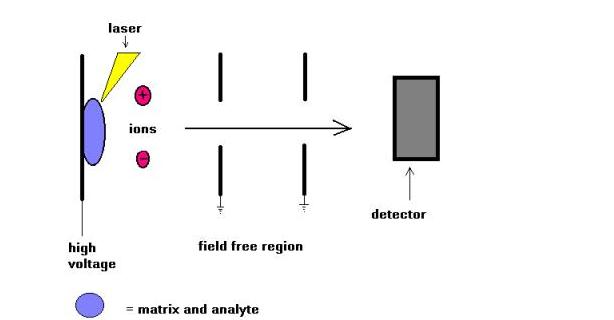
La tecnica di spettrometria di massa MALDI (Matrix Assisted Laser Desorption) è stata introdotta da Karas e Hillkamp nel 1988 per la ionizzazione di peptidi e proteine. Presto dopo questa tecnica è stato in grado di analizzare altri tipi di biomolecole, come oligosaccaridi, glicolipidi, nucleotidi e polimeri sintetici. In questa tecnica, i campioni sono cocristallizzati con una sostanza che assorbe i raggi UV chiamata matrice. Ad esempio per le proteine, la matrice di scelta è spesso l’acido sinapinico. Una radiazione di 337 nanometro dal laser dell’azoto è più comunemente usata. Il laser aiuta a introdurre energia nel sistema molecolare in modo tale da prevenire la decomposizione termica.
MALDI è spesso usato con spettrometri di massa a tempo di volo (TOF) a causa della natura pulsante della tecnica e della capacità di gamma di massa. È stato possibile misurare pesi molecolari fino a poche centinaia di dalton. Il confronto delle tecniche di ionizzazione MALDI ed ESI è stato tentato negli ultimi anni. A mio parere queste due tecniche non sono competitive ma complementari. Solo per citarne alcuni, per le specie ad alto peso molecolare, MALDI porta alla formazione di ioni molecolari con carica singola mentre ESI consente la formazione di ioni molecolari con carica multipla.
Considerazioni pratiche:
- Il rapporto molare finale campione / matrice è di circa o circa 1/5000.
- La concentrazione finale del campione è da 1 a 10 pmol/ul
- La nostra esperienza con MALDI punta a una gamma dinamica di 100 fmol/ul a poche centinaia pmol / ul
- MALDI è una tecnica di ionizzazione relativamente robusta che tollera l’uso di sali e tensioattivi e tamponi. Anche se è meglio rimuoverli per migliorare le prestazioni.
Standard peptidici e proteici per MALDI:
- Angiotensina II (umana) MW: 1046,2
- Sostanza P (umana) MW: 1347,7
- Insulina (bovina) MW: 5733,6
- Cytochrom c (equina) MW: 12.360.1
- Rnasi A (bovino) MW: 13,682.2
- Apo-Mioglobina (equini) MW: 16,951.5
- Tripsinogeno (bovino) MW: 23,980.9
Ionizzazione Chimica a Pressione Atmosferica
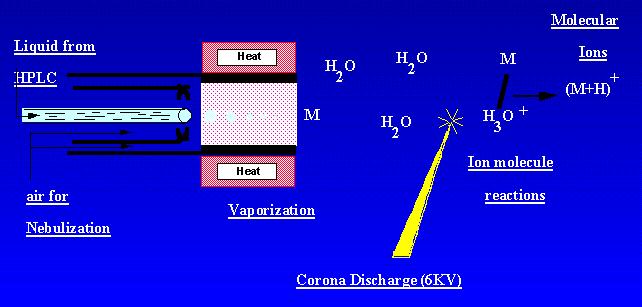
APCI è una tecnica che crea ioni a pressione atmosferica. Una soluzione del campione scorre attraverso un tubo riscaldato dove viene volatilizzata in una nebbia e spruzzata in una scarica a corona con l’aiuto della nebulizzazione dell’azoto. Il campione molecolare è ionizzato dalle reazioni della molecola dello ion dagli ioni di scarico della corona ambiant. Gli ioni sono prodotti nello scarico ed estratti nello spettrometro di massa. APCI è più adatto a campioni relativamente polari e semi-volatili. Uno spettro di massa APCI di solito conteneva lo ion quasi-molecolare, – o +.
Analisi degli ioni
È possibile utilizzare diversi parametri fisici per ottenere la separazione della massa. I tipi comuni di analizzatori di massa sono discussi di seguito. Ognuno ha vantaggi e svantaggi. Nella nostra struttura abbiamo attualmente quadrupolo, trappola ionica, amd Time-of-Flight (TOF) spettrometri di massa.
Settore magnetico spettrometro di massa
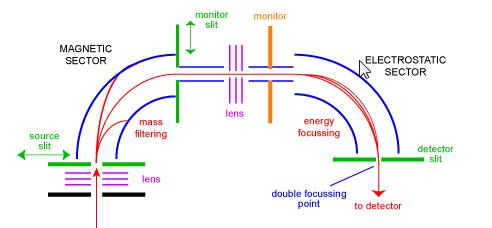
Lo spettrometro di massa settoriale era uno dei tipi più comuni di analizzatori di massa e probabilmente il più familiare allo scienziato di tutti i giorni. Nel 1950, i primi spettrometri di massa commerciali erano strumenti di settore. Sono costituiti da una combinazione di un grande elettromagnetico e da una sorta di dispositivo di messa a fuoco elettrostatica. Diversi produttori utilizzano geometrie diverse. Figura 1 mostra uno schema di uno strumento di messa a fuoco doppia geometria standard’ BE’. La configurazione BE è anche chiamata spettrometro di massa a settore geometrico inverso , ovvero uno strumento a doppio settore costituito da un settore magnetico seguito da un settore elettrostatico.
Gli ioni entrano nello strumento dalla sorgente (in basso a sinistra) dove vengono inizialmente focalizzati. Entrano nel settore magnetico attraverso la fessura della sorgente dove vengono deviati secondo la regola della mano sinistra. Gli ioni di massa superiore sono deviati meno degli ioni di massa inferiore. La scansione del magnete consente di focalizzare ioni di diverse masse sulla fessura del monitor. In questa fase, gli ioni sono stati separati solo dalle loro masse. Per ottenere uno spettro di buona risoluzione in cui tutti gli ioni con lo stesso m/z appaiono coincidenti come un picco nello spettro, gli ioni devono essere filtrati dalle loro energie cinetiche. Dopo un’altra fase di messa a fuoco gli ioni entrano nel settore elettrostatico dove gli ioni dello stesso m/z hanno le loro distribuzioni di energia corrette e sono focalizzati nel doppio punto di messa a fuoco sulla fessura del rivelatore.
Sector instruments ha avuto enormi successi commerciali negli anni ’50 e’ 60 in quanto erano l’unico modo pratico per ottenere dati ad alta risoluzione. Negli ultimi 20 anni o giù di lì, con la diminuzione dei prezzi delle FTM e lo sviluppo di alternative ad alta risoluzione (ad esempio Q-Tof) strumenti del settore sono in declino.
Spettrometria di massa a tempo di volo (TOF-MS)
Uno spettrometro di massa a tempo di volo utilizza le differenze nel tempo di transito attraverso una regione di deriva per separare gli ioni di masse diverse. Funziona in modalità pulsata, quindi gli ioni devono essere prodotti o estratti in impulsi. Un campo elettrico accelera tutti gli ioni in una regione di deriva senza campo con un’energia cinetica di qV, dove q è la carica ionica e V è la tensione applicata. Poiché l’energia cinetica dello ion è 0. 5mv2, gli ioni più leggeri hanno una velocità più alta degli ioni più pesanti e raggiungono il rivelatore all’estremità della regione della deriva prima.
Teoria:
- K. E. = qV
- 1/2 mv2 = qV
- v = (2qV/m)1/2
Il tempo di transito (t) attraverso il tubo di drift è L/v, dove L è la lunghezza del tubo di drift
- t=L / (2V/m/q)1/2
schema di un lineare TOF-MS

Questo schema mostra l’ablazione di ioni da un campione solido con un laser pulsato. Il reflectron è una serie di anelli o griglie che fungono da specchio ionico. Questo specchio compensa la diffusione nelle energie cinetiche degli ioni mentre entrano nella regione di deriva e migliora la risoluzione dello strumento. L’uscita di un rivelatore di ioni viene visualizzata su un oscilloscopio in funzione del tempo per produrre lo spettro di massa.
Trappola ionica
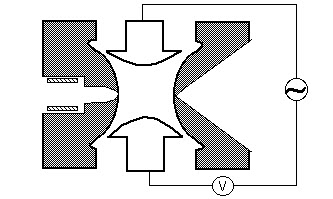
Gli ioni creati dall’impatto elettronico (EI), dall’elettrospray (ESI) o dalla ionizzazione MALDI (matrix-assisted laser desorption) sono focalizzati utilizzando un sistema di lensing elettrostatico nella trappola ionica. Un cancello ionico elettrostatico impulsi aperto (- V) e chiuso (+V) per iniettare ioni nella trappola ionica. Il pulsare del cancello ionico differenzia le trappole ioniche dagli strumenti “a fascio” come i quadrupoli in cui gli ioni entrano continuamente nell’analizzatore di massa. Il tempo durante il quale gli ioni sono ammessi nella trappola, chiamato “durata di ionizzazione”, è impostato per massimizzare il segnale riducendo al minimo gli effetti di carica spaziale. La carica spaziale deriva da troppi ioni nella trappola che causano una distorsione dei campi elettrici che porta a una riduzione complessiva delle prestazioni. La trappola ionica è tipicamente riempito con elio ad una pressione di circa 1 mtorr. Collisioni con elio smorza l’energia cinetica degli ioni e servono a contrarre rapidamente traiettorie verso il centro della trappola ionica, consentendo intrappolamento di ioni iniettati. Gli ioni intrappolati sono ulteriormente focalizzati verso il centro della trappola attraverso l’uso di un potenziale oscillante, chiamato rf fondamentale , applicato all’elettrodo ad anello. Uno ion sarà stabilmente intrappolato a seconda dei valori per la massa e la carica dello ion, la dimensione della trappola ionica (r), la frequenza oscillante della rf fondamentale ( w) e l’ampiezza della tensione sull’elettrodo ad anello ( V). La dipendenza del movimento degli ioni da questi parametri è descritta dal parametro adimensionale qz, qz = 4eV / mr2w2
Quadrupolo
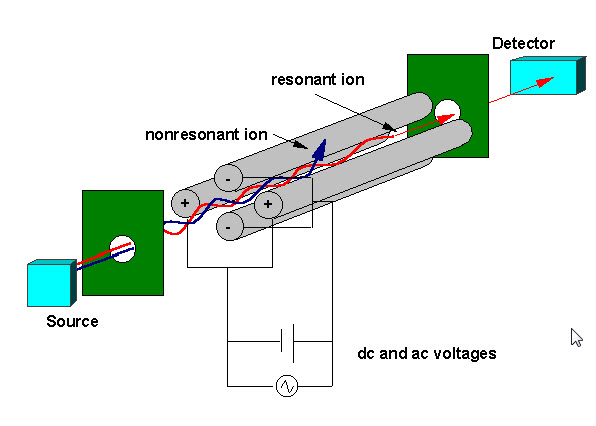
Un filtro di massa quadrupolo è costituito da quattro barre metalliche parallele disposte come nella figura seguente. Due aste opposte hanno un potenziale applicato di (U + Vcos(wt)) e le altre due aste hanno un potenziale di- (U+Vcos (wt)), dove U è una tensione cc e Vcos (wt) è una tensione ca. Le tensioni applicate influenzano la traiettoria degli ioni che viaggiano lungo la traiettoria di volo centrata tra le quattro aste. Per determinate tensioni dc e ac, solo gli ioni di un certo rapporto massa-carica passano attraverso il filtro quadrupolo e tutti gli altri ioni vengono espulsi dal loro percorso originale. Uno spettro di massa si ottiene monitorando gli ioni che passano attraverso il filtro quadrupolo come le tensioni sulle aste sono variate. Esistono due metodi: variando w e tenendo costante U e V, o variando U e V (U/V) fissati per una costante w.
Un filtro di massa a quadrupolo è costituito da quattro barre metalliche parallele disposte come nella figura seguente. Due aste opposte ha
Spettrometria di massa tandem:
La spettrometria di massa tandem, solitamente indicata come MS/MS, comporta l’uso di 2 o più analizzatori di massa. Viene spesso utilizzato per analizzare i singoli componenti in una miscela. Questa tecnica aggiunge specificità a una determinata analisi. Sebbene la spettrometria di massa tandem possa essere riferita a MS/ MS, MS / MS / MS, ecc…, in questa presentazione ho intenzione di descrivere solo MS/MS.
L’idea di base di MS / MS è una selezione di un m / z di un dato ion formato nella sorgente ionica, e sottoporre questo ion alla frammentazione, di solito per collisione con gas inerte(ad es. Argon). Gli ioni del prodotto vengono quindi rilevati. Questo è un modo potente per confermare l’identità di alcuni composti e determinare la struttura di specie sconosciute. Quindi MS / MS è un processo che coinvolge 3 passaggi: ionizzazione,selezione di massa,analisi di massa.
MS / MS potrebbe essere eseguito su strumenti come triplo quadrupolo (QQQ), trappola ionica, tempo di volo, trasformata di Fourier, ecc… Il triplo quadrupolo è lo spettrometro di massa più frequentemente utilizzato per MS / MS, forse a causa del costo e della facilità d’uso tra gli altri fattori.
Metodi di separazione per l’accoppiamento con le specifiche di massa
- GC-MS: Le miscele del campione direttamente sono vaporizzate ed entrano nelle colonne fuse legate della silice. I componenti della miscela sono separati in base alla loro differenza di affinità con la fase legata. I composti separati escono dalla colonna e entrano nel sistema di vuoto dello spettrometro di massa. Le molecole del campione sono ionizzate (EI, o CI) ed accelerate in un analizzatore di massa precalibrato (per esempio Q, trappola dello Ion, TOF, FTMS ecc…). I tempi di conservazione, le masse molecolari ed i modelli di frammentazione sono registrati. Una delle considerazioni più importanti di GC / MS è che i campioni devono essere non termolabili, ovvero termicamente stabili.
- LC-MS: Per i composti che sono termicamente instabili, il metodo di LC/MS è considerato. La separazione è basata sulla diffrence nell’affinità dei campioni con la fase stazionaria e la fase mobile. ad esempio idrofobicità in caso di cromatografia RP.
- CZE-MS: Questo metodo si basa sulle diffrenze della mobilità elettroforetica dei campioni quando la colonna di silice fusa è sotto una differenza di potenziale tra il lato di iniezione e il lato del rivelatore.
- CIEF-MS: Questa è una variante di CZE. Si basa sulle diffrerenze nei punti isoelettrici degli analiti.