acest tutorial discută aspectele de bază ale spectrometriei de masă care vă vor fi de ajutor în a decide tehnicile și măsurătorile adecvate pentru probele dvs. de cercetare.
- ce este spectrometria de masă?
- spectrometrul de masă
- metode de ionizare
- ionizare cu Impact electronic
- ionizare chimică
- desorbție laser asistată de matrice
- ionizare chimică sub presiune atmosferică
- ionizare cu Electrospray
- analiza ionilor
- spectrometrie de masă Tandem
- metode de separare pentru cuplarea cu Spec de masă
ce este spectrometria de masă?
spectrometria de masă este o tehnică analitică care implică studiul în faza gazoasă a moleculelor ionizate cu scopul uneia sau mai multor dintre următoarele:
- determinarea greutății moleculare
- caracterizare structurală
- studiu de reactivitate în fază gazoasă
- analiza calitativă și cantitativă a componentelor dintr-un amestec.
spectrometria de masă constă în principal din cântărirea ionilor în faza gazoasă. Instrumentul utilizat ar putea fi considerat un echilibru sofisticat care determină cu mare precizie masele atomilor și moleculelor individuale. În funcție de proprietățile chimice și fizice ale probelor, pot fi utilizate diferite tehnici de ionizare. Unul dintre factorii principali în alegerea tehnicii de ionizare care trebuie utilizată este termolabilitatea. Pentru probele care nu sunt themolabile și relativ volatile, ionizarea, cum ar fi impactul electronilor și/sau ionizarea chimică, poate fi utilizată în mod eficient. Pentru probele care sunt termolabile, cum ar fi peptidele, proteinele și alte probe de interes biologic, trebuie luate în considerare tehnicile de ionizare moale. Printre cele mai utilizate tehnici de ionizare moale se numără Electrospray (ESI) și desorbția laser asistată de matrice (MALDI). Numele dat unei anumite tehnici de Spec de masă indică de obicei metoda de ionizare utilizată.
masele atomice și moleculare sunt atribuite în raport cu masa izotopului de carbon, 12C, a cărui greutate atomică este definită exact ca 12. Masa reală a lui 12C este de 12 daltoni, cu un dalton egal cu 1.661 10-24 g. masa unei molecule sau a unui ion poate fi prezentată în daltoni (Da) sau kilodaltoni (kDa).
spectrometrul de masă
spectrometria de masă utilizează un instrument numit spectrometru de masă. Principalele componente ale unui spectrometru de masă sunt:
- sistem de admisie (LC, GC, sondă directă etc…)
- sursă Ionică (EI, CI, ESI, APCI, MALDI etc…)
- Analizor de masă (Quadrupol, TOF, capcană Ionică, Sector Magnetic)
- Detector (multiplicator de electroni, Plăci micro canale MCP)
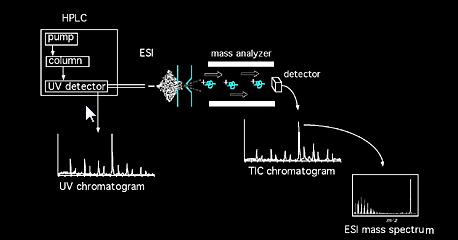
Probele pot fi introduse în spectrometrul de masă direct prin intermediul sondei solide sau, în cazul amestecurilor, prin intermediul unui dispozitiv de cromatografie (de exemplu, cromatografie în fază gazoasă, cromatografie lichidă, electroforeză capilară etc…). Odată ajuns în sursă, moleculele de probă sunt supuse ionizării. Ionii formați în sursă (ioni moleculari și fragmentați) dobândesc o anumită energie cinetică și părăsesc sursa. Un analizor calibrat analizează apoi ionii care trec în funcție de raporturile lor de masă la Încărcare. Pot fi utilizate diferite tipuri de analizor(e), Magnetic, Quadrulpole, capcană Ionică, transformare Fourier, timp de zbor etc…Fasciculul de ioni care iese din ansamblul analizorului este apoi detectat și semnalul este înregistrat. Acronimele metodei comune de ionizare includ:
- EI = impactul electronilor;
- CI = ionizare chimică;
- SIMS = Spec. de masă a ionilor secundari;
- FAB=bombardament rapid cu atomi;
- LDMS = spec. De Masă de desorbție Laser;
- PDMS=Spec. De Masă de desorbție plasmatică;
- TS=Termospray;
- AS=Aerospray;
- ESMS=Spec.de masă Electrospray.
acronimele comune ale analizorului de masă includ:
- EB = electrostatic-Magnetic;
- IT=capcană Ionică;
- Q=Patrupol;
- TOF=timpul zborului.
metode de ionizare
selectarea metodei de ionizare corespunzătoare pentru analiza eșantionului dvs. este extrem de importantă. Deși vă putem oferi sugestii, este responsabilitatea dvs. să înțelegeți și să selectați metoda(metodele) potrivită (e) pentru compușii dvs. de cercetare.
- Electron impact EI ionizare
- ionizare chimică CI
- ionizare chimică ionizare negativă
- tehnici de ionizare Electrospray
- matrice asistată Lazer desorbție (nu este oferit în facilitatea noastră, dar disponibil elswhere în campus)
- Presiunea atmosferică ionizare chimică APCI
ionizare cu Impact electronic
M + E-(70ev) —–> m+. + 2e –
EI metoda de ionizare este potrivit pentru compuși non termolabile. Este necesară volatilitatea eșantionului. Moleculele de probă în stare de vapori sunt bombardate de electroni în mișcare rapidă, convențional 70 EV energie. Aceasta duce la formarea ionilor. Un electron din cea mai mare energie orbitală este dislocat și, ca o consecință, se formează ioni moleculari. Unii dintre acești ioni moleculari se descompun și se formează ioni fragmentați. Fragmentarea unui ion dat se datorează excesului de energie pe care îl necesită în cadrul ionizării. Ionii de fragmente pot fi electroni impari sau chiar electroni. Ionii moleculari formați în ionizarea cu impact electronic sunt ioni electronici impari. Ionii impari de fragmente de electroni sunt formați prin clivaj direct (de ex. scindarea directă a unei legături C-C). Chiar și ionii de fragmente de electroni sunt adesea formați prin rearanjare (de exemplu, transfer de protoni). Eșantionul poate fi introdus la sursa EI printr-un dispozitiv de cromatografie în fază gazoasă, de exemplu în cazul amestecurilor, sau direct printr-un dispozitiv de sondare a solidelor. Cantitățile necesare pentru un experiment sunt de obicei mai mici decât un microgram de material.
spectrele de masă EI, în majoritatea cazurilor, conțin vârfuri de ioni de fragment intens și vârf de ioni moleculari mult mai puțin intens. Când vârful ionilor moleculari nu este observat în spectrul de masă, ionizarea chimică poate fi utilizată pentru a obține informații despre ionii moleculari. O regulă utilă pentru a determina dacă un ion este un ion molecular este regula azotului.
regula azotului: așa cum s-a indicat mai sus, ionii moleculari formați în ionizarea EI sunt ioni electronici impari. Dacă raportul lor masă / încărcare observat este impar, molecula investigată conține un număr impar de atomi de azot. Dacă raportul masă / încărcare este un număr par, molecula respectivă nu conține atomi de azot sau chiar atomi de azot.
ionizarea chimică
pentru chimiștii organici, ionizarea chimică (CI) este o tehnică utilă în special atunci când nu se observă ioni moleculari în spectrul de masă EI și, de asemenea, în cazul confirmării raportului masă / încărcare a ionului molecular. Tehnica de ionizare chimică folosește practic același dispozitiv de sursă de ioni ca în impactul electronilor, cu excepția faptului că CI folosește o sursă de ioni strânsă și gaz de reactiv. Gazul reactiv (de exemplu, amoniacul) este supus mai întâi impactului cu electroni. Ionii de probă sunt formați prin interacțiunea ionilor de gaz reactiv și a moleculelor de probă. Acest fenomen se numește reacții Ion-moleculă. Moleculele de gaz reactiv sunt prezente în raport de aproximativ 100:1 în raport cu moleculele de probă. Ionii pozitivi și ionii negativi se formează în procesul CI. În funcție de configurarea instrumentului (tensiuni sursă, detector etc…) se înregistrează numai ioni pozitivi sau numai ioni negativi.
în CI, reacțiile moleculelor de ioni apar între moleculele de gaz de reactiv ionizat (G) și moleculele neutre de analit Volatil (M) pentru a produce ioni de analit. Ionul Pseudo-molecular MH+ (modul ion pozitiv) sau – (modul ion negativ) sunt adesea observate. Spre deosebire de ionii moleculari obținuți prin metoda EI, detectarea MH+ și – are loc în randament ridicat și se observă mai puțini ioni de fragment.
mod ioni pozitivi:
GH + + M – – – – – – > MH + + G
mod ioni negativi:
– + M ——> – + G
aceste reacții simple de transfer de protoni sunt adevărate procese acido-bazice în fază gazoasă în sensul Bronsted-Lowrey. O sursă de ioni „strânsă” (presiune=0,1-2 torr) este utilizată pentru a maximiza coliziunile, ceea ce duce la creșterea sensibilității. Pentru a avea loc aceste reacții moleculare de ioni trebuie să fie exoterme. Transferul de protoni este unul dintre procesele simple observate în CI pozitiv:
RH+ + M —–> MH+ + R
unul dintre parametrul decisiv în această reacție este afinitatea protonului. Pentru ca reacția să apară, afinitatea protonului moleculei M trebuie să fie mai mare decât cea a moleculei de gaz. Principalele gaze reactive utilizate în CI sunt: amoniacul, metanul și Izobutanul. Ionii reactanți predominanți formați sunt prezentați în mecanismele prezentate mai jos. Alegerea gazului reactiv afectează gradul de fragmentare a ionului cvasi-molecular.
Metan (ionizare chimică cu ioni pozitivi):
- CH4 + e —–> CH4+. + 2e ——> CH3+ + H.
- CH4+. + CH4 —–> CH5+ +CH3.
- CH4+. + CH4 —–> C2H5+ + H2 + H.
Isobutane (positive ion chemical ionization):
- i-C4H10 + e —–> i-C4H10+. + 2e
- i-C4H10+. + i-C4H10 ——> i-C4H9+ + C4H9 +H2
Ammonia (positive ion chemical ionization):
- NH3 + e —–> NH3+. + 2e
- NH3+. + NH3 ——> NH4+ + NH2.
- NH4+ + NH3 ———>N2H7+
în ionizarea chimică în modul ion pozitiv cu metan, vârfurile relevante ale eșantionului observate sunt MH+, + și+; dar în principal MH+. Aceasta corespunde maselor M + 1, m+29 și M+41.
în ionizarea chimică în modul izobutan pozitiv, vârful principal observat este MH+.
în ionizarea chimică în modul ioni pozitivi de amoniac, principalele vârfuri observate sunt MH+ și +. Dacă este prezent mai mult de un sit de protonare, aductele NH3 suplimentare ar putea fi văzute corespunzând +. Aceasta corespunde maselor M + 1, M+18 și M+35.
în unele cazuri, s-ar putea observa dimeri protonați sau alți aducți; pierderea H2O urmată de protonare sau formarea ionilor de aduct este observată pentru unele clase de compuși. Dacă spectrul pe care îl observați nu pare să arate ionii de aduct adecvați sau prezintă o fragmentare extinsă, aveți grijă când încercați să interpretați rezultatele. Există o abundență de date disponibile în literatura de specialitate care discută mecanismele de ionizare chimică aplicabile claselor specifice de compuși.
doi factori determină alegerea gazului reactiv care trebuie utilizat:
- afinitate protonică PA
- transfer de energie
NH3 (amoniacul) este cel mai utilizat gaz reactiv în CI din cauza transferului redus de energie al NH4+ comparativ cu CH5+ de exemplu. Cu NH3 ca gaz reactiv, se observă de obicei MH+ și MNH4+ (17 unități de masă diferență).
ionizare chimică cu ioni negativi
trei mecanisme pot fi subliniate:
- reacția de captare a electronilor datorită atingerii electronilor „termalizați” cu mișcare lentă, cu energie redusă, care pot fi transferați mai eficient în eșantionarea moleculelor.
- transferul de electroni din gazul reactiv ionizat (de exemplu, NH2 – poate transfera un electron într-o moleculă care are o afinitate electronică mai mare decât NH2).
- ionii de gaz reactivi participă la reacții CI adevărate (de exemplu, abstractizarea protonilor, în funcție de aciditățile relative).
ionii moleculari observați în spectrele de masă de ionizare chimică cu ioni negativi sunt de obicei M – or -.
metoda de ionizare Electrospray
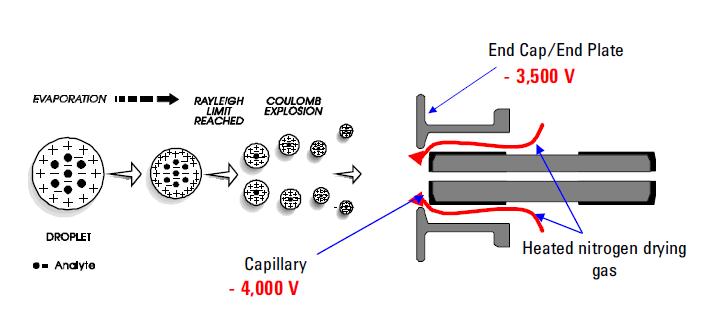
printre cele mai utilizate tehnici de ionizare prin pulverizare se numără ionizarea Electrospray (ESI). Această tehnică continuă să fie metoda de alegere pentru analiza substanțelor chimice termolabile. Capacitățile sale sunt bine documentate. Utilizează o tensiune electrică între ieșirea sondei ESI (de exemplu, capilar) și contraelectrodul, care este situat la câțiva milimetri de sondă. Procesul are ca rezultat generarea de picături foarte încărcate direct din soluția perfuzată. Moleculele de analit înmulțite și/sau încărcate individual se desorbesc din picăturile pulverizate și se prelevează prin restul spectrometrului de masă. ESI s-a remarcat pentru capacitatea sa de a produce ioni moleculari încărcați multiplu dintr-o mare varietate de polimeri, cum ar fi fragmente de proteine și ADN; permite, de asemenea, detectarea sensibilă a speciilor polare cu greutate moleculară mică încărcate individual, cum ar fi medicamentele și metaboliții medicamentelor. Formarea ionilor pozitivi sau negativi (în funcție de semnul câmpului electric aplicat) are loc cu randament ridicat. În modul ionic pozitiv molecule de analit de aducție protonată și/sau alcalină observate în general în spectrele de masă. În modul de funcționare cu ioni negativi se observă vârfuri corespunzătoare moleculelor de analit deprotonat. ESI este descris ca o tehnică de ionizare foarte „moale” în care gazul de baie din jur are un efect moderator asupra energiilor interne și translaționale ale ionilor desorbiți.
avantajele ESI:
- proces de ionizare moale astfel încât ionii moleculari intacte sunt observate
- ESI permite producerea de ioni multipli încărcate. Acest lucru are ca rezultat capacitatea de a analiza specii cu greutate moleculară foarte mare folosind cei mai disponibili analizatori de masă (de exemplu, quadrupoli).
- ESI este un proces de presiune atmosferică. Acest lucru îl face ușor de utilizat și ușor de interfață cu tehnicile de separare HPLC și CE.
Matrix Assisted laser desorbție (MALDI)
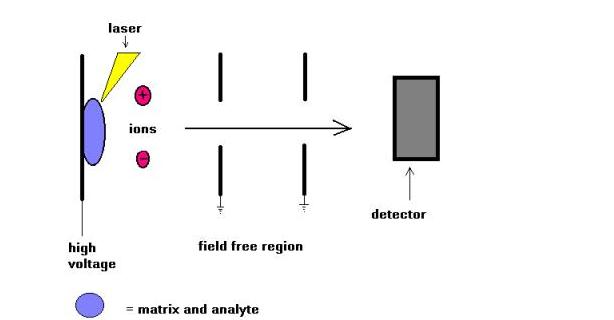
tehnica de spectrometrie de masă asistată de matrice cu laser (MALDI) a fost introdusă de Karas și Hillkamp în 1988 pentru ionizarea peptidelor și proteinelor. Curând după ce această tehnică a fost capabilă să analizeze alte tipuri de biomolecule, cum ar fi oligozaharidele, glicolipidele, nucleotidele și polimerii sintetici. În această tehnică, probele sunt cocristalizate cu o substanță absorbantă UV numită matrice. De exemplu, pentru proteine, matricea de alegere este adesea acidul sinapinic. O radiație de 337 nm de la laserul cu azot este cel mai frecvent utilizată. Laserul ajută la introducerea energiei în sistemul molecular, astfel încât să prevină descompunerea termică.
MALDI este adesea folosit cu spectrometre de masă în timpul zborurilor ( TOF ) datorită naturii pulsante a tehnicii și capacității de gamă de masă. Greutăți moleculare de până la câteva sute de Daltoni ar putea fi măsurate. În ultimii ani s-a încercat Compararea tehnicilor de ionizare MALDI și ESI. În opinia mea, aceste două tehnici nu sunt competitive, ci complementare. Pentru a numi doar câteva, pentru speciile cu greutate moleculară mare, MALDI duce la formarea de ioni moleculari încărcați individual, în timp ce ESI permite formarea de ioni moleculari încărcați multiplu.
considerații practice:
- eșantionul/matricea raportului molar final este de aproximativ sau în jur de 1/5000.
- concentrația finală a probei este de la 1 la 10 pmol/ul
- experiența noastră cu MALDI indică un interval dinamic de 100 fmol/ul la câteva sute pmol/ul
- MALDI este o tehnică de ionizare relativ robustă care tolerează utilizarea sărurilor și a agenților tensioactivi și a tampoanelor. Deși este mai bine să le eliminați pentru o performanță mai bună.
standarde de Peptide și proteine pentru MALDI:
- angiotensină II (umană) MW: 1046,2
- substanță P (umană) MW: 1347,7
- insulină (bovină) MW: 5733,6
- citocrom c (ecvină) MW: 12360.1
- Rnaza a (bovină) MW: 13,682.2
- Apo-mioglobină (ecvină) MW: 16,951.5
- tripsinogen (bovine) MW: 23,980.9
ionizarea chimică a presiunii atmosferice
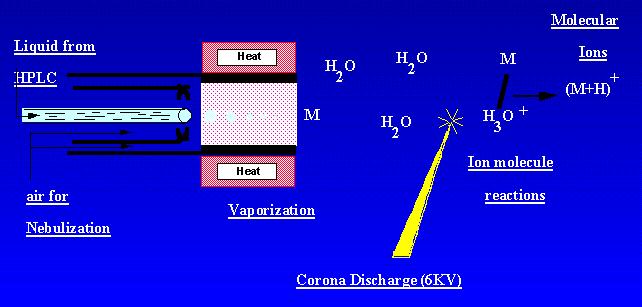
APCI este o tehnică care creează ioni la presiunea atmosferică. O soluție de probă curge printr-un tub încălzit unde este volatilizată într-o ceață și pulverizată într-o descărcare corona cu ajutorul nebulizării cu azot. Probele moleculare sunt ionizate prin reacții ale moleculelor de ioni din ionii de descărcare a coroanei ambiante. Ionii sunt produși în descărcare și extrași în spectrometrul de masă. APCI este cel mai potrivit pentru probele relativ polare, semi-volatile. Un spectru de masă APCI conținea de obicei ionul cvasi-molecular, – sau +.
analiza ionilor
este posibil să se utilizeze mai mulți parametri fizici diferiți pentru a realiza separarea în masă. Tipurile comune de analizoare de masă sunt discutate mai jos. Fiecare are avantaje și dezavantaje. În instalația noastră avem în prezent spectrometre de masă Quadrupole, Ion Trap, amd Time-of-Flight (TOF).
Spectrometru de masă cu Sector Magnetic
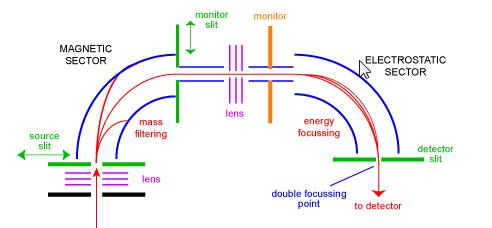
spectrometrul de masă Sectorial a fost unul dintre cele mai comune tipuri de analizor de masă și probabil cel mai familiar omului de știință de zi cu zi. În anii 1950, primele spectrometre de masă comerciale au fost instrumente sectoriale. Ele constau dintr-o combinație a unui dispozitiv electromagnetic mare și a unui fel de dispozitiv de focalizare electrostatică. Producătorii diferiți folosesc geometrii diferite. Figura 1 prezintă o schemă a unui instrument standard de focalizare dublă cu geometrie BE. Configurația BE se mai numește spectrometru de masă din sectorul geometriei inverse-adică un instrument cu sector dublu format dintr-un sector magnetic urmat de un sector electrostatic.
ionii intră în instrument de la sursă (stânga jos) unde sunt inițial focalizați. Acestea intră în sectorul magnetic prin fanta sursă unde sunt deviate conform regulii din stânga. Ionii cu masă mai mare sunt deviați mai puțin decât ionii cu masă mai mică. Scanarea magnetului permite focalizarea ionilor de mase diferite pe fanta monitorului. În acest stadiu, ionii au fost separați numai de masele lor. Pentru a obține un spectru de rezoluție bună în care toți ionii cu același m/z apar coincident ca un vârf în spectru, ionii trebuie filtrați de energiile lor cinetice. După o altă etapă de focalizare, ionii intră în sectorul electrostatic unde ionii de același m / z au distribuțiile lor de energie corectate și sunt focalizați la punctul de focalizare dublu pe fanta detectorului.
instrumentele sectoriale au avut succese comerciale uriașe în anii 1950 și 1960, deoarece au fost singura modalitate practică de a obține date de înaltă rezoluție. În ultimii 20 de ani, odată cu scăderea prețurilor FTM-urilor și dezvoltarea de alternative de înaltă rezoluție (de exemplu Q-Tof), instrumentele sectoriale sunt în declin.
spectrometrie de masă în timpul zborului (TOF-MS)
un spectrometru de masă în timpul zborului utilizează diferențele de timp de tranzit printr-o regiune de derivă pentru a separa ionii de mase diferite. Funcționează într-un mod pulsat, astfel încât ionii trebuie produși sau extrași în impulsuri. Un câmp electric accelerează toți ionii într-o regiune de derivă fără câmp cu o energie cinetică de qV, unde q este sarcina Ionică și V este tensiunea aplicată. Deoarece energia cinetică a ionilor este de 0, 5mv2, ionii mai ușori au o viteză mai mare decât ionii mai grei și ajung la detector la sfârșitul regiunii de drift mai devreme.
Teorie:
- K. E. = qV
- 1/2 mv2 = qV
- v = (2QV / m)1/2
timpul de tranzit (t) prin tubul de drift este L / v unde L este lungimea tubului de drift
- t=L / (2V / m / q)1/2
schema unui TOF-MS liniar

această schemă arată ablația ionilor dintr-o probă solidă cu un laser pulsat. Reflectonul este o serie de inele sau grile care acționează ca o oglindă Ionică. Această oglindă compensează răspândirea energiilor cinetice ale ionilor pe măsură ce intră în regiunea de drift și îmbunătățește rezoluția instrumentului. Ieșirea unui detector de ioni este afișată pe un osciloscop în funcție de timp pentru a produce spectrul de masă.
capcana Ionica
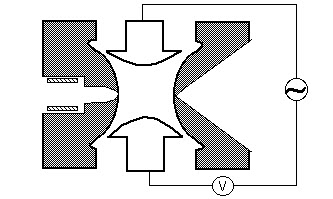
ionii creați prin Electron impact (EI), electrospray (ESI) sau ionizarea cu laser asistată de matrice (MALDI) sunt focalizați folosind un sistem de lentilă electrostatică în capcana Ionică. O poartă Ionică electrostatică pulsează deschis (- V) și închis (+V) pentru a injecta ioni în capcana Ionică. Pulsarea porții ionice diferențiază capcanele ionice de instrumentele” cu fascicul”, cum ar fi patrupolii, unde ionii intră continuu în analizorul de masă. Timpul în care ionii sunt permiși în capcană, denumit „durata ionizării”, este setat pentru a maximiza semnalul, minimizând în același timp efectele de încărcare spațială. Sarcina spațială rezultă din prea mulți ioni din capcană care provoacă o distorsiune a câmpurilor electrice care duce la o reducere generală a performanței. Capcana ionică este de obicei umplută cu heliu la o presiune de aproximativ 1 mtorr. Coliziunile cu heliul amortizează energia cinetică a ionilor și servesc la contractarea rapidă a traiectoriilor spre centrul capcanei ionice, permițând prinderea ionilor injectați. Ionii prinși sunt concentrați în continuare spre centrul capcanei prin utilizarea unui potențial oscilant, numit rf fundamental , aplicat electrodului inelar. Un ion va fi prins stabil în funcție de valorile pentru masa și sarcina ionului, dimensiunea capcanei de ioni (r), frecvența oscilantă a RF fundamental ( w) și amplitudinea tensiunii pe electrodul inelar ( V). Dependența mișcării ionice de acești parametri este descrisă de parametrul adimensional qz, qz = 4EV/mr2w2
Quadrupol
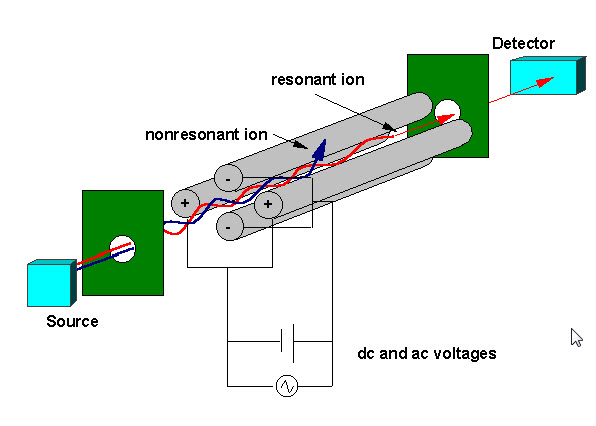
un filtru de masă cvadrupol este format din patru tije metalice paralele dispuse ca în figura de mai jos. Două tije opuse au un potențial aplicat de(U+Vcos(wt)), iar celelalte două tije au un potențial de- (U+Vcos (wt)), unde U este o tensiune dc și Vcos (wt) este o tensiune ac. Tensiunile aplicate afectează traiectoria ionilor care călătoresc pe calea de zbor centrată între cele patru tije. Pentru tensiunile dc și ac date, numai ionii cu un anumit raport masă-încărcare trec prin filtrul quadrupol și toți ceilalți ioni sunt aruncați din calea lor inițială. Un spectru de masă este obținut prin monitorizarea ionilor care trec prin filtrul quadrupol, deoarece tensiunile de pe tije sunt variate. Există două metode: variația w și menținerea Constantei U și V sau variația U și V (U/V) fixată pentru o constantă w.
un filtru de masă cvadrupol este format din patru tije metalice paralele dispuse ca în figura de mai jos. Două tije opuse ha
spectrometrie de masă Tandem:
spectrometria de masă Tandem, denumită de obicei MS/MS, implică utilizarea a 2 sau mai multe analizoare de masă. Este adesea folosit pentru a analiza componentele individuale dintr-un amestec. Această tehnică adaugă specificitate unei analize date. Deși spectrometria de masă tandem poate fi menționată la MS/ MS, MS/MS/MS etc…, în această prezentare voi descrie doar MS/MS.
ideea de bază a MS/MS este o selecție a unui m/z al unui ion dat format în sursa de ioni și supun acest ion fragmentării, de obicei prin coliziune cu gaz inert (de ex. Argon). Ionii produsului sunt apoi detectați. Acesta este un mod puternic de a confirma identitatea anumitor compuși și de a determina structura speciilor necunoscute. Deci MS / MS este un proces care implică 3 pași: ionizare,selecție de masă,analiză de masă.
MS/MS ar putea fi efectuate pe instrumente cum ar fi triple quadrupole (QQQ), capcana Ionică, timpul de zbor, transformata fourier etc… Triplul quadrupol este cel mai frecvent utilizat spectrometru de masă pentru MS/MS, poate din cauza costului și ușurinței de utilizare, printre alți factori.
metode de separare pentru cuplarea cu Spec de masă
- GC-MS: Amestecurile de probe sunt vaporizate direct și intră în coloane de silice topite lipite. Componentele amestecului sunt separate pe baza diferenței lor de afinitate cu faza legată. Compușii separați ies din coloană și intră în sistemul de vid al spectrometrului de masă. Moleculele de probă sunt ionizate (EI sau CI) și accelerate într-un analizor de masă precalibrat (de exemplu, Q, capcana Ionică, TOF, FTMS etc…). Timpii de retenție, masele moleculare și modelele de fragmentare sunt înregistrate. Una dintre cele mai importante considerații ale GC/MS este că eșantionul(eșantioanele) trebuie să fie non termolabil, adică stabil termic.
- LC-MS: pentru compușii care sunt instabili termic, se ia în considerare metoda LC/MS. Separarea se bazează pe difrența în afinitate a probelor cu faza staționară și faza mobilă. de exemplu, hidrofobicitatea în cazul cromatografiei RP.
- cze-MS: această metodă se bazează pe diferențele de mobilitate electroforetică a probelor atunci când coloana de silice topită se află sub o diferență de potențial între partea de injecție și partea detectorului.
- CIEF-MS: aceasta este o variantă a CZE. Se bazează pe difrerențe în punctele izoelectrice ale analiților.