Johdanto
glyoksylaattisykli ohittaa Krebs-syklin dekarboksylointivaiheet ja aiheuttaa nestemäisen hiilen assimilaation asetyyli-CoA: sta. Isositraattilyaasi (EC 4.1.3.1) ja malaattisyntaasi (EC 2.3.3.9) ovat ainoat tämän metaboliareitin entsyymit. Glyoksylaattikierto esiintyy siementen itämisessä (Eastmond & Graham, 2001), eräissä selkärangattomissa, kuten C. elegansissa (Edwards, Copes, Brito, Canfield, & Bradshaw, 2013) ja mikro-organismeissa, kuten E. coli (Nelson & Cox, 2009) ja S. cerevisiae (Rezaei, Aslankoohi, Verstrepen, & Courtin, 2015). Reitti kuvattiin vuonna 1957 tutkimuksissa, joissa tutkittiin mikro-organismeja, jotka kasvoivat asetaatilla ja etanolilla hiililähteenä (Kornberg & Krebs, 1957).
asetyyli-CoA sitoutuu glyoksylaattikierroksessa oksaloasetaattiin, jolloin muodostuu sitraattia ja isositraattia. Jälkimmäinen tuottaa glyoksylaattia ja sukkinaattia isositraattilyaasin katalysoimassa reaktiossa. Lisäksi glyoksylaatti tiivistyy toisen asetyyli-CoA-molekyylin kanssa malaattisyntaasin katalysoimassa reaktiossa, kun tuotettu malaatti on hapetettu oksaloasetaatiksi ja siten regeneroitu Välituote (vaiheet B-1-B-5, kuva 1). Glyoksylaattisyklin jokaisessa toistossa syntyy kaksi asetyyli-CoA-molekyyliä ja yhden sukkinaattimolekyylin nestesynteesi tapahtuu (Beeckmans, 2009; Berg, Stryer, & Tymoczko, 2015; Torres & Marzzoco, 2007).
edelleen öljykasvien varalipideistä valmistetut hiilihydraatit jaetaan kasviin ja hyödynnetään hiililähteenä, kunnes kloroplastit alkavat erilaistua folioleissa ja aloittaa yhteyttämisen. Rasvat ja öljyt ovat tärkeitä kemiallisia rakenteita monien siementen hiilivarastossa, joskin pelkistetyssä muodossa, ja ne koostuvat tärkeistä agronomisista lajeista, kuten soijasta, maapähkinästä, puuvillasta ja auringonkukasta (Junqueira, 2012). Lauriini – (12:0), myristic – (14:0), palmitic – (16:0) ja stearic – (18: 0) – hapot ovat kasvisten tärkeimmät tyydyttyneet rasvahapot; tyydyttymättömiä happoja ovat öljyhappo (18:1(Δ9)), linolihappo (18:2(Δ9, 12)) ja linoleenihappo (18: 3 (Δ9, 12, 15)) (Taiz & Zeiger, 2002).

Kuva 1.
rasvahapot tai asetaattikataboliat tuottavat energiaa glyoksylaattisyklin läpi, mikä osoittaa yhdistymistä oksidaation(vaiheet A-1-A-4), glyoksylaattisyklin (vaiheet B-1-B-5), Krebs-syklin (vaiheet C-1-c-8), glukoneogeneesin (vaiheet D-1-D-3) ja glykolyysin (vaihe E-1) välillä.
rasvahapot, joissa on parimäärä hiiltä, eivät johda hiilihydraattisynteesiin eläimillä (Nelson & Cox, 2009). Tämä johtuu siitä, että glukoneogeneesiä tukevaa oksaloasetaattia ei synny nettotuotantona, koska tässä tapauksessa rasvahapot kataboloituvat asetyyli-CoA: ksi. Välituote hapettuu Krebs-syklissä, ja jokaista asetyyli-CoA: na tulevaa kahta hiiltä kohti häviää kaksi hiiltä CO2: na (Eastmond & Graham, 2001; Nelson & Cox, 2009).
glyoksylaattisyklin puuttuminen nisäkkäiltä voi olla selektiivisen toksisuuden kohde mikrobilääkkeiden kehityksessä. 3-nitropropionamidien estävä vaikutus isositraattilyaasiin M. tuberculosis (Sriram et al., 2011), bromifenolit (Oh et al., 2010) ja sienieläimistä peräisin olevat alkaloidit Isositraattilyaasissa C. albicansissa (Lee et al., 2008; Oh et al., 2010) on analysoitu.
kirjallisuudessa ei ole tietoa energeettisistä näkökohdista, joihin liittyy lipidikataboliaa glyoksylaattisyklin kautta. Tässä yhteydessä tässä tutkimuksessa tutkittiin glyoksylaattisyklissä tuotetun energiamäärän suhdetta rasvahappoketjun kokoon ja verrattiin tätä lähestymistapaa käyttävien solujen energiatehokkuutta eläinsoluihin, joilta puuttui glyoksylaattisykli.
Materialand-menetelmät
suoritettiin vaiheista koostuva energiatase energian tuotannon ja kulutuksen kanssa, jotta saatiin yhtälö, joka liittyy suoraan sellaisen rasvahapon ketjukokoon, jonka hiililuku on kerrannainen 4, ja sen hajoamisesta syntyneeseen energiaan. Syntyneessä yhtälössä ei otettu huomioon asyyli-CoA: n rasvahappojen aktivoitumiseen liittyviä energiakustannuksia. Se on β-hapettumista edeltävä vaihe ja siihen liittyy kahden korkeaenergisen fosfaattisidoksen katkeaminen.
ehdotettu yhtälö validoitiin vertaamalla sen avulla saatua ATP: n määrää ATP: n määrään, joka saadaan lisäämällä ATP: n määrä oksidatiivisella fosforylaatiolla ja substraattitason fosforylaatiolla rasvahappojen hajoamiseen glyoksylaattisykliin osallistuvien metaboliareittien jokaisessa vaiheessa. Rasvahappojen hajoamiseen liittyy glyoksysomien β-oksidaatio, glyoksylaattisykli, Krebs-sykli, osa glukoneogeneesiä ja glykolyysiä, pyruvaatin dekarboksylaatio ja uudelleen Krebs-sykli (Kuva 1).
rasvahappojen hajoamista glyoksylaattisyklin mukana verrattiin rasvahappojen kataboliaan eläinsoluissa. Vertailussa käytettiin aiemmin validoituja yhtälöitä ja laskettiin eläinten β-oksidaatiossa syntyvä energiamäärä (Gonçalves, Valduga, & Pereira, 2012) yhdistettynä nykytutkimuksessa kehitettyihin yhtälöihin. Glyoksylaattisyklin energiatehokkuuskerroin (E%) määriteltiin rasvahappokataboliassa tuotetun ATP: n suhteella glyoksylaattisyklin ja eläinten katabolian huomioon ottaen. Parametri piirrettiin rasvahappojen hiiliatomien lukumäärää vasten. Lisäksi CH2-ykseyden tuottama ATP-nopeus esitettiin rasvahappoketjun hiilien määrän funktiona. GrapPad Prism 6.0 tuotti matemaattiset mallit, jotka edustivat suhdetta muuttujien joukossa.
tulokset ja keskustelu
mitokondrion matriisi on tärkein paikka, jossa rasvahappojen hapettuminen tapahtuu eläinsoluissa. Näiden biomolekyylien kataboliaa esiintyy kuitenkin pääasiassa lehtien peroksisomeissa ja glyoksisomeissa kasvien siementen itämisen aikana (Buchanan, Gruissem, Vickers, & Jones, 2015). Rasvahappojen hajoamiseen glyoksysomeissa sisältyvät taulukossa 1 esitetyt metaboliareitit.
energiantuotannon rinnalla rasvahappojen muuttamisella hiilihydraateiksi on muita tehtäviä, kuten rakenteellisten polysakkaridien ja nukleotidien tuottaminen pentoosifosfaattireitin kautta (Nelson & Cox, 2009). Mitä energianlisäykseen tulee, lyhyempi ja energeettisemmin taloudellinen tapa, joka luultavasti on evoluution valitsema, sisältää glukoneogeneesin fosfoenolipyruvaattiin asti (vaihe d-3 kuvassa 1), joka hajoaa glykolyyttisellä reitillä.
rasvahappojen glyoksisomaalisessa hajoamisessa
ATP: n määrä (x), joka johtuu rasvahappojen glyoksisomaalisesta hajoamisesta, jonka hiililuku on kerrannainen 4,jota seuraa glukoneogeneesi fosfoenolipyruvaattiin ja sen kataboliaan energian tuottamiseksi, voidaan laskea β-oksidaatiossa (ATP β-OX), glyoksylaattisyklissä (ATP C glyox), Krebs-sykli (ATP C Krebs), glukoneogeneesi (ATP oxal-pep) ja glykolyysi /Krebs-sykli uudelleen (ATP pep-CO2) yhtälön (1) mukaisesti:

jokainen glyoksysomien ja peroksisomien β-oksidaatiota aiheuttava hiilen ja hiilen sidoksen katkeaminen tuottaa yhden NADH: n, joka oksidatiivisessa fosforylaatiossa tuottaa 2,5 ATPs: ää (vaihe A-3 kuvassa 1). Peroksisomeissa β-oksidaation ensimmäisessä vaiheessa irronnut elektronienergia haihtuu lämpönä (kuvassa 1 oleva stepA-1).

siksi fadh2-hapetuksesta ei ole nettoenergiaa (Buchanan et al., 2015). Koska α-hiili esteröityy koentsyymi A: n kanssa, β-oksidaatio tapahtuu 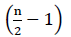 kertaa, missä n on rasvahappoketjun hiililuku. Glyoksylaattisykleen β-oksidaation tuottama ATPs-määrä saadaan yhtälöllä (2):
kertaa, missä n on rasvahappoketjun hiililuku. Glyoksylaattisykleen β-oksidaation tuottama ATPs-määrä saadaan yhtälöllä (2):

jokaista kahta glyoksylaattikiertoon siirrettyä asetyyli-CoA: ta kohti syntyy nettotuotantona yksi sukkinatemolekyyli, joka vastaa puolta asetyyli-CoA: n määrästä, joten syntyy n/4sukkinaattimolekyylejä. Krebs-syklissä sukkinaatti hapetetaan oksaloasetaatiksi, jolloin syntyy 1 FADH2 ja 1 NADH, joka tuottaa 4 ATP: tä oksidatiivifosforylaatiossa (vaiheet C-6 ja C-8, Kuva 1). Tämä arvo kerrottuna n / 4sukkinaattimolekyyleillä ilmaistaan yhtälöllä (3), joka kuvaa Krebs-syklissä ensimmäisenä tuotettua Atpamountia:

oksalasetaatti-inglyoksylaattisyklin regeneroinnissa käytetään malaatin hapettumista, jolloin saadaan 1 NADH, joka tuottaa 2,5 ATPs: ää oksidatiivisessa fosforylaatiossa (Vaihe B-5 kuvassa 1). Näin ollen glyoksylaattisyklissä tuotetun energian (ATP) määrä voidaan ilmaista yhtälöllä(4):

Krebsyklissä tuotettu ylimääräinen oksaloasetaatti voidaan ohjata glukoneogeneesiin. Energian tuottamiseksi glukoneogeneesi tapahtuu fosfoenolipyruvaatin muodostumisessa, jossa käytetään 1 GTP (vaihe 3 kuvassa 1), joka ilmaistaan yhtälöllä (5). Glukoneogeneesin jatkuminen heksoosista johdettujen metaboliittien muodostumiselle on tärkeä prosessi siementen inkerminoinnissa (Buchanan et al., 2015; Eastmond & Graham, 2001; Quettier& Eastmond, 2009):

Fosfoenolipyruvaattikatabolismi sisältää substraattitason fosforylaation, joka tuottaa pyruvaatin (vaihe E-1,kuva 1), pyruvaatin (vaihe F-1) oksidatiivisen dekarboksylaation 1 Nadh-valmistuksella ja asetyyli-CoA: n hapettumisen CO2: ksi. Asetyyli-CoA-hapettumisessa 3 NADH: n, 1 FADH2: n ja 1 GTP: n tuotanto vastaa 10: tä korkeaenergistä fosfaattibondia. Tämä lisäarvo substraattitasolle fosforylaatio ja NADH: n kanssa assosioitunut oksidatiivinen fosforylaatio tuottivat pyruvaatin dekarboksylaation, yhteensä 13,5 ATP: tä (yhtälö 6).

yhtälöiden korvaaminen(2), (3), (4),(5) ja (6) yhtälössä (1) saadaan yhtälö (7). Yksinkertaistettuna yhtälöllä (8) saadaan aikaan suora suhde tuotetun energian määrän (x) ja rasvahappoketjun koon (n) välillä.

yhtälön (8) validointi glyoksylaattisyklissä
tapahtuvan rasvahappojegradoinnin tuottaman energian (ATP) laskemiseksi siten,että yhtälö (8) voidaan validoida, sen soveltamisesta saatua ATP: n määrää verrattiin ATP: n määrään, joka on laskettu yksittäin asetyyli-CoA: n, NAHD: n ja fadh2: n molekulaaristen määrien ja substraattitason fosforylaation summasta, joka syntyy hapetushapoissa, joissa on tietty määrä glyoksysomien hiiliatomeja (Taulukko) 2). Molemmissa olosuhteissa saadut ATP-määrät vastaavat toisiaan. Kun nämä vastaavat tulokset otetaan huomioon, nykyisessä tutkimuksessa kehitetty yhtälö määritti lipidikataboliassa tuotetun energiamäärän ottaen huomioon metaboliareittien integroinnin, joka käsittää yli kaksikymmentä vaihetta.

lisäksi energeettiset tasapainotusyhtälöt, joita seuraa niiden validointi, voivat olla tärkeä väline analysoitaessa eri aineenvaihduntareittejä. Biokemiassa esimerkiksi stoikiometrisiä suhteita metaboliareiteillä voidaan lähestyä nykytutkimuksen tulosten avulla.

Vertailu rasvahappojen glyoksylaattisyklin aiheuttaman hajoamisen tehokkuuden ja eläimellisen atabolian välillä
aiempien tutkimusten mukaan eläinsolujen energiamäärä, joka syntyy ATP: ssä rasvahappojen hajoamisesta hiiliparin numerolla, voi olla algebrallisesti verrannollinen rasvasidin ketjun kokoon. Tämä suhde ilmaistaan yhtälöllä (9) (Gonçalves et al., 2012), jota voidaan verrata nykyisessä tutkimuksessa kehitettyyn yhtälöön (8). Näitä kahta yhtälöä voidaan käyttää vertaamaan energiatehokkuutta β-oksidaation välillä eläinsoluissa ja eliösoluissa, joissa tapahtuu glyoksylaattikierto.

jakamalla yhtälö(8) yhtälöllä (9) ja kertomalla luvulla 100 saadaan rasvahappohajoamisen prosentuaalinen hyötysuhde (E%) energian tuottamiseksi suhteessa eläinten kataboliaan, kuten yhtälöllä (10) ilmaistaan.

vertaamalla e%: a rasvahappoketjun pituuteen (kuva 2) varmistetaan, että hyötysuhde heikkenee hiilivetyketjun kasvaessa. Lisäksi rasvahappojen hapettumisenergia soluissa glyoksylaattikierron avulla saavuttaa alle 90 prosenttia siitä energiatasosta, joka syntyisi vastaavalla tavalla eläinsolussa.
ATP: n tuottonopeus hapettunutta hiiliatomia kohti (ATP/n) riippuu myös rasvahappojen pituusketjusta, maksiminopeudella, joka on lähellä kuutta ATP/n: ää (kuva 3-a), kun taas eläinsoluissa tämä nopeus on suurempi (kuva 3-b).

kuva 2.
Vertailu rasvahappojen hajoamisen energeticefficiency in animal β-oxidation and β-oxidation in eliöt withglyoksylate cycle enzymes, koska rasvahappojen pituusketju.
päinvastoin kuin eläimillä, kasvikset ja eräät mikro-organismit pystyvät muuttamaan rasvahappojen oksidaatiosta syntyvän asetyyli-CoA: n sokereiksi. Eliöissä yhdistyvät glyoksylaattikierto ja glukoneogenesisreaktiot, jotka lokeroituvat glyoksysomien / peroksisomien,mitokondrioiden ja sytosolin välille. Tämä ominaisuus antaa suuremman metabolisen monipuolisuuden, jolloin bakteerit voivat käyttää asetaattia energianlähteenä ja kasvit varastoida siemeniin energianlähteenä käytettäväksi itämisen aikana.

kuva 3.
ATP-määrä, joka syntyy hiiliatomin (ATP / n) vaikutuksesta happaman rasvan hiiliatomien (n) vaikutuksesta glyoksylaattikiertoon (a) ja elottomaan kataboliaan (b). ATP / n: n määrä kasvaa merkittävästi, kunnes N = 20, vastedes määrä kasvaa vähemmän merkittävällä tavalla.
johtopäätös
rasvahappojen hajoamiseen glyoksylaattisyklin avulla energian tuottamiseksi liittyy β-oksidaatio, jonka erityispiirteitä ovat glyoksysomit, glyoksylaattisykli, Krebs-sykli, glukoneogeneesi ja glykolyysi. Näistä vaiheista ja aineenvaihduntareiteistä huolimatta rasvahappojen ketjun pituuden ja sen hajoamisessa syntyvän energiamäärän välinen stoikiometrinen suhde voidaan määrittää algebrallisesti.
näihin metaboliareitteihin osallistuvan stoikiometrian ja eläinsoluissa esiintyvän β-oksidaation stoikiometrisen energeettisen stoikiometrian vertailu osoittaa energiatehokkuuden heikkenevän verrattuna eläinten aineenvaihduntaan. Krebs-kierron dekarboksylaatioreaktioiden ohitus antaa eliöille evolutiivisia adaptaatioita, mutta se määrittää myös pienemmän energiamäärän, joka syntyy hiiliatomia kohti verrattuna rasvahappojen hajoamiseen eläimissä.