Bevezetés
a glioxilát-ciklus megkerüli a Krebs-ciklus dekarboxilezési lépéseit, és az acetil-CoA-ból származó folyékony szén asszimilációját okozza. Az izocitrát-liáz (EC 4.1.3.1.) és a malát-szintáz (EC 2.3.3.9.) az egyetlen enzim ebben a metabolikus útvonalban. A glioxilát ciklus a mag csírázásában (Eastmond & Graham, 2001), néhány gerinctelen állatban, például C. elegansban (Edwards, Copes, Brito, Canfield, & Bradshaw, 2013) és mikroorganizmusokban, például E. coli (Nelson & Cox, 2009) és S. cerevisiae (Rezaei, Aslankoohi, Verstrepen, & Courtin, 2015). Az utat 1957-ben írták le olyan mikroorganizmusokon végzett vizsgálatok során, amelyek acetáton és etanolon növekedtek szénforrásként (Kornberg & Krebs, 1957).
az acetil-CoA a glioxilát ciklusban oxaloacetáttal kötődik, citrátot és izocitrátot termel. Ez utóbbi az izocitrát-liáz által katalizált reakcióban glioxilátot és szukcinátot termel. Továbbá a glioxilát egy második acetil-CoA molekulával kondenzálódik egy malát-szintáz által katalizált reakcióban, miután az előállított malátot oxaloacetáttá oxidáljuk, és így regeneráljuk a köztiterméket (B-1-B-5 lépések, 1.ábra). A glioxilátciklus minden ismétlésekor két acetil-CoA molekulát vezetünk be, és egy szukcinátmolekula folyadékszintézise következik be (Beeckmans, 2009; Berg, Stryer, & Tymoczko, 2015; Torres & Marzzoco, 2007).
továbbá az olajos magvak tartalék lipidjeiből előállított szénhidrátokat elosztják a növényben, és szénforrásként hasznosítják, amíg a kloroplasztok elkezdenek differenciálódni a foliolákban és fotoszintézist nem kezdenek. A zsírok és olajok fontos kémiai struktúrák számos mag széntárolásában, bár csökkentett formában, olyan fontos agronómiai fajokból, mint a szójabab, a földimogyoró, a gyapot és a napraforgó (Junqueira, 2012). Laurinsav (12:0), mirisztinsav (14:0), palmitinsav (16:0) és sztearinsav (18:0) a zöldségekben a legfontosabb telített zsírsavak; míg a telítetlen savak az olajsav (18:1 (69)), a linolsav(18:2) (9,12)) és a linolénsav(18,3) (9,12,15)) (Taiz & Zeiger, 2002).

1.ábra.
a zsírsavak vagy az acetát katabolizmusa energiát termel a glioxilát-cikluson keresztül, ami bizonyítja az oxidáció(a-1-A-4 lépés), a glioxilát-ciklus (B-1-B-5 lépés), a Krebs-ciklus (C-1-C-8 lépés), a glükoneogenezis (D-1-D-3 lépés) és a glikolízis (E-1 lépés) integrációját.
a pár szénatomos zsírsavak nem eredményeznek szénhidrátszintézist állatokban (Nelson & Cox, 2009). Ez a tény azért fordul elő, mert nincs nettó oxaloacetát termelés a glükoneogenezis támogatására, mivel ebben az esetben a zsírsavak acetil-CoA-vá katabolizálódnak. Az intermedier a Krebs-ciklusban oxidálódik, és minden acetil-CoA-ként belépő két szénatomra két szén CO2-ként veszít (Eastmond & Graham, 2001; Nelson & Cox, 2009).
emlősökben a glioxilát-ciklus hiánya szelektív toxicitás célpontja lehet az antimikrobiális szerek kifejlesztésében. A 3-nitropropionamidok izocitrát-liázra gyakorolt gátló hatása M. tuberculosisban (Sriram et al., 2011), brómfenolok (Oh et al., 2010) és a szivacsok alkaloidjai izocitrát-liázon C. albicans-ban (Lee et al., 2008; Oh et al. 2010) elemezték.
a szakirodalomban nincsenek adatok a lipid katabolizmust érintő energetikai szempontokról a glioxilát cikluson keresztül. Ebben az összefüggésben a jelen kutatás a glioxilát-ciklusban előállított energia mennyisége és a zsírsav-lánc mérete közötti összefüggést vizsgálta, és összehasonlította az ezt a megközelítést alkalmazó sejtek energiahatékonyságát a glioxilát-ciklus nélküli állati sejtekkel.
anyagés módszerek
az energiatermeléssel és az energiafogyasztással kapcsolatos lépések energiamérlegét olyan egyenlet elérése érdekében hajtottuk végre, amely közvetlenül kapcsolódik a 4-es szénatomszámú zsírsav láncméretéhez a lebomlása által termelt energiával. A generált egyenletben az acil-CoA zsírsav aktiválásával járó energiaköltséget nem számoltuk el. Ez egy lépés az oxidáció előtt, és két nagy energiájú foszfátkötés megszakítását jelenti.
a javasolt egyenletet úgy validáltuk, hogy összehasonlítottuk az alkalmazásával kapott ATP-mennyiséget az oxidatív foszforiláció és a szubsztrát szintű foszforiláció során keletkező ATP-mennyiség hozzáadásával kapott ATP-arányokkal a zsírsav-lebomlásban részt vevő metabolikus utak minden egyes lépésében, beleértve a glioxilát-ciklust. A zsírsav lebomlása magában foglalja a glyoxysomes, a glioxilát ciklus, a Krebs-ciklus, a glükoneogenezis és a glikolízis egy részét, a piruvát dekarboxilezést és a Krebs-ciklust (1.ábra).
a zsírsavak glioxilátciklussal járó lebomlásának energiahatékonyságát hasonlították össze a zsírsavak állati sejtekben történő katabolizmusával. Ebben az összehasonlításban a korábban validált egyenleteket használtuk, és kiszámítottuk az állatoknál előforduló 6-as oxidáció során keletkező energia mennyiségét (gon 6valves, Valduga, & Pereira, 2012), a jelenlegi kutatásban kifejlesztett egyenletekkel párosítva. A glioxilát-ciklus energiahatékonysági tényezőjét (E%) a zsírsav-katabolizmusban termelt ATP aránya határozta meg, figyelembe véve a glioxilát-ciklust és az állati katabolizmust. A paramétert a zsírsav szénatomjainak számához viszonyítva ábrázoltuk. Ezenkívül a CH2 egység által termelt ATP sebességet a zsírsavlánc szénatomszámának függvényében ábrázoltuk. A GrapPad Prism 6.0 generálta azokat a matematikai modelleket, amelyek a változók közötti kapcsolatot ábrázolták.
Eredményekés megbeszélés
a mitokondriális mátrix a fő hely, ahol a zsírsavak oxidációja az állati sejtekben történik. Ezeknek a biomolekuláknak a katabolizmusa azonban elsősorban a lombszövetek peroxiszómáiban és a glioxiszómákban fordul elő a növények magcsírázása során (Buchanan, Gruissem, Vickers, & Jones, 2015). A zsírsavak glioxiszómákban történő lebomlása magában foglalja az 1.táblázatban bemutatott metabolikus útvonalakat.
az energiatermeléssel párhuzamosan a zsírsavak szénhidrátokká történő átalakításának más funkciói is vannak, például szerkezeti poliszacharidok és nukleotidok előállítása a pentóz-foszfát útvonalon keresztül (Nelson & Cox, 2009). Ami az energianyereséget illeti, a rövidebb és energetikailag gazdaságosabb módszer, amelyet valószínűleg az evolúció választott ki, magában foglalja a glükoneogenezist a foszfoenolpiruvátig (D-3 lépés az 1.ábrán), amelyet a glikolitikus út bomlik le.
a zsírsavak glioxiszomális lebomlása során keletkező energia (ATP) mennyisége
a 4-es szénatomszámú zsírsavak glioxiszomális lebomlásából származó ATP mennyiség (x), amelyet a glükoneogenezis követ a foszfoenolpiruvátig és annak katabolizmusáig, az energiatermelés céljából,kiszámítható az előállított és felhasznált ATP sebességek összegével a (ATP)-oxidáció (ATP), glioxilát ciklus (ATP C) során glyox), Krebs ciklus (ATP C Krebs), glükoneogenezis (ATP oxal-Pep)és ismét glikolízis /Krebs ciklus (ATP Pep-CO2), az (1) egyenlet szerint:

a glioxiszómákban és a peroxiszómákban az oxidáció során a szén-szén kötés minden egyes megszakadása egy NADH-t eredményez, amely inoxidatív foszforilációval 2,5 ATPs-t eredményez (A-3 lépés az 1.ábrán). A peroxiszómákban az első lépés során eltávolított elektron energia nak,-nek 6-oxidáció hő formájában disszipálódik (stepA-1 Az 1.ábrán).

ezért nincs nettó energia a FADH-ból2 oxidáció (Buchanan et al., 2015). Mivel a szén-dioxidot a koenzim A-val észterezzük, az a-oxidáció 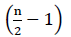 – szer fordul elő, ahol n A zsírsavlánc szénszáma. Az atps által termelt mennyiség a glyoxylate cikluson belüli oxidáció által egyenletből adódik(2):
– szer fordul elő, ahol n A zsírsavlánc szénszáma. Az atps által termelt mennyiség a glyoxylate cikluson belüli oxidáció által egyenletből adódik(2):

minden két acetil-CoA molekuláraa glioxilát ciklusra irányítva egy szukcinatemolekula nettó termelése van, amely megfelel az acetil-CoA mennyiségének felének, így n/4szukcinát molekulák keletkeznek. A Krebs-ciklusban a szukcinát oxaloacetáttá oxidálódik, 1 FADH2-t és 1 NADH-t termel, amely oxidatív foszforilezéssel 4 ATP-t termel (C-6 és C-8 lépések, 1.ábra). Ezt az értéket szorozva n/4szukcinátmolekulákkal a (3) egyenlet fejezi ki, amely a Krebs-ciklusban először előállított ATP-mennyiséget képviseli:

az oxalacetát inglioxilát ciklus regenerálása magában foglalja a malát oxidációját, amely 1 NADH-t eredményez, amely 2,5 ATP-t hoz létre oxidatív foszforiláció során (B-5.lépés az 1.ábrán). Következésképpen a glioxilát-ciklusban előállított energia mennyisége (ATP) egyenlettel fejezhető ki(4):

a Krebscycle-ben termelt oxaloacetát felesleg glükoneogenezisre irányulhat. Annak érdekében, hogy energiát termeljen, aa glukoneogenezis a foszfoenolpiruvát képződésben fordul elő, 1 GTP-vel (3.lépés az 1. ábrán), az (5) egyenletben kifejezve. A glükoneogenezis folytatásaa hexózból származó metabolitok képződéséhez fontos folyamatmagok csírázása (Buchanan et al., 2015; Eastmond & Graham, 2001; Quettier& Eastmond, 2009):

a Foszfoenolpiruvát-katabolizmus szubsztrátszintű foszforilezést jelent,amely piruvátot (E-1.lépés, 1. ábra), a piruvát oxidatív dekarboxilezését (F-1. lépés) 1 NADH-termeléssel, valamint acetil-CoA oxidációt eredményez CO2-vé. Az acetil-CoA oxidációban 3 NADH, 1 FADH2 és 1 GTP termelése 10 nagy energiájú foszfátkötésnek felel meg. Ez az érték hozzáadódik a szubsztrát szintű foszforilációhoz és az oxidatív foszforilációhoz, amely a piruvát NADH által generált dekarboxilezéséhez kapcsolódik, összesen 13,5 ATP-vel (6.egyenlet).

egyenletek helyettesítése(2), (3), (4),(5) és (6) Az (1) egyenletben a (7) egyenletet kapjuk. Algebrai egyszerűsítés esetén a (8) egyenlet közvetlen arányt állapít meg a termelt energia mennyisége (x) és a zsírsavlánc mérete (n) között.

Validationof egyenlet (8) kiszámításához az energia (ATP) által termelt zsírsavakdegradáció révén glioxilát ciklus
annak érdekében,hogy az egyenlet (8) lehet validálni, az ATP mennyisége, nyert annak alkalmazása, összehasonlítottuk az ATP összeg egyedileg kiszámított összege acetil-CoA, NAHD és FADH2 molekulaszám, és szubsztrát szintű foszforiláció, generált oxidációs ofsatty savak meghatározott számú szénatomok glioxiszómákban (2.táblázat). Mindkét körülmények között a kapott ATP mennyiségek egyenértékűek. Figyelembe véve ezeket az ekvivalens eredményeket, a jelenlegi tanulmányban kidolgozott egyenlet meghatározta a lipid katabolizmusban előállított energia mennyiségét, figyelembe véve a több mint húsz lépést magában foglaló metabolikus utak integrációját.

ezenkívül a generáló egyenletek energetikai egyensúlya, majd validálása fontos eszköz lehet a különböző anyagcsere-útvonalak elemzéséhez. A biokémiában olyan szempontok, mint a sztöchiometrikus kapcsolatok az anyagcsere-útvonalakon, a jelenlegi kutatások eredményeinek felhasználásával közelíthetők meg.

a zsírsavak glioxilátciklussal történő lebomlásának hatékonysága és az állati katabolizmus
a korábbi vizsgálatok szerint az ATP-ben a zsírsavak szénpárszámmal történő lebomlása által termelt állati sejtek energiamennyisége algebrailag összefügghet a zsírsav láncméretével. Ezt az összefüggést a (9) egyenlet fejezi ki (gon 6valves et al., 2012), amely összehasonlítható a jelenlegi tanulmányban kidolgozott (8) egyenlettel. A két egyenlet alkalmazható az állati sejtekben és az organizmusokban végbemenő, a glioxilátciklusban végbemenő oxidáció közötti energiahatékonyság összehasonlítására.

a (8) egyenletet a(9) egyenlettel elosztva és 100-zal megszorozva megkapjuk a zsírsav lebomlásának százalékos hatásfokát (E%) az energiatermeléshez, az állati katabolizmushoz viszonyítva, a (10) egyenletben kifejezve.

az e% – os zsírsav-lánchossz ábrázolása (2.ábra) azt igazolja, hogy a hatékonyság a szénhidrogénlánc növekedésével csökken. Ezenkívül a zsírsavak oxidációjából nyert energia a sejtekben glioxilátciklussal eléri az energiaszint kevesebb mint 90% – át, amelyet egy állati sejtben hasonló módon generálnának.
az oxidált szénatomonként (ATP/n) termelt ATP sebesség szintén függ a zsírsav hosszláncától, legfeljebb hat ATP/n-hez közeli sebességgel (3-A ábra), míg ez az arány magasabb az állati sejtekben (3-b ábra).

2.ábra.
a zsírsav lebomlásának energetikushatékonyságának összehasonlítása az állatokban a CA-oxidáció és a CA-oxidáció között a glioxilát ciklusú enzimekkel rendelkező szervezetekben, a zsírsav hosszlánca miatt.
ellentétben az állatokkal, zöldségekkel és néhány mikroorganizmus képes átalakítani az acetil-CoA-t a zsírsavak oxidációjából cukrokká. Az organizmusok kombinálják a glioxilát ciklust és a glükoneogénreakciókat,amelyek a glioxiszómák / peroxiszómák, a mitokondriumok és a citoszol között vannak felosztva. Ez a funkció nagyobb metabolikus sokoldalúságot biztosít,lehetővé téve a baktériumok számára, hogy az acetátot energiaforrásként használják, a növények pedig a csírázás során felhasznált energiaforrásként tárolják a magvakban lévő lipideket.

3.ábra.
ATP sebesség által termelt szénatom (ATP / n) miatt a sav zsírsav szénatomjai (n) a glioxilát ciklus (a) és az állati katabolizmus (b). Az ATP / n arány jelentősen megnőkörülbelül n = 20, ettől kezdve a sebesség kevésbé jelentős módon növekszik.
következtetés
a zsírsavak lebomlása a glioxilát-ciklus által az energiatermelés céljából magában foglalja az oxidációt, melynek sajátos jellemzői A glioxiszómák, a glioxilát-ciklus, a Krebs-ciklus, a glükoneogenezis és a glikolízis. E lépések és anyagcsere-útvonalak ellenére algebrai értelemben sztöchiometrikus összefüggés állapítható meg a zsírsavak lánchossza és a lebomlása során keletkező energiamennyiség között.
az ezekben a metabolikus útvonalakban részt vevő sztöchiometriai energia és az állati sejtekben előforduló, az oxidáció során bekövetkező sztöchiometriai energia összehasonlítása az energiahatékonyság csökkenését mutatja az állati anyagcseréhez képest. Míg a Krebs-ciklus dekarboxilezési reakcióinak megkerülése evolúciós alkalmazkodást biztosít az organizmusoknak, ha jelen vannak, a szénatomonként keletkező kisebb energiamennyiséget is meghatározza, összehasonlítva a zsírsavak állatokban történő lebomlásával.