ez a bemutató a tömegspektrometria alapvető szempontjait tárgyalja, amelyek hasznosak lesznek a kutatási minták megfelelő technikáinak és méréseinek eldöntésében.
- mi a tömegspektrometria?
- a tömegspektrométer
- ionizációs módszerek
- elektron hatás ionizáció
- kémiai ionizáció
- mátrix segített lézer deszorpció
- légköri nyomás kémiai ionizáció
- elektrospray ionizáció
- ionok elemzése
- Tandem tömegspektrometria
- elválasztási módszerek tömegspektrométerrel való összekapcsoláshoz
mi a tömegspektrometria?
a tömegspektrometria olyan analitikai technika, amely magában foglalja az ionizált molekulák gázfázisában végzett vizsgálatot az alábbiak közül egy vagy több céljával:
- Molekulatömeg meghatározása
- szerkezeti jellemzése
- gázfázisú reaktivitási vizsgálat
- keverékben lévő komponensek minőségi és mennyiségi elemzése.
a tömegspektrometria alapvetően az ionok gázfázisban történő méréséből áll. Az alkalmazott műszer kifinomult egyensúlynak tekinthető, amely nagy pontossággal meghatározza az egyes atomok és molekulák tömegét. A minták kémiai és fizikai tulajdonságaitól függően különböző ionizációs technikák alkalmazhatók. Az egyik fő tényező az alkalmazandó ionizációs technika kiválasztásában a hőkezelhetőség. A nem molabil és viszonylag Illékony minták esetében az ionizáció, például az Elektronhatás és/vagy a kémiai ionizáció hatékonyan alkalmazható. Termolabil minták, például peptidek, fehérjék és egyéb biológiai szempontból érdekes minták esetében lágy ionizációs technikákat kell figyelembe venni. A leggyakrabban használt lágyionizációs technikák közé tartozik az elektrospray (ESI) és a Matrix Assisted Laser deszorpció (MALDI). Egy adott tömegspektrum-technikának adott név általában az alkalmazott ionizációs módszerre utal.
az atom-és molekulatömegeket a 12C szénizotóp tömegéhez viszonyítva határozzuk meg, amelynek atomtömege pontosan 12. A 12C tényleges tömege 12 Dalton, egy dalton egyenlő 1-vel.661 10-24 g. egy molekula vagy ion tömege daltonban (Da) vagy kilodaltonban (kDa) jeleníthető meg.
a tömegspektrométer
tömegspektrometria egy tömegspektrométernek nevezett műszert használ. A tömegspektrométer fő összetevői a következők:
- bemeneti rendszer (LC, GC, közvetlen szonda stb…)
- Ionforrás (EI, CI, ESI, APCI, MALDI stb…)
- Tömegelemző (Kvadrupol, TOF, Ioncsapda, mágneses szektor)
- detektor (elektron szorzó, Mikrocsatornás lemezek MCPs)
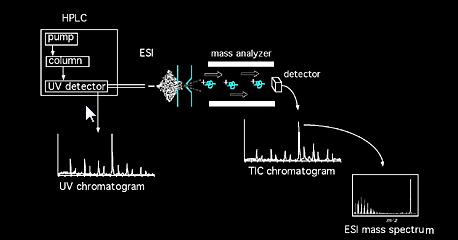
A mintákat a tömegspektrométerbe közvetlenül szilárd szondán keresztül, keverékek esetén kromatográfiás eszköz közvetítésével (pl. gázkromatográfia, folyadékkromatográfia, kapilláris elektroforézis stb…). A forrásba kerülve a mintamolekulákat ionizációnak vetik alá. A forrásban képződő ionok (molekuláris és fragmentum ionok) kinetikus energiát nyernek, és elhagyják a forrást. Ezután egy kalibrált analizátor elemzi az elhaladó ionokat tömegük függvényében a töltési arányokhoz. Különböző típusú analizátorok használhatók, mágneses, Quadrulpole, Ioncsapda, Fourier transzformáció, repülési idő stb…Az analizátor egységből kilépő ionnyalábot ezután detektáljuk, és a jelet regisztráljuk. A közös ionizációs módszer rövidítései a következők:
- EI = elektron hatás;
- CI = kémiai ionizáció;
- SIMS = másodlagos ionok Tömegspektruma;
- FAB = gyors Atombombázás;
- LDMS=lézer deszorpciós Tömegspektruma;
- PDMS=Plazma deszorpciós Tömegspektruma;
- TS=Thermospray;
- AS=Aerospray;
- ESMS=elektrospray tömegspektrométer.
közös mass analyzer rövidítések közé:
- EB = elektrosztatikus-mágneses;
- IT=ioncsapda;
- Q=Kvadrupol;
- TOF=repülési idő.
ionizációs módszerek
a megfelelő ionizációs módszer kiválasztása a minta elemzéséhez rendkívül fontos. Bár javaslatokat tudunk ajánlani, az Ön felelőssége, hogy megértse és kiválassza a kutatási vegyületekhez megfelelő módszert(módszereket).
- elektron hatás ei ionizáció
- kémiai ionizáció Ci
- negatív Ion kémiai ionizáció
- elektrospray ionizációs technikák
- mátrix segített Lazer deszorpció (nem kínált a létesítmény, de elérhető elswhere az egyetemen)
- légköri nyomás kémiai ionizáció APCI
elektron ütközési ionizáció
M + E-(70ev) —–> M+. + 2e –
az EI ionizációs módszer alkalmas nem termolabil vegyületekre. A minta volatilitása szükséges. A gőzállapotú mintamolekulákat gyorsan mozgó elektronok bombázzák, hagyományosan 70 eV energia. Ez ionképződést eredményez. A legmagasabb pályaenergiából egy elektron elmozdul, ennek következtében molekuláris ionok képződnek. Ezen molekuláris ionok egy része lebomlik és fragmentum ionok képződnek. Egy adott ion fragmentációja annak az energiafeleslegnek köszönhető, amelyet az ionizáción belül igényel. A fragmentumionok lehetnek páratlan elektronok vagy akár elektronok is. Az elektronhatású ionizációban képződött molekuláris ionok páratlan elektronionok. A páratlan elektronfragmensionok közvetlen hasítással (pl. C-C kötés közvetlen hasítása). Még az elektronfragmensionok is gyakran átrendeződéssel képződnek (pl. proton transzfer). A minta gázkromatográfiás berendezésen, például keverékek esetében, vagy közvetlenül szilárdanyag-mérő berendezésen keresztül vezethető be az EI-forrásba. A kísérlethez szükséges mennyiségek általában kisebbek, mint egy mikrogramm anyag.
az EI tömegspektrumok a legtöbb esetben intenzív fragmentumion-csúcsokat és sokkal kevésbé intenzív molekuláris ion-csúcsokat tartalmaznak. Ha a molekuláris ioncsúcs nem figyelhető meg a tömegspektrumban, kémiai ionizáció alkalmazható molekuláris ioninformációk megszerzésére. Az egyik hasznos szabály annak meghatározására, hogy egy ion molekuláris ion-e, a nitrogén szabály.
nitrogén szabály: mint fentebb jeleztük, az EI ionizációban képződött molekuláris ionok páratlan elektronionok. Ha a megfigyelt tömeg / töltés arány páratlan, a vizsgált molekula páratlan számú nitrogénatomot tartalmaz. Ha ez a tömeg / töltés arány páros szám, akkor a molekula nem vagy akár nitrogénatomokat is tartalmaz.
kémiai ionizáció
szerves kémikusok számára a kémiai ionizáció (Ci) különösen hasznos technika, ha az EI tömegspektrumában nem figyelhető meg molekuláris ion, valamint a molekuláris ion tömeg / töltés arányának megerősítése esetén is. A kémiai ionizációs technika gyakorlatilag ugyanazt az ionforrás-eszközt használja, mint az elektron-ütközésnél, kivéve, hogy a CI szűk ionforrást és reagensgázt használ. A reagensgázt (például ammóniát) először elektron ütközésnek vetik alá. A mintaionok a reagensgáz-ionok és a mintamolekulák kölcsönhatásából keletkeznek. Ezt a jelenséget ion-molekula reakcióknak nevezik. A reagens gázmolekulák körülbelül 100:1 arányban vannak jelen a mintamolekulákhoz képest. A CI folyamat során pozitív és negatív ionok képződnek. A műszer beállításától függően (forrásfeszültségek, detektor stb…) csak pozitív ionokat vagy csak negatív ionokat rögzítenek.
A CI-ben ionmolekula-reakciók lépnek fel az ionizált reagensgáz-molekulák (G) és az illékony analit-semleges molekulák (M) között az analit-ionok előállításához. Pszeudo-molekuláris ion MH+ (pozitív ion mód) vagy – (negatív ion mód) gyakran megfigyelhető. Az EI módszerrel nyert molekuláris ionoktól eltérően az MH+ és – detektálás nagy hozammal történik, és kevesebb fragmentumion figyelhető meg.
pozitív ion mód:
GH + + M ——> MH + + G
negatív ion mód:
– + M ——> – + G
ezek az egyszerű protonátviteli reakciók valódi gázfázisú sav-bázis folyamatok Bronsted-Lowrey értelemben. “Szoros” ionforrást (nyomás=0,1-2 torr) használnak az ütközések maximalizálására, ami növeli az érzékenységet. Ezeknek az ionmolekuláknak exoterm reakcióknak kell lenniük. A protontranszfer a pozitív CI-ben megfigyelt egyszerű folyamatok egyike:
RH+ + M- – – – – > MH+ + R
ennek a reakciónak az egyik meghatározó paramétere a proton affinitás. A reakció bekövetkezéséhez az M molekula proton affinitásának magasabbnak kell lennie, mint a gázmolekula. A CI-ben használt fő reagensgázok: ammónia, metán és izobután. A képződött domináns reagensionokat az alábbiakban bemutatott mechanizmusok adják meg. A reagensgáz megválasztása befolyásolja a kvázi molekuláris ion fragmentációjának mértékét.
metán (pozitív ion kémiai ionizáció):
- CH4 + e —–> CH4+. + 2e ——> CH3+ + H.
- CH4+. + CH4 —–> CH5+ +CH3.
- CH4+. + CH4 —–> C2H5+ + H2 + H.
Isobutane (positive ion chemical ionization):
- i-C4H10 + e —–> i-C4H10+. + 2e
- i-C4H10+. + i-C4H10 ——> i-C4H9+ + C4H9 +H2
Ammonia (positive ion chemical ionization):
- NH3 + e —–> NH3+. + 2e
- NH3+. + NH3 ——> NH4+ + NH2.
- NH4 + + NH3 ———>N2H7+
metánpozitív ion módú kémiai ionizációban a megfigyelt releváns mintacsúcsok MH+, + és +; de főleg MH+. Ez megfelel az M+1, M+29 és M+41 tömegeknek.
izobután pozitív ion módú kémiai ionizációban a megfigyelt fő csúcs az MH+.
ammónia pozitív ion módú kémiai ionizációban a megfigyelt fő csúcsok MH+ és +. Ha egynél több protonációs hely van jelen, további NH3 adduktok láthatók A + – nak megfelelően. Ez megfelel az M+1, M+18 és M+35 tömegeknek.
egyes esetekben protonált dimerek vagy más adduktok láthatók; a H2O vesztesége, amelyet protonálás vagy adduktionképződés követ a vegyületek egyes osztályaiban. Ha úgy tűnik, hogy a megfigyelt spektrum nem mutatja a megfelelő adduktionokat, vagy kiterjedt fragmentációt mutat, legyen óvatos, amikor megpróbálja értelmezni az eredményeket. A szakirodalomban rengeteg adat áll rendelkezésre, amelyek a vegyületek meghatározott osztályaira alkalmazható kémiai ionizációs mechanizmusokat tárgyalják.
két tényező határozza meg az alkalmazandó reagensgáz kiválasztását:
- Proton affinitás PA
- energiaátadás
NH3 (ammónia) a leggyakrabban használt reagensgáz A CI-ben, mivel az NH4+ alacsony energiaátadása például a CH5+ – hoz hasonlítható. NH3 reagensgáz esetén általában MH+ és MNH4 + (17 tömegegység különbség) figyelhető meg.
negatív Ion kémiai ionizáció
három mechanizmus aláhúzható:
- Elektronfogási reakció a lassan mozgó, alacsony energiájú “termalizált” elektronok elérése miatt, amelyek hatékonyabban átvihetők a mintamolekulákba.
- Elektrontranszfer ionizált reagensgázból (pl. NH2 – elektront vihet át olyan molekulába, amelynek az NH2-nél nagyobb elektron affinitása van).
- Reagensgáz-ionok vesznek részt a valódi ci-reakciókban (pl. proton absztrakció, a relatív savasságok szerint).
a negatív ion kémiai ionizációs tömegspektrumokban megfigyelt molekuláris ionok általában M – vagy -.
elektrospray ionizációs módszer
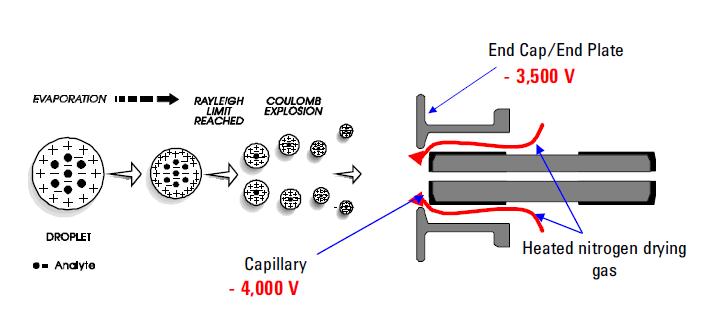
a leggyakrabban használt permetező ionizációs technikák közé tartozik az elektrospray ionizáció (ESI). Ez a technika továbbra is a választott módszer a termolabil vegyi anyagok elemzésére. Képességei jól dokumentáltak. Elektromos feszültséget használ az ESI szonda kilépése (például kapilláris) és az ellenelektróda között, amely néhány milliméterre helyezkedik el a szondától. A folyamat eredményeként erősen töltött cseppek keletkeznek közvetlenül az infúziós oldatból. A permetezett cseppecskékből sokszorosított és/vagy egyszeresen töltött analitmolekulák deszorbeálódnak, és a tömegspektrométer többi részéből mintát vesznek. Az ESI-t megkülönböztették azzal a képességgel, hogy sokféle polimerből, például fehérjéből és DNS-fragmensből képes többszörösen töltött molekuláris ionokat előállítani; lehetővé teszi az egyenként töltött kis molekulatömegű poláris fajok, például gyógyszerek és gyógyszer-metabolitok érzékeny kimutatását is. A pozitív vagy negatív ionok képződése (az alkalmazott elektromos mező jelétől függően) nagy hozammal történik. A pozitív ion mód protonált és / vagy alkáli adduktum analit molekulák általában megfigyelhető a tömegspektrumokban. A negatív ion üzemmódban a deprotonált analit molekuláknak megfelelő működési csúcsok figyelhetők meg. Az ESI-t nagyon “puha” ionizációs technikának nevezik, ahol a környező fürdőgáz mérséklő hatást gyakorol a deszorbált ionok belső és transzlációs energiájára.
az ESI előnyei:
- lágy ionizációs folyamat, így ép molekuláris ionok figyelhetők meg
- az ESI lehetővé teszi a többszörösen töltött ionok előállítását. Ez lehetővé teszi a nagyon nagy molekulatömegű Fajok elemzését a rendelkezésre álló tömeganalizátorok (például kvadrupolok) segítségével.
- az ESI egy légköri nyomású folyamat. Ez megkönnyíti a használatát és a HPLC és CE elválasztási technikákkal való könnyű kapcsolódást.
mátrix segített lézer deszorpció (MALDI)
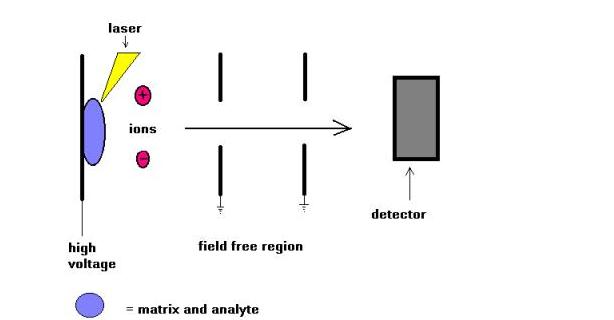
A Matrix Assisted Laser deszorpciós (MALDI) tömegspektrometriás technikát Karas és Hillkamp vezette be 1988-ban a peptidek és fehérjék ionizációjára. Hamarosan ez a technika képes volt elemezni más típusú biomolekulákat, például oligoszacharidokat, glikolipideket, nukleotidokat és szintetikus polimereket. Ebben a technikában a mintákat mátrixnak nevezett UV-abszorbeáló anyaggal kokristályosítjuk. Például a fehérjék esetében a választott mátrix gyakran szinapinsav. A nitrogén lézer 337 nm-es sugárzását használják leggyakrabban. A lézer segíti az energia bejuttatását a molekuláris rendszerbe oly módon, hogy megakadályozza a termikus bomlást.
a MALDI-t gyakran használják repülési idő tömegspektrométerekkel (TOF ) a technika pulzáló jellege és a tömegtartomány képessége miatt. A molekulatömeg akár néhány száz Dalton is mérhető. A MALDI és az ESI ionizációs technikák összehasonlítását az elmúlt években megkísérelték. Véleményem szerint ez a két technika nem versenyképes, hanem kiegészíti egymást. Csak hogy néhányat említsünk, a nagy molekulatömegű fajok esetében a MALDI egy töltésű molekuláris ionok képződéséhez vezet, míg az ESI lehetővé teszi a többszörösen töltött molekuláris ionok képződését.
gyakorlati megfontolások:
- a végső mólarány minta / mátrix körülbelül vagy körülbelül 1/5000.
- a minta végső koncentrációja 1-10 pmol/ul
- a MALDI-val kapcsolatos tapasztalataink 100 fmol/ul és néhány száz pmol/ul
- a MALDI viszonylag robusztus ionizációs technika, amely tolerálja a sók, felületaktív anyagok és pufferek használatát. Bár a jobb teljesítmény érdekében a legjobb eltávolítani őket.
peptid és fehérje standardok MALDI:
- angiotenzin II (humán) MW: 1046,2
- Anyag P (humán) MW: 1347,7
- inzulin (szarvasmarha) MW: 5733,6
- citokróm c (ló) MW: 12 360.1
- RNáz a (szarvasmarha) MW: 13,682.2
- Apo-mioglobin (ló) MW: 16,951.5
- tripszinogén (szarvasmarha) MW: 23,980.9
légköri nyomás kémiai ionizáció
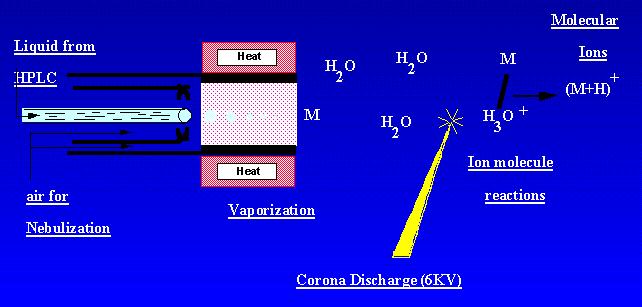
az APCI olyan technika, amely légköri nyomáson ionokat hoz létre. A mintaoldat egy fűtött csövön keresztül áramlik, ahol ködben elpárologtatják, majd nitrogén porlasztás segítségével koronakisülésbe permetezik. A mintamolekulákat az ambiáns koronakisülési ionok ionmolekula-reakciói ionizálják. A kisülés során ionokat állítanak elő és extrahálják a tömegspektrométerbe. Az APCI a legalkalmasabb a viszonylag poláris, félig Illékony mintákhoz. Az APCI tömegspektrum általában a kvázi molekuláris iont tartalmazta, – vagy +.
ionok elemzése
számos különböző fizikai paraméter használható a tömeg szétválasztására. A tömegelemzők általános típusait az alábbiakban tárgyaljuk. Mindegyiknek vannak előnyei és hátrányai. Létesítményünkben jelenleg Quadrupole, Ion Trap, amd Time-of-Flight (Tof) tömegspektrométerek vannak.
mágneses szektor tömegspektrométer
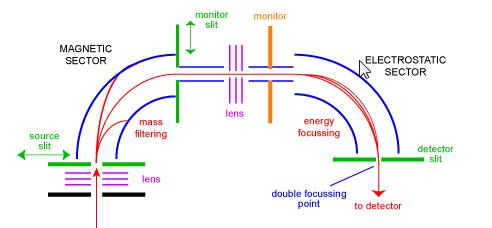
az ágazati tömegspektrométer a tömeganalizátorok egyik leggyakoribb típusa volt, és valószínűleg a legismertebb a mindennapi tudósok számára. Az 1950-es években az első kereskedelmi tömegspektrométerek ágazati eszközök voltak. Ezek egy nagy elektromágneses és valamilyen elektrosztatikus fókuszáló eszköz kombinációjából állnak. A különböző gyártók eltérő geometriákat használnak. Az 1. ábra egy szabványos ‘be’ geometria kettős fókuszáló eszköz vázlatát mutatja. A be konfigurációt fordított geometriai szektor tömegspektrométernek is nevezik – vagyis egy kettős szektorú műszer, amely mágneses szektorból áll, amelyet elektrosztatikus szektor követ.
az ionok a forrásból (bal alsó sarokban) jutnak be a műszerbe, ahol kezdetben fókuszálnak. A mágneses szektorba a forrásrésen keresztül lépnek be, ahol a bal oldali szabály szerint elhajlanak. A nagyobb tömegű ionok kevésbé térnek el, mint az alacsonyabb tömegű ionok. A mágnes letapogatása lehetővé teszi a különböző tömegű ionok fókuszálását a monitor résén. Ebben a szakaszban az ionokat csak tömegük választotta el. Ahhoz, hogy jó felbontású spektrumot kapjunk, ahol az összes azonos m/z Ion egybeesőnek tűnik, mint egy csúcs a spektrumban, az ionokat kinetikus energiájukkal kell szűrni. A fókuszálás egy újabb fázisa után az ionok belépnek az elektrosztatikus szektorba, ahol az azonos m / z-es ionok energiaeloszlását korrigálják, és a detektor résén lévő kettős fókuszpontra fókuszálnak.
az ágazati eszközök hatalmas kereskedelmi sikereket értek el az 1950-es és 1960-as években, mivel ezek voltak az egyetlen gyakorlati módszer a nagy felbontású adatok megszerzésére. Az elmúlt 20 évben az FTM-ek csökkenő áraival és a nagy felbontású alternatívák (például a Q-Tof) fejlődésével az ágazati eszközök hanyatlóban vannak.
repülési idő tömegspektrometria (TOF-MS)
a repülési idő tömegspektrométer a sodródási tartományon keresztüli tranzitidő különbségeit használja a különböző tömegű ionok elválasztására. Impulzusos üzemmódban működik, így az ionokat impulzusokban kell előállítani vagy extrahálni. Az elektromos mező az összes iont egy mező nélküli sodródási régióba gyorsítja, amelynek kinetikus energiája qV, ahol q az ion töltése, V pedig az alkalmazott feszültség. Mivel az ion kinetikus energiája 0,5 MV 2, a könnyebb ionok nagyobb sebességgel rendelkeznek, mint a nehezebb ionok, és hamarabb elérik a detektort a drift régió végén.
Elmélet:
- K. E. = qV
- 1/2 mv2 = qV
- v = (2qV / m)1/2
a sodródó csövön keresztüli tranzitidő (t) L / v, ahol L a sodródó cső hossza
- t=L / (2V / m / q)1/2
lineáris TOF-MS vázlata

ez a vázlatos ábra egy szilárd mintából származó ionok ablációját mutatja pulzáló lézerrel. A reflectron gyűrűk vagy rácsok sorozata, amelyek ion tükörként működnek. Ez a tükör kompenzálja az ionok kinetikus energiáinak terjedését, amikor belépnek a sodródási régióba, és javítja a műszer felbontását. Az ionérzékelő kimenete egy oszcilloszkópon jelenik meg a tömegspektrum előállításához szükséges idő függvényében.
Ioncsapda
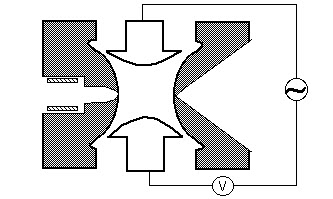
által létrehozott ionok elektron ütés (EI), elektrospray (ESI), vagy mátrix-asszisztált lézer deszorpció (MALDI) ionizáció elektrosztatikus lencserendszerrel fókuszáljuk az ioncsapdába. Az elektrosztatikus ionkapu nyitott (-V) és zárt (+V) impulzusokat ad az ioncsapdába. Az ionkapu pulzálása megkülönbözteti az ioncsapdákat a” sugár ” műszerektől, például a kvadrupoloktól, ahol az ionok folyamatosan belépnek a tömegelemző készülékbe. Az az idő, amely alatt az ionokat beengedik a csapdába, az úgynevezett “ionizációs időtartam”, úgy van beállítva, hogy maximalizálja a jelet, miközben minimalizálja a tér-töltés hatásait. A tér-töltés túl sok ionból származik a csapdában, amelyek az elektromos mezők torzulását okozzák, ami a teljesítmény általános csökkenéséhez vezet. Az ioncsapdát általában héliummal töltik meg körülbelül 1 mtorr nyomásig. A héliummal való ütközések csillapítják az ionok mozgási energiáját, és gyorsan összehúzódnak az ioncsapda közepe felé, lehetővé téve a befecskendezett ionok csapdázását. A csapdába esett ionok tovább koncentrálódnak a csapda közepe felé egy oszcilláló potenciál, az úgynevezett alapvető rf, amelyet a gyűrűelektródára alkalmaznak. Az ion stabilan csapdába esik az ion tömegének és töltésének értékeitől, az ioncsapda méretétől ( r), az alapvető rf oszcillációs frekvenciájától ( w) és a gyűrűelektróda feszültségének amplitúdójától (V) függően. Az ionmozgás ezen paraméterektől való függését a QZ dimenzió nélküli paraméter írja le, qz = 4EV / mr2w2
Kvadrupol
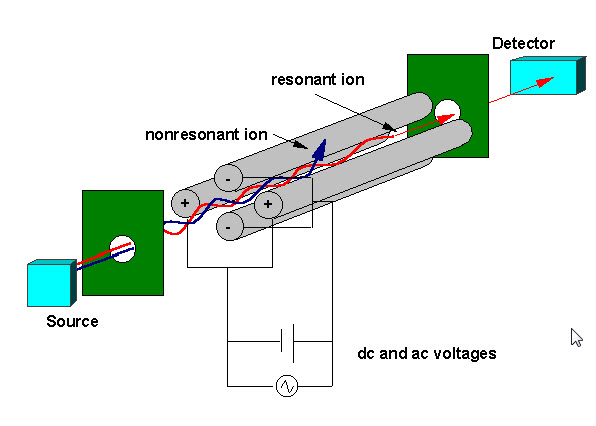
a kvadrupol tömegszűrő négy párhuzamos fémrúdból áll, amelyek az alábbi ábra szerint vannak elrendezve. Két ellentétes rúd Alkalmazott potenciálja (U + Vcos(wt)), a másik két rúd potenciálja- (U+Vcos (wt)), ahol U egyenfeszültség, Vcos (wt) pedig váltakozó feszültség. Az alkalmazott feszültségek befolyásolják a négy rúd középpontja között a repülési útvonalon haladó ionok pályáját. Adott dc és ac feszültség esetén csak egy bizonyos tömeg / töltés arányú ionok haladnak át a kvadrupol szűrőn, és az összes többi iont kidobják eredeti útjukból. Tömegspektrumot kapunk a kvadrupol szűrőn áthaladó ionok megfigyelésével, mivel a rudak feszültsége változatos. Két módszer létezik: változó w és az U és V állandó tartása, vagy változó U és V (U/V) állandó w-re rögzítve.
a kvadrupol tömegszűrő négy párhuzamos fémrúdból áll, amelyek az alábbi ábra szerint vannak elrendezve. Két ellentétes rúd ha
Tandem tömegspektrometria:
Tandem tömegspektrometria, amelyet általában MS/MS-nek neveznek, 2 vagy több tömegelemző használatát foglalja magában. Gyakran használják a keverék egyes összetevőinek elemzésére. Ez a technika specifikusságot ad egy adott elemzéshez. Bár a tandem tömegspektrometria MS / MS, MS / MS / MS stb…, ebben az előadásban csak leírom MS/MS.
az MS/MS alapgondolata egy adott ion m/z-jének kiválasztása, amely az ionforrásban képződik, és ezt az iont fragmentációnak teszi ki, általában inert gázzal való ütközéssel (pl. Argon). Ezután a termékionokat detektálják. Ez egy hatékony módszer bizonyos vegyületek azonosságának megerősítésére és az ismeretlen fajok szerkezetének meghatározására. Tehát az MS / MS egy olyan folyamat,amely 3 lépést foglal magában: ionizáció,tömegválasztás, tömegelemzés.
MS / MS elvégezhető olyan műszereken, mint a hármas kvadrupol (QQQ), az ioncsapda, a repülési idő, a fourier-transzformáció stb… A hármas kvadrupol a leggyakrabban használt tömegspektrométer az MS/MS számára, talán a költségek és a könnyű használat miatt.
elválasztási módszerek a
- GC-MS tömegspektrométerrel történő összekapcsoláshoz: A mintakeverékeket közvetlenül elpárologtatják, és ragasztott olvasztott szilícium-dioxid oszlopokba kerülnek. A keverék komponenseit elválasztjuk a kötött fázissal való affinitáskülönbségük alapján. Az elválasztott vegyületek kilépnek az oszlopból, és belépnek a tömegspektrométer vákuumrendszerébe. A mintamolekulákat ionizálják (EI vagy CI), és egy előre kalibrált tömeganalizátorba gyorsítják (pl. Q, Ioncsapda, TOF, FTMS stb…). A retenciós időket, a molekulatömegeket és a fragmentációs mintákat rögzítik. A GC/MS egyik legfontosabb szempontja, hogy a minta(K) nak nem termolálhatónak kell lennie, vagyis termikusan stabilnak kell lennie.
- LC-MS: a termikusan instabil vegyületek esetében az LC/MS módszert veszik figyelembe. Az elválasztás a minták állófázissal és mozgófázissal való affinitásának diffranciáján alapul. például hidrofóbitás RP kromatográfia esetén.
- CZE-MS: ez a módszer a minták elektroforetikus mobilitásának eltérésein alapul, amikor az olvasztott szilícium-dioxid oszlop a befecskendezési oldal és a detektor oldal közötti potenciálkülönbség alatt van.
- CIEF-MS: ez a CZE egyik változata. Az analitok izoelektromos pontjainak diffrerenciáin alapul.