- introduktion
- materialer og metoder
- Vævspræparat
- Dobbelt-Label Fluorescensimmunhistokemi
- Antistofkarakterisering
- konfokal analyse
- Antistofkontroller
- resultater
- NGF-Immunmærkning
- NGF og Gabaergisk Co-lokalisering
- NGF og Glutamatergisk Co-lokalisering
- Diskussion
- interessekonflikt Erklæring
- anerkendelser
- supplerende materiale
introduktion
neurotrophin nervevækstfaktor (NGF) er involveret i flere kritiske processer i det udviklende og modne pattedyrs nervesystem, herunder målinnervation, celledifferentiering og neuronal overlevelse (Large et al., 1986; Li et al., 1995; Sofie et al., 2001; Lad et al., 2003). I den voksne hjerne spiller NGF en nøglerolle i vedligeholdelsen og funktionen af det basale forhjerne kolinerge system (Lad et al., 2003). Niveauer af NGF er højest i områder, der modtager det største antal basale forhjerne kolinerge fremspring, nemlig hippocampus og bark (Korsching et al., 1985; Shelton og Reichardt, 1986), og receptorer for NGF i hjernebarken er stort set begrænset til basal forhjerne corticopetal fremspring., 1988; Torben et al., 2001; Rossi et al., 2002). Nervevækstfaktorsignalering opretholder kolinerge kortikopetale fremspring i voksen alder (Chen et al., 1997; Debeir et al., 1999) og kan forhindre degeneration af disse neuroner efter transektion af deres aksoner (Hefti, 1986; Tussynski et al., 1990; Torben et al., 1994). Desuden forbedrer NGF frigivelsen af acetylcholin fra basale forhjernekulturer (Auld et al., 2001) og kan modulere kolinerge funktion gennem fænotypisk kontrol af det kolinerge gen locus (Rylett et al., 1993; Hu et al., 1997).
det basale forhjerne-kolinerge system påvirker læring og erfaringsafhængig plasticitet i barken (Bakin og Veinberger, 1996; Kilgard og Mersenich, 1998; Conner et al., 2003, 2005), og NGF-signalering er blevet antaget for at understøtte og muligvis forbedre basal forhjernemedieret læring og plasticitet. For eksempel reducerer blokade af NGF-signalering via gentagne injektioner af NGF-antistoffer i den isolerede bark lokal kolinerge innervering og forstyrrer erhvervelse af to processer, der afhænger af integriteten af kolinerge input, konditioneret smagsaversion og hæmmende undgåelsesindlæring (Gutierres et al., 1997). En nylig undersøgelse foretaget af Conner et al. (2009) viste, at både rumlig læring og hippocampal langvarig potentiering (LTP) forbedres efter infusioner af NGF i septalkernen, den primære kilde til kolinerge innervation til hippocampus.
fokal anvendelse af NGF kan også inducere hurtig udvidelse af den lokale knurhårrepræsentation i tøndebarken hos rotter. Denne proces er afhængig af kolinerge fremspring fra den basale forhjerne (Prakash et al., 1996, 2004), hvilket antyder, at kortikal NGF-signalering kan stimulere hurtig kolinerge-afhængig funktionel omorganisering. Ud over dets langsigtede trofiske virkninger på basale forhjerne kolinerge celler kan NGF således også deltage i kortvarig kredsløbsomdannelse. Denne” dual-action ” hypotese understøttes af eksistensen af konstitutive og aktivitetsafhængige frigivelsesmekanismer for NGF (Blochl og Thoenen, 1995; Lessmann et al., 2003), der potentielt ligger til grund for henholdsvis NGF ‘ s langsigtede trofiske og kortsigtede modulerende virkninger. Desuden er både retrograde (langsigtede) og lokale (kortsigtede) signalveje blevet observeret for NGF (Huang og Reichardt, 2003).
celler, der udtrykker NGF, er blevet påvist i hjernebarken, cerebellum, hippocampus, thalamus, striatum, basal forhjerne og hjernestamme (Gall og Isackson, 1989; Maisonpierre et al., 1990; Isackson et al., 1991; Conner og Varon, 1992; Hayashi et al., 1993; Mufson et al., 1994; Chang et al., 2007). Selvom NGF-mRNA efter sigende er blevet observeret i astrocytter og andre glia, produceres langt størstedelen af kortikal NGF af neuroner., 2001). De specifikke typer neuroner, der producerer NGF i barken, er imidlertid ikke kendt, og kolinerge kortikopetale fremspring har vist sig at innervere både stimulerende og hæmmende neuroner i barken., 1999). I ekstrakortiske regioner såsom hippocampus, striatum og basal forhjerne er NGF-produktion overvejende lokaliseret til GABAergiske hæmmende neuroner (Lauterborn et al., 1993, 1995; Pascual et al., 1998; Pernille et al., 1999). Identifikation af NGF-producerende celler i barken er vigtig for at identificere potentielle mekanismer, der ligger til grund for modulering af kolinerge kortikale input, og mekanismer med kortikal plasticitet. I den aktuelle undersøgelse identificerer vi en delmængde af kortikale GABAergiske celler som den primære kilde til NGF-produktion i voksenbarken med relativt sjælden produktion af glutamatergiske neuroner.
materialer og metoder
alle forsøgspersoner blev behandlet i overensstemmelse med institutionelle retningslinjer for dyrepleje. På grund af lave endogene niveauer af kortikal NGF–ekspression, der forbød identifikation af specifikke celletypekilder til NGF i tidligere undersøgelser, udførte vi lokale colchicin-infusioner for at hæmme mikrotubuli-polymerisering og derved blokere NGF-transport væk fra cellelegemet og resulterede i akkumulering af detekterbart NGF-antigen i Soma af producerende celler (Schubert et al., 1972; Hokfelt et al., 1975; Hanson og Edstr, 1978; Conner og Varon, 1992). Tidligere rapporter har vist, at colchicinbehandling øger påvisning af NGF ved hjælp af immunhistokemiske teknikker (Conner og Varon, 1992). Desuden, colchicin niveauer svarende til det, der blev brugt i den aktuelle undersøgelse, inducerer ikke grove abnormiteter i neuronal fordeling af neurotrophin-familiemedlemmet BDNF (Conner et al., 1997).
Vævspræparat
otte voksne Fischer 344 rotter (4 Han, 4 hun) blev bedøvet med 2 ml/kg af en 25 mg/ml ketamin, 1,3 mg/ml og 0,25 mg/ml cocktail og injiceret med 5.0 kolchicin (10 kolchicin / kolchicin i aCSF) på de kortikale steder, der er anført nedenfor med en hastighed på 0,5 kolchicin/min ved hjælp af en 10 kolchicin Hamilton-sprøjte. Efter infusion forblev nålen på plads i fire minutter for at tillade tilstrækkelig diffusion til det omgivende væv. Fire dyr modtog bilaterale injektioner i den primære motorbark (M1) ved +1,2 mm anterior (A/P) og 2,5 mm lateral (m/L) til bregma. Halvdelen af opløsningen blev injiceret ved 1,6 mm under hjernens overflade (D/V) og resten ved 1,0
Dobbelt-Label Fluorescensimmunhistokemi
sekventiel dobbelt-label immunhistokemi blev brugt til at visualisere neuroner, der udtrykte NGF og enten GABAergiske eller glutamatergiske cellemarkører. Fritflydende sektioner blev vasket i Tris bufferet saltvand (TBS), permeabiliseret med 0,25% Triton 100, og ikke-specifik mærkning blev derefter blokeret med 5% æsel serum. Sektioner blev inkuberet i 72 timer ved 4 liter C i kanin-anti-NGF-antistof (Conner og Varon, 1992) fortyndet 1:1000 i TBS, 0,25% Triton H-100 og 5% æsel serum. Efter primær antistofinkubation blev sektioner inkuberet i æsel anti-kanin biotinkonjugeret IgG (1: 200; Vektorlaboratorier, Burlingame, CA, USA). Tyramid signal amplification (TSA; PerkinElmer, MA, USA) blev anvendt til at forstærke NGF-signalet, hvorefter sektioner blev vasket i TBS og inkuberet i Aleksa Fluor 488 eller 594-konjugeret streptavidin (Invitrogen, Carlsbad, CA, USA) fortyndet 1:200 i 3 timer ved 4 kur C. Efter en kort vask blev sektioner inkuberet i både mus anti-glutamat decarboksylase (GAD) 65 (GAD-6, AntibodyRegistry:AB_528264, 1:2000; udviklingsstudier Hybridoma Bank,IOA City, IA, USA) og mus anti-GAD67 (AnitbodyRegistry: AB_2278725, 1:1500; Millipore, Temecula, CA, USA) eller i mus anti-GAD67 (AnitbodyRegistry: AB_2278725, 1:1500; Millipore, Temecula, CA, USA) eller i mus anti-GAD67 (AnitbodyRegistry: AB_2278725, 1:1500; Millipore, Temecula, CA, USA) eller i mus anti-gad parvalbumin (antibodyregistry: ab_2174013, 1:30000; Millipore, Temecula, CA, USA), mus anti-calbindin-d-28k (Antibodyregistry: Ab_476894, 1: 1500; Sigma-Aldrich, St. Louis, MO, USA) eller mus anti-Ca2+/calmodulin-afhængig proteinkinase IIA (CAMKIIA, antibodyregistry: ab_2067919, 1: 1500; Millipore) i 72 timer ved 4 liter C. endelig blev sektioner vasket, inkuberet i Aleksa Fluor 594 eller 488-konjugeret æsel anti-mus (Invitrogen) i 3 timer ved stuetemperatur, vasket igen, monteret på glasrutschebaner og dækket i Fluoromount-G (Southern Biotech, Birminghan, AL, USA). For at maksimere identifikationen af GABAergiske celler blev gad65 og GAD67 antistoffer Co-inkuberet. En delmængde af sektioner blev dækket i ProLong Gold med DAPI (Invitrogen) til visualisering af cellekerner.
Antistofkarakterisering
NGF-antistoffet anvendt i denne undersøgelse er en affinitetsrenset polyklonal opdrættet i Kanin mod oprenset mus NGF (Conner og Varon, 1992). Antistoffet genkender oprenset mus og rekombinant human NGF, men krydsreagerer ikke med rekombinant BDNF eller NT-3 (Conner og Varon, 1996). Desuden matcher det immunreaktive mønster af NGF-ekspression i rottehjernen tæt det, der opnås ved in situ-analyse i rottehjernen (Conner og Varon, 1997).
det monoklonale antistof GAD-65 (Developmental Studies Hybridoma Bank, Gad-6) blev produceret ved immunisering af mus med GAD-protein immunoaffinitet-oprenset fra rottehjerne. Vestlig blot-analyse af rottehjernehomogenater afslørede, at antistoffet selektivt genkender GAD-65, men ikke GAD-67 (Chang og Gottlieb, 1988). Yderligere undersøgelser har vist, at GAD-6-antistoffet genkender en epitop placeret mellem aminosyrer 475-571 af C-terminalen af GAD-65 (Butler et al., 1993).
GAD – 67 musen monoklonal (Millipore, MAB 5406, lot: 25010139) blev rejst mod aminosyrerester 4-101 af human GAD-67 og genkender et enkelt 67-kDa-bånd på vestlig blot-analyse af rottehjerne (producentens tekniske information). Præinkubering af antistoffet med et GST-GAD-67 fusionsprotein resulterede i intet immunopositivt signal i hjernen (Ito et al., 2007).
musens monoklonale anti-CaMKIIa (Millipore, MAB 8699, lot: LV1366080) genkender specifikt alfa-underenheden af calcium/calmodulinafhængig proteinkinase II. Vestlig blot-analyse viser, at antistoffet identificerer et enkelt bånd på 50 kDa og genkender både phosphorylerede og ikke-phosphorylerede former (Erondu og Kennedy, 1985).
monoklonal anti-calbindin-D-28k (Sigma–Aldrich, C9848, lot: 088k4799) er afledt af BALB/C-mus immuniseret med oprenset bovin nyre calbindin-D-28k. Immunoblotting viste, at antistoffet genkender et 28-kDa-bånd og reagerer ikke med lignende molekyler, såsom calbindin-D-9K, calretinin, myosin-let kæde og parvalbumin (producentens tekniske oplysninger). Preabsorption med et calbindin-D-27 kDa-protein oprenset fra kylling-og rottehjerner viste sig at eliminere calbindin-immunfarvning i hjernen (Pasteels et al., 1987).
Anti-parvalbumin (Millipore, MAB 1572, lot: LV1378387) blev opsamlet fra mus immuniseret mod parvalbumin oprenset fra frømuskel. Det monoklonale antistof er rettet mod en epitop på det første Ca2+-bindingssted, og immunoblotanalyse viser, at det genkender et hjerneprotein på 12 kDa (producentens tekniske information).
konfokal analyse
billeder blev taget ved hjælp af en Olympus ØKSE70 med Magnafire-program (version 2.0; Karl stors billedbehandling, Goleta, CA, USA). 2 mm anterior / posterior til colchicin-injektionssteder, formodentlig på grund af mangel på colchicin-diffusion og det resulterende fravær af somatisk NGF-akkumulering, blev kun sektioner inden for 1,5 mm fra hvert colchicin-injektionssted analyseret. Hver 10. sektion (400 kr.) blev undersøgt inden for en kortikal region. Celler blev manuelt talt, og mindst tre sektioner blev analyseret i hver kortikal region og antistofkombination pr. Kun tre dyr blev evalueret i den tidlige region på grund af ikke-detekterbar NGF-mærkning i den fjerde. Enkelt-og dobbeltmærkede celler blev kvantificeret ved hjælp af både enkelt-og dobbeltkanalbilleder. Flere kriterier blev brugt til at identificere mærkede celler, herunder størrelse, morfologi, signal vs. baggrund og sammenfaldende DAPI-mærkning ved vurdering af DAPI-farvet væv. I en delmængde af sektioner blev der opsamlet 5 mm stakke ved hjælp af en Olympus Fluovvisning FV1000 for at sikre neuronal lokalisering af det mærkede objekt. På grund af vores interesse i andelen og ikke det absolutte antal af dobbeltmærkede celler blev stereologiske metoder ikke anvendt.
procentdelen af dobbeltmærkede celler pr.immunreaktiv (ir) cellegruppe blev bestemt for hvert billedfelt. Gennemsnitlig-standardfejl blev beregnet for hvert kortikalt område, der blev undersøgt. Envejsanalyse af varians (ANOVA) blev brugt til at evaluere forskelle mellem kortikale regioner. Fisher ‘ s HSD blev brugt til post-hoc analyse. Alle statistiske analyser blev udført med SPSS 15.0 for vinduer.
Antistofkontroller
kontroller omfattede udeladelse af primære antistoffer, udeladelse af sekundære antistoffer og udskiftning af primært antistof med uspecifik antistof (kanin IgG). Alle manipulationer havde de forventede virkninger og understøttede påstanden om, at mærkede celler repræsenterer ægte antigenmærkning ved deres tilsvarende antistoffer.
resultater
NGF-Immunmærkning
distinkt NGF-mærkning var synlig inden for en radius på 1.5 mm fra colchicin kortikale injektionssteder. Inden for disse områder var NGF-mærkning overvejende begrænset til celle somata (Figur 1). Sjældent kunne der også skelnes mellem en eller flere cellulære processer. Uden for denne radius på 1,5 mm var NGF-mærkning næsten ikke detekterbar i barken. Da kortikal ekspression af NGF-receptorerne TrkA og p75 er begrænset til kolinerge kortikopetale fibre, er det usandsynligt, at den observerede mærkning af NGF afspejler ENDOCYTOSERET NGF, men er i stedet tegn på NGF-producerende celler., 1995; Rossi et al., 2002; Stephens et al., 2005). Som rapporteret tidligere (Ribak et al., 1978) intensiverede colchicinbehandling GAD-mærkning i cellelegemer såvel som neuronale processer. Colchicin havde ingen påviselig virkning på mærkning af parvalbumin, calbindin eller CaMKIIa.
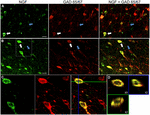
FIGUR 1. Nervevækstfaktor kolokaliseres i vid udstrækning med hæmmende cellemarkører. Immunreaktive celler i (A) primær motorisk hjernebark og (B) præfrontal hjernebark. Billeder viser, at NGF-mærkede celler (grøn) kolokaliseres i vid udstrækning med GAD 65/67-mærkede celler (rød). Hvide pile viser et eksempel celle immunreaktiv for både NGF og GAD 65/67 i hver kortikal region. Blå pile viser celler immunreaktive kun for GAD 65/67. (C) forstørret billede af området inde hvid boks i (B). D) rekonstruktion af den dobbeltmærkede celle, der er angivet i litra c). Grønne og blå linjer angiver dissektionsniveauer i hhv. Skalestænger = 25 liter.
NGF og Gabaergisk Co-lokalisering
nervevækstfaktor co-lokaliseret i vid udstrækning med de GABAergiske cellemarkører GAD65 og GAD67, uanset det undersøgte kortikale område (Figur 1; Tabel 1). Samlet set er 91 liter 0,9% af NGF-mærkede kortikale celler også mærket for GAD65/67. Procentdelen af NGF-mærkede celler, der co-udtrykker GAD65 / 67, viste ringe forskel mellem de præfrontale (90,0 liter 1,5%), motor (91,7 liter 1,5%), parietal (89,6 liter 3,5%) og temporal (93,4 liter 8,1%) cortices (envejs ANOVA; p = 0,78). Omvendt NGF Co-lokaliseret med kun 55 den 2.3% af alle GAD65 / 67-mærkede celler. For at bestemme, om NGF-produktion var begrænset til en specifik undertype af Gabaergisk neuron, co-mærkede vi væv til NGF og enten parvalbumin eller calbindin (figur 2). NGF-mærkede celler blev observeret at kolokalisere med begge markører. NGF-kolokalisering med parvalbumin (67,8 liter 3,6%) var imidlertid over 2 liter større end med calbindin (29,1 liter 3,9%). Derudover udgjorde NGF-IR-celler mindre end halvdelen af alle parvalbumin (47,7 gir 4,6%) og calbindin (25,7 gir 4,9%) immunreaktive celler.

FIGUR 2. NGF colabeled med hæmmende neuron underklasse markører. Skiver af motorbarken blev mærket for NGF og enten parvalbumin eller calbindin. (A) celler viste omfattende overlapning af NGF og parvalbumin mærkning (hvide pile). B) omvendt var kolabeling af NGF og calbindin mindre almindelig. Skalestænger = 25 liter.

TABEL 1. NGF-og GAD65/67-immunreaktive celler efter kortikal region.
Nervevækstfaktorudtrykkende neuroner blev observeret gennem alle kortikale lag. Tidligere undersøgelser har rapporteret ujævn fordeling af NGF-mærkede neuroner i de kortikale laminer (Pitts and Miller, 2000, 2006). Kvantitativ analyse efter lag blev imidlertid ikke udført i den aktuelle undersøgelse, da NGF-mærkningsintensiteten faldt med stigende afstand fra colchicin-injektionsstedet.
NGF og Glutamatergisk Co-lokalisering
mærkning af CaMKIIa blev primært observeret inden for celle somata og proksimale processer (figur 3). I modsætning til den omfattende co-lokalisering set med NGF og GABAergiske markører, NGF-mærkede celler sjældent Co-lokaliseret med CaMKIIa-mærkede celler (figur 3; Tabel 2). I alt blev 4,9 1,1% af NGF-immunreaktive celler Co-mærket med CaMKIIa-antistoffer. Co-lokalisering adskilte sig markant efter kortikal region (envejs ANOVA; p = 0,03); Fishers post hoc afslørede, at den præfrontale bark havde en større andel af dobbeltmærkede NGF-celler (7,6 liter 2,1%) sammenlignet med den primære motorbark (2,4 liter 1,0%; p = 0,02) og parietalbark (2,9% liter 1,5; p = 0,01).

FIGUR 3. Nervevækstfaktor kolokaliseres minimalt med den spændende cellemarkør CaMKIIa. Immunoreaktive celler i den præfrontale hjernebark. Celler blev sjældent colabeled for NGF (grøn) og CaMKIIa (rød), uanset kortikal region undersøgt. Guldpile viser et eksempel på en celle, der kun er immunreaktiv for NGF. Skalestænger = 25 liter.

TABEL 2. NGF – og CaMKIIa-immunreaktive celler efter kortikal region.
celler immunreaktive for CaMKIIa overgik i høj grad dem, der er mærket af NGF-antistoffer. Den samlede andel af CaMKIIa-mærkede celler, der samtidig udtrykker NGF-signal, var 2 liter 0,6%. Denne procentdel adskilte sig markant efter region (envejs ANOVA p = 0,003), hvor den præfrontale bark udviste en større andel af dobbeltmærkede NGF/CaMKIIa-celler (3,7 liter 1,1%) end den primære motorbark (0,8% liter 0,3; p = 0,001), parietalbarken (1,4% liter 0,6; p = 0,01) og den tidsmæssige bark (1,5 liter 0,6%; p = 0,01).
Diskussion
den aktuelle undersøgelse viser, at langt størstedelen (> 90%) af NGF-producerende neuroner i barken er GABAergiske, mens halvdelen af alle GABAergiske neuroner kolokaliseres med NGF. I modsætning hertil udviser markører af spændende neuroner kun sjælden co-lokalisering med NGF. Disse resultater var konsistente gennem flere kortikale regioner analyseret i denne undersøgelse, hvilket indikerer, at NGF primært produceres af hæmmende interneuroner i rotten neokorteks.
selvom NGF-immunreaktivitet sjældent faldt sammen med ophidsende cellemarkører (CAMKIIa), var en lille procentdel (~5%) positiv for CaMKIIa i alle undersøgte kortikale regioner. Konfokal analyse bekræftede, at denne dobbelte mærkning stammede fra det samme brændplan og ikke skyldtes diskret signal, der stammer fra overlappende celler. Den funktionelle betydning af NGF-ekspression i en så lille brøkdel af ophidsende celler i ikke kendt, men det er muligt, at disse NGF-producerende neuroner repræsenterer en tidligere uidentificeret underklasse af ophidsende neuroner i neokorteksen.
vores resultater er i overensstemmelse med resultaterne af tidligere undersøgelser i andre hjerneområder, der viser, at NGF næsten udelukkende lokaliserer med GABAergiske celler i striatum, basal forhjerne og hippocampus (Lauterborn et al., 1993, 1995; Pascual et al., 1998; Pernille et al., 1999). Således kan NGF-produktion af GABAergiske celler være en generel egenskab for alle mål, der modtager basal forhjerne cholinerge innervation (inklusive selve basal forhjerne). Disse kolinerge neuronale populationer kræver NGF til vedligeholdelse af deres fænotype og fremskrivninger (Rylett et al., 1993; Chen et al., 1997; Hu et al., 1997; Debeir et al., 1999). På tværs af undersøgelser, hæmmende interneuroner fremstår nu som den primære kilde til NGF-trofisme for basale forhjerne kolinerge neuroner.
selvom basal forhjerne cholinerge neuroner innerverer både stimulerende og hæmmende kortikale netværk., 1999), er kilden til trofisk støtte overvældende fra den hæmmende befolkning, som vides at spille en kritisk rolle i formidling af plasticitet i kortikale kredsløb (Hensch og Stryker, 2004; Yasaki-Sugiyama et al., 2009; Donato et al., 2013). Kolinerg signalering ser ud til at bidrage til differentiel aktivering af forskellige hæmmende subpopulationer og derved modulere ophidsende-hæmmende balance., 1998; Froemke et al., 2007). NGF kan derved fungere som et feedbacksignal mellem stærkt plastiske hæmmende netværk og de kolinerge indgange, der aktiverer dem. Faktisk øger NGF plasticitet og adfærdsmæssig læring gennem kolinerge-afhængige mekanismer (Prakash et al., 1996, 2004; Gutierres et al., 1997; Conner et al., 2009). Aktivitetsafhængig frigivelse af NGF (Blochl and Thoenen, 1995; Lessmann et al., 2003), parret med NGFS evne til at øge kolinerge aktivitet (Rylett et al., 1993; Hu et al., 1997; Auld et al., 2001), antyder, at NGF kan fremme omorganisering af aktive kredsløb via forbedret kolinerge funktion.
fremtidige undersøgelser vil forsøge at identificere, hvilke underklasser af hæmmende neuroner der udtrykker NGF, og hvordan dette udtryk præcist påvirker kortikale kredsløb. Til dette formål tog vi indledende skridt til at bestemme, om NGF Co-lokaliseret med to almindelige markører af hæmmende neuroner, parvalbumin (primært forbundet med kurv-og lysekroneceller) og calbindin (forbundet med adskillige hæmmende celletyper; McBain og Fisahn, 2001; Markram et al., 2004). Vores resultater viser, at NGF primært blev påvist i parvalbumin-immunreaktive celler, skønt mange celler mærket af parvalbumin ikke Co-udtrykte NGF. Det er vigtigt, at NGF-IR-celler også kolokaliseres med calbindin-mærkede celler, hvilket antyder, at mere end en underklasse af hæmmende neuron producerer NGF.
sammenfattende udtrykkes inden for rotten neokorteks NGF primært af hæmmende neuroner, en egenskab, der ser ud til at være konserveret fra fylogenetisk ældre hjerneområder, og som kan generaliseres til hjernen som helhed. Vores resultater antyder, at kortikale hæmmende interneuroner spiller en vigtig rolle i vedligeholdelsen af kolinerge projektionsneuroner i den basale forhjerne. GABAergiske interneuroner kan således fremme kortikal reorganisering via reguleret NGF-signalering.
interessekonflikt Erklæring
forfatterne erklærer, at forskningen blev udført i mangel af kommercielle eller økonomiske forhold, der kunne fortolkes som en potentiel interessekonflikt.
anerkendelser
finansieret af NIH (AG10435), Veterans Administration og Dr. Miriam og Sheldon G. Adelson Medical Research Foundation.
supplerende materiale
det supplerende materiale til denne artikel kan findes online på: http://www.frontiersin.org/journal/10.3389/fncel.2014.00220/abstract
Auld, D. S., Mennicken, F., Og R. (2001). Nervevækstfaktor inducerer hurtigt langvarig frigivelse af acetylcholin fra dyrkede basale forhjernneuroner: differentiering mellem neuromodulatoriske og neurotrofiske påvirkninger. J. Neurosci. 21, 3375–3382.
Pubmed abstrakt / Pubmed Fuld tekst
Bakin, J. S., og Viinberger, N. M. (1996). Induktion af en fysiologisk hukommelse i hjernebarken ved stimulering af nucleus basalis. Proc. Natl. Acad. Sci. USA 93, 11219-11224. doi: 10.1073 / pnas.93.20.11219
CrossRef Fuld tekst
J. L., Lauterborn, J. C. og Gall, C. M. (1999). Subpopulationer af striatale interneuroner kan skelnes på basis af neurotrofisk faktorekspression. J. Comp. Neurol. 408, 283–298. doi: 10.1002 / (SICI)1096-9861(19990531)408:2<283::støtte-CNE9>3.0.CO;2-2
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Blochl, A. og Thoenen, H. (1995). Karakterisering af nervevækstfaktor (NGF) frigivelse fra hippocampale neuroner: bevis for en konstitutiv og en ukonventionel natriumafhængig reguleret vej. EUR. J. Neurosci. 7, 1220–1228. doi: 10.1111 / j. 1460-9568.1995.tb01112.
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
de Camilli, P. (1993). Identifikation af en dominerende epitop af glutaminsyre decarboksylase (GAD-65) anerkendt af autoantistoffer i stiff-man syndrom. J. Eksp. Middelhavs. 178, 2097–2106. doi: 10.1084 / jem.178.6.2097
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Chang, Y. C. og Gottlieb, D. I. (1988). Karakterisering af proteinerne oprenset med monoklonale antistoffer mod glutaminsyre decarboksylase. J. Neurosci. 8, 2123–2130.
Chen, K. S., Nishimura, M. C., Armanini, M. P., C., Spencer, S. D. og Phillips, H. S. (1997). Forstyrrelse af en enkelt allel af nervevækstfaktorgenet resulterer i atrofi af basale forhjerne kolinerge neuroner og hukommelsesunderskud. J. Neurosci. 17, 7288–7296.
Pubmed abstrakt / Pubmed Fuld tekst
Conner, J. M., Chiba, A. A., M. H. (2005). Det basale forhjerne kolinerge system er afgørende for kortikal plasticitet og funktionel genopretning efter hjerneskade. Neuron 46, 173-179. doi: 10.1016 / j. neuron.2005.03.003
Pubmed Abstrakt / Pubmed Fuld Tekst / CrossRef Fuld Tekst
Conner, J. M. Culberson, A., Packovsky, C., Chiba, A. A., M. H. (2003). Læsioner i det basale forhjerne kolinerge system forringer opgaveopkøb og afskaffer kortikal plasticitet forbundet med motorisk færdighedsindlæring. Neuron 38, 819-829. doi: 10.1016 / S0896-6273(03)00288-5
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Conner, J. M., Franks, K. M., Titterness, A. K., Russell, K., Merrill, D. A., Christie,B. R., et al. (2009). NGF er afgørende for hippocampus plasticitet og læring. J. Neurosci. 29, 10883–10889. doi: 10.1523 / JNEUROSCI.2594-09.2009
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Conner, J. M., Lauterborn, J. C., Yan, K., Gall, C. M. Og Varon, S. (1997). Fordeling af hjerneafledt neurotrofisk faktor (BDNF) protein og mRNA i den normale voksne rotte CNS: bevis for anterograd aksonal transport. J. Neurosci. 17, 2295–2313.
Pubmed abstrakt / Pubmed Fuld tekst
Conner, J. M. Og Varon, S. (1992). Fordeling af nervevækstfaktorlignende immunreaktive neuroner i den voksne rottehjerne efter colchicin-behandling. J. Comp. Neurol. 326, 347–362. doi: 10.1002 / cne.903260304
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Conner, J. M. Og Varon, S. (1996). Karakterisering af antistoffer mod nervevækstfaktor: assayafhængig variabilitet i krydsreaktivitet med andre neurotrofiner. J. Neurosci. Metoder 65, 93-99. doi: 10.1016/0165-0270(95)00151-4
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Conner, J. M. Og Varon, S. (1997). UDVIKLINGSPROFIL af NGF-immunreaktivitet i rottehjernen: en mulig rolle for NGF i etableringen af kolinerge terminale felter i hippocampus og bark. Brain Res. Dev. Brain Res. 101, 67-79. doi: 10.1016 / S0165-3806(97)00051-5
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Debeir, T., Saragovi, H. U. Og Cuello, A. C. (1999). En nervevækstfaktor mimetisk TrkA-antagonist forårsager tilbagetrækning af kortikale kolinerge boutoner hos den voksne rotte. Proc. Natl. Acad. Sci. USA 96, 4067-4072. doi: 10.1073 / pnas.96.7.4067
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Donato, F., Rompani, S. B. Og Caroni, P. (2013). Parvalbumin-udtrykker kurv-celle netværk plasticitet induceret af erfaring regulerer Voksenuddannelse. Natur 504, 272-276. doi: 10.1038 / nature12866
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Erondu, N. E. og Kennedy, M. B. (1985). Regional fordeling af type II Ca2+ / calmodulin-afhængig proteinkinase i rottehjernen. J. Neurosci. 5, 3270–3277.
Froemke, R. C. M. M. Og Schreiner, C. E. (2007). Et synaptisk hukommelsesspor for kortikal modtagelig feltplasticitet. Natur 450, 425-429. doi: 10.1038 / nature06289
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Gall, C. M. Og Isackson, P. J. (1989). Limbiske anfald øger neuronal produktion af messenger RNA til nervevækstfaktor. Videnskab 245, 758-761. doi: 10.1126 / videnskab.2549634
CrossRef Fuld tekst
(1997). Indlæringsvanskeligheder og kolinerg deaferentation efter kortikal nervevækstfaktor deprivation. J. Neurosci. 17, 3796–3803.
Pubmed abstrakt / Pubmed Fuld tekst
Hanson, M., Og Edstr Larsm, A. (1978). Mitosehæmmere og aksonal transport. Int. Rev. Cytol. Suppl. 373–402.
(1993). Ekspression af genet for nervevækstfaktor (NGF) i Abens centralnervesystem. Hjerne Res. 618, 142-148. doi: 10.1016/0006-8993 (93) 90437-R
CrossRef Fuldtekst
Hefti, F. (1986). Nervevækstfaktor fremmer overlevelse af septale kolinerge neuroner efter fimbriale transektioner. J. Neurosci. 6, 2155–2162.
Hensch, T. K. og Stryker, M. P. (2004). Søjlearkitektur skulptureret af GABA-kredsløb til udvikling af kattes visuelle bark. Videnskab 303, 1678-1681. doi: 10.1126 / videnskab.1091031
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Hokfelt, T., Kellerth, J. O., Nilsson, G. og Pernou, B. (1975). Eksperimentelle immunhistokemiske undersøgelser af lokalisering og distribution af stof P i kat primære sensoriske neuroner. Brain Res. 100, 235-252. doi: 10.1016/0006-8993(75)90481-3
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
det er en af de mest almindelige måder at gøre det på. (1995). TrkA-ekspression i CNS: bevis for eksistensen af flere nye NGF-responsive CNS-neuroner. J. Neurosci. 15, 1567–1576.
Pubmed Abstrakt / Pubmed Fuld Tekst
Hu, L., Cote, S. L. og Cuello, A. C. (1997). Differentiel modulering af den kolinerge fænotype af nucleus basalis magnocellularis neuroner ved at anvende NGF på cellelegemet eller kortikale terminale felter. Eksp. Neurol. 143, 162–171. doi: 10.1006 / eksnr.1996.6357
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Huang, E. J. og Reichardt, L. F. (2003). Trk-receptorer: roller i neuronal signaltransduktion. Annu. Pastor Biochem. 72, 609–642. doi: 10.1146 / annurev.biochem.72.121801.161629
CrossRef Fuld tekst
Isackson, P. J., Huntsman, M. M., Murray, K. D. og Gall, C. M. (1991). BDNF mRNA-ekspression øges hos voksne rottehjerne efter limbiske anfald: tidsmæssige induktionsmønstre, der adskiller sig fra NGF. Neuron 6, 937-948. doi: 10.1016 / 0896-6273 (91)90234-K
Pubmed abstrakt | Pubmed Fuld tekst / CrossRef Fuld tekst
Ito, T., Hioki, H., Nakamura, K., Tanaka, Y., Nakade, H.,Kaneko, T., et al. (2007). Gamma-aminosmørsyreholdige sympatiske preganglioniske neuroner i rotte thoracale rygmarv sender deres aksoner til den overlegne cervikale ganglion. J. Comp. Neurol. 502, 113–125. doi: 10.1002 / cne.21309
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Kilgard, M. P., M. M. (1998). Cortical kort reorganisering aktiveret af nucleus basalis aktivitet. Videnskab 279, 1714-1718. doi: 10.1126 / videnskab.279.5357.1714
Pubmed Abstrakt / Pubmed Fuld Tekst / CrossRef Fuld Tekst
J. H., Bartus, R. T. M., Schatteman, G. og Gash, D. M. (1988). Nervevækstfaktorreceptorimmunoreaktivitet i den ikke-humane primat (Cebus apella): distribution, morfologi og kolokalisering med kolinerge stoffer. J. Comp. Neurol. 277, 465–486. doi: 10.1002 / cne.902770402
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
han er en af de mest kendte og mest kendte mennesker i verden, der har en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens til at have en tendens. (1994). Den gamle abe basal forhjerne: redning og spiring af aksotomiserede basale forhjernneuroner efter transplantater af indkapslede celler, der udskiller menneskelig nervevækstfaktor. Proc. Natl. Acad. Sci. USA 91, 10898-10902. doi: 10.1073 / pnas.91.23.10898
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Korsching, S., Auburger, G., Heumann, R., Scott, J. og Thoenen, H. (1985). Niveauer af nervevækstfaktor og dets mRNA i rottens centralnervesystem korrelerer med kolinerg innervering. EMBO J. 4, 1389-1393.
Pubmed abstrakt / Pubmed Fuld tekst
Lad, S. P., Neet, K. E. og Mufson, E. J. (2003). Nervevækstfaktor: struktur, funktion og terapeutiske konsekvenser for sygdommen. Curr. Lægemiddelmål CNS Neurol. Disord. 2, 315–334. doi: 10.2174/1568007033482724
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
stor, T. H., Bodary, S. C., Clegg, D. O., Viskamp, G., Otten, U. Og Reichardt, L. F. (1986). Nervevækstfaktorgenekspression i den udviklende rottehjerne. Videnskab 234, 352-355. doi: 10.1126 / videnskab.3764415
CrossRef Fuld tekst
Lauterborn, J. C., J. L., Tran, T. M. og Gall, C. M. (1995). NGF mRNA udtrykkes af GABAergiske, men ikke kolinerge neuroner i rottebasal forhjerne. J. Comp. Neurol. 360, 454–462. doi: 10.1002 / cne.903600307
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Lauterborn, J. C., Tran, T. M., Isackson, P. J. og Gall, C. M. (1993). Nervevækstfaktor mRNA udtrykkes af GABAergiske neuroner i rotte hippocampus. Neuroreport 5, 273-276. doi: 10.1097/00001756-199312000-00023
CrossRef Fuld tekst
Lessmann, V., Gottmann, K. og Malcangio, M. (2003). Neurotrophinsekretion: aktuelle fakta og fremtidsudsigter. Prog. Neurobiol. 69, 341–374. doi: 10.1016 / S0301-0082(03)00019-4
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
D. M., Kromer, L. F., Kaplan, D. R., Chua-Cousons, J., Clary,D. O., et al. (1995). Regulering af TrkA og ChAT udtryk i udviklingen af rotte basal forhjerne: bevis for, at både eksogen og endogen NGF regulerer differentiering af kolinerge neuroner. J. Neurosci. 15, 2888–2905.
Pubmed abstrakt / Pubmed Fuld tekst
det er en af de mest almindelige måder at gøre det på. (1990). NT-3, BDNF og NGF i det udviklende rotte nervesystem: parallelle såvel som gensidige udtryksmønstre. Neuron 5, 501-509. doi: 10.1016 / 0896-6273 (90)90089-
Pubmed abstrakt | Pubmed Fuld tekst / CrossRef Fuld tekst
Markram, H.(2004). Interneuroner af det neokortiske hæmmende system. Nat. Pastor Neurosci. 5, 793–807. doi: 10.1038 / Nrn1519
Pubmed abstrakt | Pubmed Fuld tekst | CrossRef Fuld tekst
McBain, C. J. og Fisahn, A. (2001). Interneuroner ubundet. Nat. Pastor Neurosci. 2, 11–23. doi: 10.1038/35049047
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Mufson, E. J., Conner, J. M., Varon, S., J. H. (1994). Nervevækstfaktor-lignende immunreaktive profiler i primat basal forhjerne og Hippocampus dannelse. J. Comp. Neurol. 341, 507–519. doi: 10.1002 / cne.903410407
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Pascual, M., Rocamora, N., Acsady, L., Freund, T. F. og Soriano, E. (1998). Ekspression af nervevækstfaktor og neurotrophin – 3 mRNA ‘ er i hippocampale interneuroner: morfologisk karakterisering, ekspressionsniveauer og kolokalisering af nervevækstfaktor og neurotrophin-3. J. Comp. Neurol. 395, 73–90. doi: 10.1002 / (SICI)1096-9861(19980525)395:1<73::støtte-CNE6>3.0.CO; 2-E
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Pasteels, B., Miki, N., Hatakenaka, S. og Pochet, R. (1987). Immunhistokemisk krydsreaktivitet og elektroforetisk comigration mellem calbindin D-27 kDa og visinin. Brain Res. 412, 107-113. doi: 10.1016/0006-8993(87)91444-2
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
S., P. (2006). Udviklingsmæssige ændringer af neurotrophin mRNA-ekspression i lagene af rottebark. EUR. J. Neurosci. 24, 2453–2460. doi: 10.1111 / j. 1460-9568.2006.05126.
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Pitts, A. F. Og Miller, M. V. (2000). Ekspression af nervevækstfaktor, hjerneafledt neurotrofisk faktor og neurotrophin-3 i den somatosensoriske bark af den modne rotte: coekspression med neurotrofinreceptorer med høj affinitet. J. Comp. Neurol. 418, 241–254. doi: 10.1002 / (SICI)1096-9861(20000313)418:3<241::støtte-CNE1>3.0.CO;2-m
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Prakash, N., Cohen-Cory, S. og Frostig, R. D. (1996). Hurtige og modsatte virkninger af BDNF og NGF på den funktionelle organisering af voksenbarken in vivo. Natur 381, 702-706. doi: 10.1038 / 381702a0
Pubmed abstrakt | Pubmed Fuld tekst | CrossRef Fuld tekst
Prakash, N., Cohen-Cory, S., Penschuck, S. og Frostig, R. D. (2004). Basal forhjerne kolinerge system er involveret i hurtig nervevækstfaktor (NGF)-induceret plasticitet i tøndebarken hos voksne rotter. J. Neurofysiol. 91, 424–437. doi: 10.1152 / jn.00489.2003
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Ribak, C. E., Vaughn, J. E. og Saito, K. (1978). Immunocytokemisk lokalisering af glutaminsyre decarboksylase i neuronal somata efter colchicin inhibering af aksonal transport. Brain Res. 140, 315-332. doi: 10.1016/0006-8993(78)90463-8
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Rossi, F. M., Sala, R. og Maffei, L. (2002). Ekspression af nervevækstfaktorreceptorerne TrkA og p75NTR i den visuelle bark af rotten: udvikling og regulering af det kolinerge input. J. Neurosci. 22, 912–919.
Pubmed abstrakt / Pubmed Fuld tekst
Rylett, R. J., Goddard, S., Schmidt, B. M. og Vilhelm, L. R. (1993). Acetylcholinsyntese og frigivelse efter kontinuerlig intracerebral administration af NGF hos voksne og ældre Fischer-344 rotter. J. Neurosci. 13, 3956–3963.
Pubmed abstrakt / Pubmed Fuld tekst
Schubert, P., Kreutberg, G. V. og H. D., H. D. (1972). Neuroplasmisk transport i dendritter: effekt af colchicin på morfologi og fysiologi af motoneuroner i katten. Brain Res. 47, 331-343. doi: 10.1016/0006-8993(72)90643-9
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Shelton, D. L. Og Reichardt, L. F. (1986). Undersøgelser af ekspressionen af beta nervevækstfaktor (NGF) gen i centralnervesystemet: niveau og regional fordeling af NGF mRNA antyder, at NGF fungerer som en trofisk faktor for flere forskellige populationer af neuroner. Proc. Natl. Acad. Sci. USA 83, 2714-2718. doi: 10.1073 / pnas.83.8.2714
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
(2001). Nervevækstfaktor signalering, neurobeskyttelse og neural reparation. Annu. Pastor Neurosci. 24, 1217–1281. doi: 10.1146 / annurev.neuro.24.1.1217
CrossRef Fuld tekst
Stephens, H. E., Belliveau, A. C., Gupta, J. S., Mirkovic, S. og Kablar, B. (2005). Neurotrophins rolle i vedligeholdelsen af rygmarvsmotorneuroner og dorsale rodganglier proprioceptive sensoriske neuroner. Int. J. Dev. Neurosci. 23, 613–620. doi: 10.1016 / j. ijdevneu.2005.07.002
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
M. H., Armstrong, D. M. Og Gage, F. H. (1990). Basal forhjernecelletab efter fimbria / forniks-transektion. Brain Res. 508, 241–248. doi: 10.1016 / 0006-8993(90)90402-V
CrossRef fuldtekst
Huguenard, J. R. og Prince, D. A. (1998). Kolinerge skift inden for neokortikale hæmmende netværk. Videnskab 281, 985-988. doi: 10.1126 / videnskab.281.5379.985
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
Kang, S., Cateau, H., Fukai, T. og Hensch, T. K. (2009). Tovejs plasticitet i hurtigt spiking GABA kredsløb ved visuel oplevelse. Natur 462, 218-221. doi: 10.1038 / nature08485
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
(1999), Somogyi, J., Nadasdy, S., og Kallo, I. (1999). Det basale forhjerne kortikopetal system revideret. Ann. N. Y. Acad. Sci. 877, 339–367. doi: 10.1111 / j. 1749-6632.1999.tb09276.
Pubmed abstrakt / Pubmed Fuld tekst / CrossRef Fuld tekst
H. T., H. T., Li, L. Y., Song, H. B., Hu, Y. L., Feng,S. T., Et Al. (2007). Immunhistokemisk fordeling af NGF, BDNF, NT-3og NT-4 i voksne rhesusabehjerner. J. Histochem. Cytochem. 55, 1–19. doi: 10.1369/jhc.6A6952.2006
Pubmed Abstract | Pubmed Full Text | CrossRef Full Text