Kvantitative målinger av fysiologiske egenskaper som enzymaktivitet uttrykkes ofte som aktivitetsenheter per milligram protein. Selv om mange analyser er utviklet for å måle proteininnhold, inkludert kolorimetriske analyser Av Amido Black (1), Biuret (2), Bikinchoninsyre (3) Og Coomassie Blue (4,5), Er Lowry-analysen (6) eller dens modifikasjoner (7,8) mer vanlig enn andre analyser (9). Lowry-analysen er enkel, sensitiv og presis, og er den mest siterte (10) prosedyren for kvantitativ proteinbestemmelse.
et bredt utvalg av forbindelser som reagerer Med Folin-Ciocalteu fenol (Folins) reagens (11) er en kilde til potensiell interferens I Lowry og modifiserte Lowry proteinanalyser. Heldigvis er korreksjoner gjennom en passende blank tilstrekkelig for de fleste forbindelser (6,7) unntatt lipider (12), vaskemidler (13) og fargede stoffer (14). Vanskeligheter med å analysere proteiner i nærvær av lipider og vaskemidler (brukt i løseliggjøring av fettvev, myelin og skjelettmuskler) ble overvunnet av den modifiserte Lowry-analysen (15; referert Til I dette papiret Som U-1988-analysen, 16). Fargeinterferens ved å bestemme proteininnholdet i rødvin (14,17,18) ble overvunnet ved å benytte omfattende kromatografi. Ovennevnte tilnærming er tungvint og ikke veldig praktisk for å håndtere et stort antall prøver. Ingen av de kjente proteinanalysene var egnet til å måle proteiner i fargede biologiske prøver, f. eks., farget frukt og grønnsaker, rødvin, pigmenterte mikrober og drøvtyggende galle.
vår utvikling Av u-2012-analysen fra sine forgjengere u-1988 og Lowry-analysen har oppnådd tre store fordeler (i) bekvemmelighet gjennom stabilitet av reagensformuleringene, (ii) måling av protein i både fargeløse og fargede biologiske prøver uten å svekke følsomheten, og (iii) analyse av proteiner ved svært lave konsentrasjoner. Denne nye analysen vil gjelde for kvantitativ bestemmelse av protein i både fargeløse og fargede biologiske prøvehomogenater, inkludert de som er rike på lipider (f.eks. avokado) og de som er vanskelige å homogenisere.
- Materialer og metoder
- Biologiske prøver – rødbeter, blåbær og rødvin
- Kjemiske reagenser
- Forbedringer Av u-1988-analysen
- u-2012-analysen
- Estimering av fargeinterferenser i u-2012-analysen
- standardkurven og dens parametere
- Beregning av proteininnhold i homogenatene
- Resultater og diskusjon
- Forbedringer I u-1988-analysen
- proteinestimering i fargede biologiske prøver
- proteinekstraksjon
- Eliminere forstyrrende stoffer
- Standardkurver og deres parametere
- Proteininnhold av farget homogenat
- Anerkjennelser
- Konkurrerende interesser
- Supplerende data
Materialer og metoder
Biologiske prøver – rødbeter, blåbær og rødvin
Rødbeter og blåbærhomogenater ble fremstilt som beskrevet i Tilleggsmaterialet. Rødvin krevde ikke proteinekstraksjon før u-2012-analysen.
Kjemiske reagenser
alle kjemiske reagenser, unntatt natriumhypokloritt og perklorsyre (PCA), ble oppnådd Fra Sigma Eller Sigma-Aldrich (St Louis, MO. USA). Natriumhypokloritt var Fra Acros Organic, New Jersey, USA. PCA ble hentet FRA BDH (England).
Forbedringer Av u-1988-analysen
Bytte fra karbonat til fosfatbuffer ved pH 12,0 forbedret reagensstabilitet og ga en liten økning i følsomhet. Acetonitril ble introdusert for å unngå vaskemiddelinducerte bobler. NaOH erstattet KOH for å unngå nedbør i proteinanalysen. I tillegg ble effektiviteten forbedret ved å kombinere forskjellige komponenter Av Lowry-reagenset i en reagensblanding.
u-2012-analysen
Fullstendige detaljer Om u-2012-analysen er gitt I Tilleggsmateriale. Protokollen, kort oppsummert I Figur 1, beskriver behandlingen av rødvin og homogenatene av rødbeter og blåbær, og inkluderer forbedringene Til u-1988-analysen. U-2012-analysen ble anvendt for ubehandlede, bearbeidede og omvendte bearbeidede (H2O2-behandling etterfulgt av TCA eller PCA-utfelling) proteiner. Analyser ble utført PÅ BSA, karbonsyreanhydrase, cytokrom C, isocitrat dehydrogenase, lysozym og trypsin for utvikling av standardkurver og i fargede biologiske prøver. Bestemmelsen av proteiner i de biologiske prøvene ble utført ved å kalibrere til passende standardkurver.
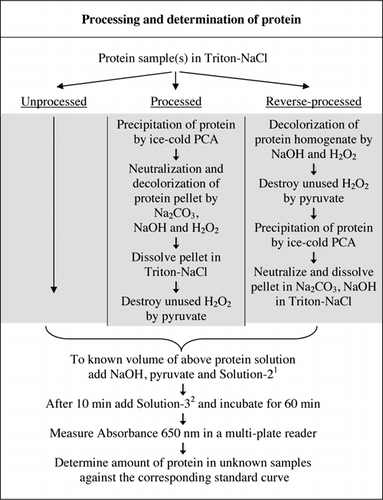
1solution-2 inneholdt kobbersulfat (CuSO4.5h2o), Na-K-Tartrat, SDS og acetonitril i 100 mM fosfatbuffer (pH 12,0). 2For Løsning-3 ble Folin-Ciocalteus fenolreagens fortynnet 1:1 med avionisert vann rett før bruk.
Estimering av fargeinterferenser i u-2012-analysen
fargeinterferens ble bestemt ved å sammenligne absorpsjon fra bearbeidede og ubehandlede rødbeter -, blåbær-og rødvinsprøver både med Og uten Bruk Av Folins reagens som beskrevet i Figur 1. Forholdet ble brukt til å fastslå omfanget av interferens, Hvor Abs1 er absorbans av ubehandlede prøver Med Folins reagens; Abs2 er absorbans av ubehandlede prøver uten Folins reagens; Abs3 er absorbans av behandlede prøver Med Folins reagens; Og Abs4 er absorbans av behandlede prøver uten Folins reagens.
standardkurven og dens parametere
Løsning-1b og 1c beskrevet i Oppskriftsdelen av det vedlagte Tilleggsmaterialet ble brukt til utvikling av standardkurvene. Konsentrasjonen AV BSA og de tilsvarende absorbansverdiene ble plottet ved Hjelp Av en xy-scattergraf. Formen på denne grafen (Figur 2) viser en mettet respons ved høyere konsentrasjoner med en svært begrenset innledende lineær respons. Dette var en foretrukket kurveform rapportert tidligere (20). I utgangspunktet ble dette modellert ved hjelp av en eksponentiell form (19), men senere studier viste at en rektangulær hyperbel ga en forbedret tilpasning med responsen, spesielt ved lavere konsentrasjoner. Denne sistnevnte form er nå standardisert og følgende tre-parameter ligning ble brukt til å beskrive absorbans-proteinkonsentrasjon forholdet:

Konc = proteinkonsentrasjon,
A = Absorbans Ved Konc,
A0= Absorbans ved nullkonsentrasjon,
AM = Absorbans ved maks konsentrasjon,
C50= Konsentrasjon som gir absorbans
(AM + A0) / 2.
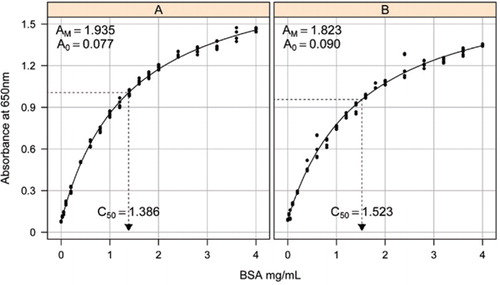
Estimering av standardkurven mellom absorbansen (650 nm) og konsentrasjoner AV bsa-protein ble gjort på tre tekniske replikater til (a) den ubehandlede proteinanalysen (parametere A0= 0,077, Am=1,935, C50=1.386), Og (B) den behandlede proteinanalyse (parametere A0=0,90, Am=1,823, C50=1,523). En rektangulær hyperbel – modell (ligning ) ble montert på de observerte dataene. Parameterestimater identifiseres i kurvene Med c50-estimeringen på x-aksen (prikket svart linje).
Parameter A0 ble eksperimentelt bestemt MENS AM Og C50 ble estimert ved Hjelp Av Microsoft Excel Toolbox add-In Solver Funksjon. Et prøvesett med parametere ble brukt til å beregne den modellerte absorbansen ved hver av standardkonsentrasjonene (Konc) ved hjelp av ligning . Solver ble deretter befalt å minimere reststandardavviket mellom den målte og modellerte absorbansen for standardsettet ved å justere AM og C50.
vi observerte forholdet mellom absorbans og konsentrasjon for å vise en ikke-lineær kurve over hele konsentrasjonsområdet, noe som sannsynligvis skyldes en komponent av lysspredning som øker etter hvert som konsentrasjonen av protein øker ved måling av absorbans. En dårlig lineær passform ved lav absorbans ble også rapportert Av Coakley Og James (20).
Beregning av proteininnhold i homogenatene
Analysene ble utført på bearbeidet og ubehandlet rødvin og homogenater av rødbeter og blåbær. BSA og andre proteinprøver ble behandlet identisk for passende standardkurver for å bestemme a0 -, AM-og C50-verdier. Disse parametrene ble deretter brukt til å konvertere prøveabsorbans (A) til proteinkonsentrasjon i hvert homogenat ved bruk av:

fordi ligningen har en mettet form, reduserer følsomheten som absorbans (A), og dermed konsentrasjonen øker. Feil i proteinberegninger kan minimeres ved å justere konsentrasjonene av homogenater i analysen slik at De ikke overskrider C50-verdien for mye.
Homogenatkonc-verdien ble deretter omdannet til vevsproteinkonsentrasjon (Vevskonc i mg/g vev) ved hjelp av følgende formel:

Når Homogenatkonc (i mg protein/mL) er korrigert for enhver pre-konsentrasjon eller fortynning under analysen. Homogenatprosent var 100 g vev homogenisert til et totalt volum på 200 mL (i vårt tilfelle 50%).
i en separat studie ble en rektangulær hyperbel-modell montert ved bruk av ikke-lineære blandede effekter (NLME) – pakken (21) I R (22) (Figur 2). Hver BSA-løsning, laget uavhengig i laboratoriet, ble modellert som en tilfeldig effekt, med en felles A0 men forskjellige am og C50 koeffisienter. Dette modellerer hierarkiet av biologiske prøvereplikater og tekniske analysereplikater.
Resultater og diskusjon
Forbedringer I u-1988-analysen
begrensningen Av u-1988 og Lowry-analysen er ustabiliteten til karbonatbasert reagens. Karbonatbufferen (pH 11,4 ved 2% = 188,7 mM) I U-1988 ble erstattet med 40 mM fosfat ved pH-verdier fra 11,4 til 12,5. Innledende bakker fra standardkurvene til proteinanalysen ved BRUK av BSA ved 0,5 mg BSA / mL og 1,0 mg BSA / mL ble beregnet. De første bakkene med fosfatbuffere ved pH 11,4 og ved optimal pH 12,0 var 99 x10-6 og 197 x10-6respektivt. Hellingen for karbonatbufferen (pH 11,4) var 162 x10-6.Siden hellingsverdien er en direkte indikasjon på analysefølsomhet, fosfatbuffer (pH 12.0) ble valgt for å erstatte karbonatbuffer, noe som gir en 25% økning i følsomhet.
større stabilitet ble oppnådd ved å øke konsentrasjonen av fosfatbufferen til 100 mM. den resulterende fosfat / CuSO4 / Na-K-tartratoppløsningen var stabil ved romtemperatur i to uker, betydelig lengre enn karbonat / CuSO4 / Na-K-tartratoppløsningen, som må tilberedes daglig før proteinanalyse. For alle fremtidige eksperimenter ble 100 mM fosfat (pH 12,0) brukt til å forberede CuSO4/Na-K-tartrat-løsningen. Vi tror at erstatning av karbonat med fosfat vil øke bekvemmeligheten Av u-2012-analysen.
bobler indusert Vaskemiddel blir en viktig feilkilde i absorbansmålinger ved bruk av en flerbrønnplateleser (ikke et problem med kyvetter). Disse boblene ble betydelig redusert ved tilsetning av et antall polare løsningsmidler (f.eks. aceton, acetonitril, etanol og metanol). Acetonitril, den mest polare av disse løsningsmidlene (23) ble valgt for sin effektivitet og inkludert I Solution-2 (se Figur 1 bildetekst og Oppskrifter delen Av Supplerende Materiale).
Fosfatbuffer, CuSO4, Na-K-tartrat, sds og acetonitril kan tilsettes individuelt, og rekkefølgen av deres tillegg påvirker ikke den resulterende absorbansen. Imidlertid forbedrer bruk av en ferdigblandet løsning ytterligere bekvemmelighet, spesielt når et stort antall prøver skal analyseres. Vi grupperte derfor disse komponentene i analyseblandingen I Løsning-2 (Figur 1). En slik ferdigblandet oppløsning var ikke mulig for Den opprinnelige Lowry-analysen (6) på grunn av ustabilitet i karbonatoppløsningen. Forsøket på å inkludere Solution – 3 I Solution-2 resulterte i dramatisk reduksjon i utviklingen av blå farge og ble ikke vurdert videre.
proteinestimering i fargede biologiske prøver
proteinekstraksjon
Proteiner fra rødbeter og blåbær ble ekstrahert I Triton X-100-NaCl-oppløsning med mild homogenisering. Slike homogenater beholder deres enzymaktivitet (15). Denne utvinningen var ikke nødvendig for rødvin.
Eliminere forstyrrende stoffer
for fargede prøver er det nødvendig å fjerne forstyrrelsen på grunn av den iboende prøvefargen og andre ikke-proteinstoffer som reagerer med proteinreagensene før kolorimetrisk proteinanalyse. Nyheten Av U-2012 er å utarbeide en avfargingsprotokoll som er kompatibel med en kolorimetrisk proteinanalyse.
Avfarging av fargede pigmenter med natriumhypokloritt eller H2O2 og selektiv utfelling av proteiner med PCA eller TCA ble vurdert for fjerning av interfererende stoffer. Natriumhypokloritt, H2O2, TCA og PCA ble evaluert for deres kompatibilitet Med u-2012-analysen ved BRUK AV BSA som testprotein. Mellom natriumhypokloritt OG H2O2 var BARE H2O2 kompatibel da et bunnfall ble dannet i nærvær av hypokloritt. Proteiner utfelt AV TCA eller PCA kan analyseres Av U-2012 etter tilstrekkelig nøytralisering av restsyre i pelleten. Overlegenhet AV PCA over TCA for proteinutfelling er rapportert (24,25). I kontrast, i vår komparative evaluering, avslørte lignende C50-verdier FOR PCA (1.395) og TCA (1.400). VI foretrakk PCA fordi DEN er lett tilgjengelig som en ferdig løsning (70% v / v) og derfor lett fortynnet til ønsket styrke. TCA er et hygroskopisk fast stoff som er vanskelig å veie nettopp på grunn av det variable vanninnholdet.
det er to mulige måter å kombinere PCA og H2O2 på. FOR» behandlede «proteiner BLE PCA-behandling etterfulgt AV H2O2-behandling og FOR» omvendt behandlet » protein, gikk H2O2-behandling foran PCA-nedbør. Fordelene ved å bruke ‘bearbeidet’ protein var fjerning av en rekke forstyrrende stoffer i supernatanten og mulig inaktivering av proteolytiske enzymer under prøvepreparering. Dette ble bekreftet ved analyse av behandlet og omvendt behandlet trypsin og BSA (Se Tabell 1). Bare behandlede prøver ble brukt til å bestemme det faktiske proteininnholdet i fargede biologiske prøver
BÅDE PCA-og H2O2-behandlinger av fargede prøver var nødvendige for interferenseliminering I u-2012-analysen. Syreutfelling alene av de fargede prøvene fjernet ikke forstyrrelsen helt. Med alle de fargede prøvene ble noe farge kassert i supernatanten, men pelletsene ble også farget. Farge ble eliminert fra pellets VED H2O2 behandling. Alkaliske forhold var nødvendig for både effektiv avfarging AV H2O2 (26) og fargeutviklingen Av Folins reagens for å sikre at proteinnivåene måles riktig. Selv Om Både NaOH og KOH kunne gi den nødvendige alkaliteten, var Bare NaOH kompatibel med u-2012-analysen. Et bunnfall ble dannet i NÆRVÆR AV KOH. I pellets ble PCA nøytralisert Ved Hjelp Av Na2CO3 Og NaOH (27). Ytterligere NaOH ble lagt til under analysen; det optimaliserte volumet var mellom 50 til 70 µ (60 µ ble rutinemessig brukt); Se Figur 1.
Rødbeter, blåbær og rødvin ble misfarget med 15 µ på 30% H2O2 og tok henholdsvis 0,5 og 2 timer ved 50°C og romtemperatur. Tjue mikroliter på 30% H2O2 for 1 h ved 50°C ble brukt til å takle sterkere fargede prøver. Oksidasjon av stoffer som sukker bundet TIL proteiner VED H2O2 ved 50°C virker kritisk da romtemperaturbehandling overvurderer proteininnholdet. For rødbeter reduserte 50°c-behandling det tilsynelatende proteinestimatet til 14% av det ubehandlede, mens romtemperaturbehandling bare halverte dette estimatet.
det var tydelig fra kolorimetriske analyser utført etter hydrogenperoksidbehandling at NOEN H2O2 ikke ble benyttet i avfargingen. I en slik prøve ble Sluttfargen Til Lowry-analysen delvis ødelagt. Det var derfor nødvendig å ødelegge det gjenværende hydrogenperoksidet før proteinanalyse. Det er to KILDER TIL H2O2 I u-2012-analysen; H2O2 tilsatt for avfarging og H2O2 tilstede som forurensning I Triton X-100 (0,22%, Produktinformasjon: Triton X-100, www.sigmaaldrich.com). Hydrogenperoksid blir vanligvis degradert av enzymet katalase. Imidlertid vil den høye pH i proteinanalysen inaktivere kjente katalaser. Også tilsetning av katalase vil føre til tilsetning av ekstra protein. Vi valgte kjemisk destruksjon AV H2O2 ved hjelp av pyruvat (28). Kjemien til pyruvat-H2O2-interaksjonsligningen er godt etablert (28,29). Pyruvat ødelegger H2O2 ved romtemperatur i henhold til følgende reaksjon:

Resterende H2O2 i pelletsuspensjonen ble ødelagt ved behandling med 0,9 m pyruvat (1,5 x konsentrasjon AV H2O2) for 0,5 h ved romtemperatur. For å motvirke forurensende H2O2 I Triton X-100 ble ekstra pyruvat også tilsatt i proteinanalysen (Figur 1). Tilsetningen av pyruvat ga lavere absorbans for et ikke-proteinemne . Vi foreslår at peroksidforurensningen I Triton X-100 reagerer med acetonitrilen I Solution-2, noe som gir litt høyere absorpsjon.
fargeforstyrrelsen forbundet med de fargede biologiske prøvene kan ikke bare tas i betraktning ved å kjøre en proteinanalyse i fravær Av Folins reagens. De beregnede forholdene (Abs1-Abs2) / (Abs3-Abs4) indikerte at interferens fra prøvefarge var høyest for rødvin (=40) og mindre for blåbær (=6) og rødbeter (=2). Denne forstyrrelsen oversettes til unormalt høye estimater av ekte proteinnivåer; for eksempel konsentrasjonen av protein ved bruk av ubehandlede og bearbeidede rødbeterhomogenater (henholdsvis 20,21 mot 2,89 mg protein / g vev). I tillegg til fargeinterferens vil rødvin og homogenater av rødbeter og blåbær sannsynligvis inneholde stoffer som vil reagere Med Folins reagens i u-2012-analysen (e .g., små peptider og komplekse sukkerarter). Disse ble fjernet ved selektivt utfelling av proteiner med iskald PCA ved en endelig konsentrasjon på 5% (Figur 1).
Standardkurver og deres parametere
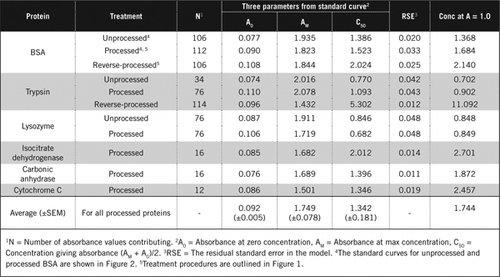
Standardkurver for ubehandlet OG bearbeidet BSA er vist I Figur 2. De avledede parametrene (A0, AM Og C50) er også oppført I Tabell 1 for BSA og andre proteiner.
resultatene viser at reststandardfeilen i modellen er lav (0,012 til 0,048), noe som indikerer at dataene passer bedre til den rektangulære hyperbel-trenden. For å sammenligne informasjon mellom ulike proteiner og deres behandling ble parametrene omdannet til konsentrasjonen for absorbans = 1,0 ved 650 nm (høyre kolonne I Tabell 1).
disse resultatene viser at tap av protein (sammenlignet med ubehandlet protein) i behandlede prøver var mindre enn de omvendte behandlede prøvene. Dette tapet var mer tydelig i tilfelle av trypsin, og det kan forklares på grunnlag av sin auto-katalytiske aktivitet under omvendt behandling. Vi anbefaler at den bearbeidede protokollen (Supplerende Materiale) bare følges for biologiske prøver som sannsynligvis inneholder proteolytiske enzymer.
i Den opprinnelige Lowry-analysen (6) og dens modifiserte versjon U-1988 (15) ble bare den lineære delen av standardkurven oppnådd ved å plotte absorbansen mot mengden protein brukt i kvantitativ bestemmelse av protein. I u-2012-analysen bruker vi dataene mer effektivt ved å montere en rektangulær hyperbola-ligning som beskrevet i Materials and methods-delen i tråd Med Coakley og James (20).
Proteininnhold av farget homogenat
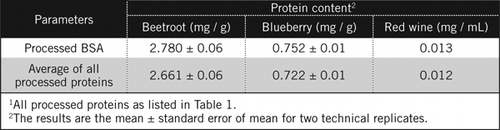
proteinkonsentrasjoner i ukjente prøver ble beregnet ved ligning og mot behandlet BSA-standard og gjennomsnittet av alle behandlede proteiner oppført i Tabell 1. Sistnevnte vil være nærmere et sant estimat for biologiske prøver som inneholder en blanding av proteiner. Vi estimerte proteinmengdene i blåbær og rødbeter i forhold til rødvin som henholdsvis 60 og 230 ganger (Tabell 2).
som BSA ble rødvin og 50% homogenater av rødbeter og blåbær behandlet ved pca-nedbør og avfarging AV H2O2 (Figur 1). På dette stadiet ble de biologiske prøvene konsentrert 40 ganger for rødvin og 4 ganger for rødbeter og blåbær. PÅ SAMME MÅTE ble BSA (2 mg/mL) også konsentrert 4 ganger til 8 mg/mL. Absorbansen av de fargede prøvene som var nær absorbansen For C50 (for ubehandlet BSA) ble brukt til å beregne proteininnholdet, som beskrevet ved ligning og .
Avslutningsvis har u-2012-analysen benyttet stabile reagenser, gitt forbedret følsomhet (selv for fargeløse biologiske prøver) og overvunnet fargeindusert interferens for fargede biologiske prøver. U-2012-analysen er ikke begrenset til den lineære delen av responsen mellom proteinkonsentrasjon og absorbans og gjør mer effektiv bruk av data i den ikke-lineære regionen gjennom en rektangulær hyperbolsk kurvemodell tilpasset standardene ved hjelp av enkle prosedyrer I Microsoft Excel.
Anerkjennelser
Forfattere anerkjenner Stiftelsen For Forskning, Vitenskap Og Teknologi New Zealand For økonomisk støtte (C06X0809).
Konkurrerende interesser
forfatterne erklærer ingen konkurrerende interesser.
Supplerende data
for å se supplerende data som følger med denne artikkelen, vennligst besøk journalens nettside på: www.future-science.com/doi/suppl/10.2144/000113818
- 1. Kaplan, R. S. Og P. L. Pedersen. 1985. Bestemmelse av mikrogram mengder protein i nærvær av milligram nivåer av lipid med amido svart 10b.Anal. Biochem. 150:97–104.Crossref, Medline, CAS, Google Scholar
- 2. Han er en av de eldste i verden. 1949. Bestemmelse av serumproteiner ved hjelp av biuret-reaksjonen. J. Biol. Chem. 177:751–766.Medline, CAS, Google Scholar
- 3. Smith, P. K., R. I. Krohn, G. T. Hermanson, A. K. Mallia, F. H. Gartner, M. D. Provenzano, E. K. Fujimoto, N. M. Goeke, et al.. 1985. Måling av protein ved bruk av bikinchoninsyre. Anal. Biochem. 150:76–85.Crossref, Medline, CAS, Google Scholar
- 4. Bradford, M. M. 1976. En rask og sensitiv metode for kvantifisering av mikrogram mengder protein utnytte prinsippet om protein-fargestoff binding. Anal. Biochem. 72:248–254.Crossref, Medline, CAS, Google Scholar
- 5. Zor, T. Og Z. Selinger. 1996. Linearisering Av Bradford – proteinanalysen øker følsomheten: teoretiske og eksperimentelle studier. Anal. Biochem. 236:302–308.Crossref, Medline, CAS, Google Scholar
- 6. Han er en av de eldste i verden. 1951. Proteinmåling med Folinfenolreagenset. J. Biol. Chem. 193:265–275.Medline, CAS, Google Scholar
- 7. Peterson, G. L. 1979. Gjennomgang av folin fenol protein kvantifisering metoden For Lowry, Rosebrough, Farr Og Randall. Anal. Biochem. 100:201–220.Crossref, Medline, CAS, Google Scholar
- 8. Sapan, C. V., R. L. Lundablad Og N. C. Price. 1999. Colorimetric protein assay teknikker. Bioteknologi. Appl. Biochem. 29:99–108.Medline, CAS, Google Scholar
- 9. Okutucu, B., A. Dıç,Ö Habib, Og F. Zıı 2007. Sammenligning av fem metoder for bestemmelse av total plasmaproteinkonsentrasjon. J. Biochem. Biophys. Metoder 70: 709-711.Crossref, Medline, CAS, Google Scholar
- 10. Kresge, N., R. D. Simoni Og R. L. Hill. 2005. Det mest siterte papiret i publiseringshistorien: proteinbestemmelse Av Oliver H. Lowry. J. Biol. Chem. 25:280.Google Scholar
- 11. Det er en av de mest kjente artene i verden. 2010. Grundig studie av reaktivitet av ulike sammensatte klasser mot Folin-Ciocalteu Reagens. J. Agric. Matkjem. 58:8139–8144.Crossref, Medline, CAS, Google Scholar
- 12. Eichberg, J. Og L. C. Mokrasch. 1969. Interferens ved oksiderte lipider ved bestemmelse av protein Ved Lowry-prosedyren. Anal. Biochem. 30:386–390.Crossref, Medline, CAS, Google Scholar
- 13. Dulley, J. R. Og P. A. Grieve. 1975. En enkel teknikk for å eliminere forstyrrelser av vaskemidler I Lowry – metoden for proteinbestemmelse. Anal. Biochem. 64:136–141.Crossref, Medline, CAS, Google Scholar
- 14. Brillouet, J.-M., M.-P. Belleville, Og M. Moutounet. 1991. Mulige protein-polysakkaridkomplekser i røde viner. Er. J. Enol. Vitic. 42:150–152.CAS, Google Scholar
- 15. Upreti, G. C., R. A. Ratcliff og P. C. Riches. 1988. Protein estimering i vev som inneholder høye nivåer av lipid: modifikasjoner Til Lowry metode for proteinbestemmelse. Anal. Biochem. 168:421–427.Crossref, Medline, CAS, Google Scholar
- 16. Upreti, G. C., C. Davis, Og J. Oliver. 1991. Fremstilling av representative homogenater av biologiske vev: effekt av salt på proteinutvinning. Anal. Biochem. 198:298–301.Crossref, Medline, CAS, Google Scholar
- 17. Han er en av de eldste i Verden. 2011. Kvantitativ Kolorimetrisk Analyse for Totalt Protein Påført Rødvin Pinot Noir. J. Agric. Matkjem. 59:6871–6876.Crossref, Medline, CAS, Google Scholar
- 18. Det er en av de mest kjente artene i verden. 2009. Analyse Av Proteinsammensetningen Av Rødvin I Sammenligning Med Rosé og Hvite Viner Ved Elektroforese og Høytrykks Væskekromatografi-Massespektrometri (HPLC-MS). J. Agric. Matkjem. 57:4328–4333.Crossref, Medline, CAS, Google Scholar
- 19. I tillegg til å være en del av det norske samfunnet, er det en del av det norske samfunnet. 2009. En stabil og sensitiv proteinanalyse (u-2009 modifisert analyse) for fargede biologiske prøver. ComBiol. New Zealands Siste Program Desember 2009. Universitetet I Canterbury, Christchurch, New Zealand.Google Scholar
- 20. Coakley, W. T. Og C. J. James. 1978. En enkel lineær transformasjon For Folin-Lowry proteinkalibreringskurven til 1,0 mg / mL. Anal. Biochem. 85:90–97.Crossref, Medline, CAS, Google Scholar
- 21. Pinheiro, J. C. Og D. M. Bates. 2000. Mixed-Effects Modeller I S OG S-PLUS, Statistikk Og Databehandling Serien. Springer-Verlag, New York, NY.Google Scholar
- 22. R Utvikling Kjerneteam. 2009. R: et språk og miljø for statistisk databehandling. R Foundation For Statistical Computing, Wien, Østerrike, ISBN 3-900051-07-0, URL http://www.R-project.org.Google Scholar
- 23. De fleste av disse er: Furrow. 1988. Væskekromatografiske gjenstander og toppforvrengning: Sample-solvent interaksjon i separasjon av karotenoider. Anal. Chem. 60:807–811.Crossref, Medline, CAS, Google Scholar
- 24. Cernik, A. A. 1970. Bestemmelse av bly chelatert med etylendiamintetraeddiksyre i blod etter utfelling av protein med perklorsyre. Brit. J. Industry Med. 27:40–42.Medline, CAS, Google Scholar
- 25. Det er en av de mest kjente artene i verden. 1990. Perklorsyre og trikloreddiksyre som utfellingsmidler av protein i endogen ileal digesta fra rotte. J. Sci. Mat Agric. 52:13–21.Crossref, CAS, Google Scholar
- 26. Galbá, Z. M. og L. J. Csá 1983. Alkali-indusert dekomponering av hydrogenperoksid. J. Chem. Soc. Dalton Trans. 11:2353–2357.Crossref, Google Scholar
- 27. Scopes, R. K. 1988. Proteinrensing: Prinsipper og Praksis, Andre Utg. Springer-Verlag New York Inc., New york, ny.Google Scholar
- 28. Det er også en del av det norske samfunnet. 1998. Studier på aromatisk aminosyreoksidaseaktivitet i ram spermatozoa: rolle av pyruvat som en antioksidant. Anim. Irettesettelse. Sci. 51:275–287.Crossref, Medline, CAS, Google Scholar
- 29. Holleman, M. A. F. 1904. Legg merke til l ‘action de l’ eau oxygenee sur les syrer α-cetoniques og les dicetones 1.2. Recl. Trav. Chim. Pays-Bas Belg. 23:169–172.Crossref, CAS, Google Scholar