著者:ブリット-ロング、MD(@long_brit、SAUSHEC EM主治医)とジャスティン-R-ワリックス、DO、FAAEM(EM主治医、セントラルペニンシュラ病院、Soldotna、AK)//編集:アレックス-Koyfman、MD(@EMHighAK、EM主治医、UT南西医療センター/パークランド記念病院)
今日、我々はいくつかの論争と最先端の治療法を見て、コアEMトピックに関するケースベースの議論を持っています。
—————————-
透析、高血圧、およびCADの腎臓病の歴史を持つ62歳の女性は悪心および弱さと示します。 今日の透析セッションを欠場しました。 彼女のVSは正常であり、彼女の試験も正常です。 あなたが得るあなたの最初のテストは何ですか?
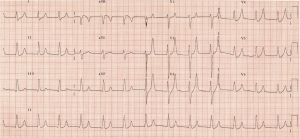
あなたはP波の不在と大きな、ピークのT波を参照してください。 VBGは7.3mmol/Lのカリウム、ナトリウム140mmol/Lおよび正常な乳酸塩と戻ります。 あなたの標準的な高カリウム血症の養生法、またはCの大きいKの低下を頼みます–https://canadiem.org/tiny-tip-hyperkalemia-management/
からの多くを見て下さいこの養生法はカルシウム(gluconateか塩化物の塩)、ベータアゴニスト(nebulized10-20mgのアルブテロール)および/または重炭酸塩(1amp)、インシュリン(10単位の規則的な/ブドウ糖D50 1amp)、Kayexalate(15-30gの口頭か直腸)、Diuretics(Furosemide40mg)、および腎臓の単位から古典的に成っています患者の透析のため。
このレジメンの背後にある文献は何ですか? 何か良いことはありますか?
始める前に、いくつかの基本をカバーしましょう。
–ほとんどのカリウムは細胞内(98%)であり、75%は骨格筋に見られる。 細胞内環境と細胞外環境との間の有意な勾配は、細胞活動電位の生成において重要な役割を果たす。1–5
-腎臓系はカリウムの調節(排泄の90%)において最も重要な役割を果たす。 正常なレベルは3.5-5.0mEq/Lまたはmmol/Lです。1,2
– これらのレベルの変化は細胞膜電位に影響を与え、心臓および神経筋症状をもたらす。 N a-K-Atpアーゼポンプは細胞膜勾配において大きな役割を果たす。
–軽度の高カリウム血症:5.5-6.5mEq/L(入院患者の10%に近い)。4–7
-中等度のレベルは6.5-7.5mEq/L、重度の>7.5mEq/Lである。4-7
病因:カリウム上昇の原因には次のものが含まれます: excessive exogenous potassium, excessive endogenous potassium (hemolysis, rhabdomyolysis, burns, tumor lysis syndrome, trauma), redistribution (acidemia, medications (succinylcholine, beta-blockers), and insulin deficiency), decrease in excretion (renal failure/injury, decreased mineral corticoids, medications), factitious (hemolysis, thrombocytosis, venipuncture issue, leukocytosis).5-8
Clinical Manifestations: Since potassium plays an important role in Na-K-ATPase physiology, hyperkalemia can result in several important effects, primarily cardiac and neuromuscular. しかし、臨床的特徴は非特異的であり、一般的な衰弱、嗜眠、または混乱を含む。 脳神経、横隔膜機能、および感覚は典型的には正常であるが、深部腱反射はうつ病または不在である可能性がある。 GIの効果は悪心、嘔吐および下痢を含んでいます。
-心電図は高カリウム血症における最も重要な診断検査の1つです。 予測された変化は、古典的に1)ピークT波、2)p波の損失を伴うPR間隔の延長、3)QRSの拡大、4)正弦波パターン、および6)収縮期に従うと考えられている。 ピークに達したT波は、休止中の膜電位変化の結果である。9–12
-これらの変更は順番に表示されません。 ダッジ他 発見された患者は洞調律からV fibに進行する可能性があります。13ECGは、高カリウム血症の予測において34-43%の感度を示し、特異性は85-86%である。12,14
–血清カリウムのゆっくりとした変化は心電図の変化をもたらさず、9.0mEq/Lを超えるレベルは期待される所見を示さない可能性がある。12,15
私たちの患者は衰弱と心電図の変化を示しました。 あなたはいくつかの薬を求めている、とのは、高カリウム血症の治療に私たちの深いダイビングを開始してみましょう。
管理
–治療は高カリウム血症の原因に依存せず、不整脈の影響や合併症を逆転または回避することに焦点を当てる必要があります。
–IVアクセス、継続的な監視、およびO2のセーフティネットを確立します。
–管理は、心臓の安定化、経細胞シフト、およびカリウム排泄に焦点を当てています。 これは、ECGの変化(ピークT波を含む)またはカリウム>6.5mmol/Lのいずれかによって、高カリウム血症が疑われると直ちに開始しなければならない。4,5,10,11,16

1) 心臓膜安定化
カルシウムは高カリウム血症の脱分極効果を低下させ、数分以内に心筋細胞の閾値電位を低下させる。4,5,17-19これは心臓細胞膜を安定させるが、他の薬物を必要とするカリウムの経細胞シフトまたは排泄をもたらさない。
–カルシウムは二つの形として与えることができます: 塩化物またはグルコン酸塩。 塩化Ca塩は13.6meqを10mL中に含み、グルコン酸Ca塩は4.6meqを10mL中に含む。4,5,18,19caグルコン酸塩は、末梢IVラインを介して与えることができます。 Caの塩化物のextravasationによりティッシュの壊死を引き起こすことができ中央線は可能であれば推薦されます(コード状態がなければ。)4,5
-CaCl1gには約270mgのCa2+が含まれていますが、3アンプルのグルコン酸カルシウムには当量(アンプルあたり約90mgのCa2+)が含まれています。18,19
–文献は、グルコン酸Caが塩化Caと同様の発症時間を有し、肝臓活性を必要としないことを示唆している。 肝臓移植を受けている患者で実施されたいくつかの研究は、いずれかの製剤の後にCaの同様の増加を示す。19-21犬および小児患者で実施された研究では、同様の所見が示されています。21
–作用の開始は3分未満で、持続時間は20-60分である。4,5
結論:1g(10mL)のグルコン酸Ca IVは、ECG所見(ピークT波または悪化)を有する患者に提供され、5分以内に再評価されるべきである。 ECGの変化や悪化が観察されない場合は、より多くのカルシウムを提供する必要があります。 心停止中または中枢アクセスを有する患者には、1gの塩化Ca IVを投与する必要があります。
心臓安定化のための別の選択肢はありますか? これは主に低ナトリウム血症と高カリウム血症の患者で研究されているが、高張生理食塩水(3%)は、100ミリリットルのボーラスで使用することができま22
2)経細胞シフト
これは、カリウムを再分配するために、カルシウムとともに、またはカルシウムの直後に起こるべきである。4,5,23-25

A)インシュリンおよびブドウ糖–これらの手段は線量の依存した方法の血清のカリウムを下げます。4,5,23-26Na-K-ATPaseの活性化と細胞膜への細胞内ポンプ動員(GLUT4受容体)は、細胞内K輸送の原因となっている。27
–古典的には、血糖値が250mg/dL未満の場合、通常のインスリン10-20単位が提供され、デキストロース25g(D50の1amp)が提供される。4,5,28,29
–インスリンとグルコースは15分以内にカリウムを0.45-0.61mmol/L、30-32 0減少させる。30分で87mmol/L、33、34および1時間で0.47mmol/L。23,24,33,34他の調査はそれが1.2mmol/L.まで減少で起因するかもしれないことを提案します。23,24
– インシュリン/ブドウ糖に行為の手始めがより少しにより15分(一般に5-10分)、および最高の行為の時間25-30分あります。23,24アクションの持続時間は2時間です。
–リスクには低血糖が含まれ、これはしばしば過小評価されます。 この率は規則的なインシュリンの8.7単位との10%に達します。35末期腎疾患患者の研究では13%の割合が示唆され、36は血液透析を受けている患者で75分で60%に達する。26系統的レビューは18%を示唆している。26
–提供すべきグルコースの量を決定することは困難であり、以下の表1は、提供すべきものを決定するための簡単な手段を提供する。
–要因には、以前の糖尿病の欠如、糖尿病薬の欠如、および治療前の低グルコースが含まれる。 腎臓の傷害か病気はインシュリンがrenally新陳代謝するので、潜在的な要因です。4,5,36
–潜在的な変化には、より短い半減期を有し、より迅速に吸収され、腎不全/傷害において延長されないlisproまたはaspartのような短時間作用型インスリン これは、10単位のみの短時間作用型インスリンボーラス、または6単位ボーラスに続いてlisproまたはaspartの1時間注入あたり20単位として提供することがで これらの養生法はより少ないhypoglycemiaに終って間、血清のカリウムの同じような減少を提供します。4,5
–グルコースのみは推奨されず、高カリウム血症や高カリウム血症を引き起こす可能性があります。37,38
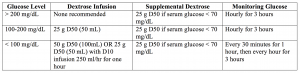
要点:上でようにブドウ糖の注入を用いる短い代理のインシュリン10単位IV。

B)Βアゴニスト-カテコールアミンは、Na-K-ATPaseポンプおよびNa-K-2cl cotransporterの活性を増加させる。1-5,39,40
– ネブライズされたアルブテロールは、閉塞性疾患のための通常の5mgではなく、10-20mgの用量で与えられる。
–レバルブテロールとアルブテロールは、カリウムを減少させる同等の能力を示す。4,5,23,24
-アルブテロールは0.50mgの線量のIVを与え、terbutalineは0.25mgの線量のIMを与えることができます。 4,5,23,24,31,41-43
– カリウムは0.6ミリモル/Lで10mg、1.0ミリモル/Lで20mgで一時間減少する。31,41-43
– 発症は20-30分であり、持続時間は二時間以上である。31,41-43
– IV製剤には、エピネフリン、アルブテロール0.5mg、またはサルブタモール2.5mgが含まれるが、副作用がより一般的である。23,24,34
–副作用には振戦、動悸、不安が含まれます。 IV型は、血圧や頭痛のリスクが高くなります。
-インスリンとグルコースとの併用治療は、カリウムのより大きな減少をもたらす、1。薬物の管理の後の1時間の2-1.5mmol/L。31,41-43
ボトムライン:アルブテロール20mg4mLの通常の生理食塩水に10分にわたって噴霧した。

C)重炭酸ナトリウム–ボーラス重炭酸ナトリウムは、長期の重炭酸塩注入(時間以上)を評価する研究に基づいて、高カリウム血症の急性治療に推奨されて23,24,31,32,44-46
– しかし、正常なpHを有する患者の文献は、高カリウム血症の重炭酸塩を支持しない。4,5,23,24
–他の薬剤と比較した場合、重炭酸塩は30分および60分でカリウムの有意な減少をもたらさない。23,24,32いくつかの制御された研究は、重炭酸ナトリウムが60分以内にカリウムを減少させないことを示している。4,5,23,24研究は、時間をかけて注入重炭酸塩を利用した減少を示唆しています(むしろボーラスよりも)そして酸性血症の患者で.47,48
併用治療
–複数の薬剤を使用することで、カリウム再分配の最良の手段が提供され、コクランレビューではインスリン、グルコース、ベータアゴニストの併用が推奨されている。4,5,23-26
– Allon et al. nebulized albuterolのIVインシュリンのブドウ糖との1.21mmol/Lカリウムの最高の減少を見つけます。31
–重炭酸塩は、患者が酸血症でない限り使用すべきではありません。4,5
結論:重炭酸ナトリウムは、酸性血症および高カリウム血症の患者に使用することができるが、他の患者には有用ではない。 併用療法はβアゴニストとインスリン/グルコースとの併用療法が有効である。
患者のグルコースは153である。 あなたはグルコン酸カルシウムを与えます10%10ML IV,続いて10一つのアンプD50と20mgのアルブテロールnebulizedと単位短時間作用型インスリン. あなたの次のステップは何ですか?
3)カリウム排泄
排泄手段には、尿、GI系、血液が含まれる。1-5腎臓は排泄の支配的な経路である。 医師は、患者の容積状態および尿を産生する能力を評価すべきである。 患者が尿を産生することができれば、利尿薬が有効な選択肢である。4,5しかし、血液透析は、決定的なカリウム除去の最良の手段です。

A)尿中利尿-これは、血液透析のために患者を準備している間に使用することができます。 尿中利尿は、患者が尿を産生できない場合には有用ではないが、適度に腎機能が低下した患者には有用である可能性がある。4,5
–フロセミドなどのループ利尿薬は、カリウムの最大の尿中排泄を提供します。
-アセタゾラミドとの併用はカリウム排泄をさらに増加させる可能性がありますが、本剤単独では推奨されません。49
–これらの薬剤は、高volemiaまたはeuvolemiaの患者に最も適しています。 提供されれば、医者は注意深く尿の出力および電解物を監視するべきです。
–血液量が減少した場合は、IV液を提供する必要があります。 この投稿では、どちらが最適かは評価されませんが、文献では、乳酸リンガーまたは血漿が通常の生理食塩水よりも優れていることが示唆されています。 詳細については、PulmCritのJosh Farkasからのこの投稿を参照してください:https://emcrit.org/pulmcrit/myth-busting-lactated-ringers-is-safe-in-hyperkalemia-and-is-superior-to-ns/。

B)GI–複数の選択はKayexalateよりよい選択を提供していて複数の新しい代理店が利用できます。
–ポリスチレンスルホン酸ナトリウム(sps)、またはKayexalateは、ナトリウムをアンモニウム、カルシウム、マグネシウム、カリウムと交換して糞便を介してカリウムを除去するイオン交換樹脂である。4,5,23-26残念なことに、SPSの背後にある文献は非常に弱く、最近の研究とコクランのレビューはその使用に対して推奨しています。50,51この薬は、便秘、閉塞、さらに悪いことに、腸の虚血および壊死のリスクに患者を配置しながら、ナトリウム負荷を提供します。 薬物はFDAからのブラックボックスの警告を所有しています。4,5,23,24,52詳細については、http://www.emdocs.net/skeptical-em-myths-evidence/を参照してください。http://rebelem.com/kayexalate-useful-treatment-hyperkalemia-emergency-department/
– Patiromerはnonabsorbable球形のビードから成っている総合的なポリマーです。52,53薬の作用の開始は7-48時間であり、効果の持続時間は12-24時間である。 52-54健康なボランティアは15-20ミリモルによってカリウムの線量関連の減少を示す。15-30g/dayの55-57の線量は有効ようです。 最も一般的な副作用には低マグネシウム血症(8.6%)が含まれますが、心臓不整脈はこれらの患者には見られませんでした。 ノートの、薬物は他の口頭薬物からの少なくとも6時間の分離のためのブラックボックスの警告を所有しています。4
-ジルコニウムシクロケイ酸ナトリウム(ZS-9)は、吸収性のない球状ビーズからなる合成ポリマーである。53,54結晶構造内の一つの結合孔がカリウムに特異的に結合するので、薬物はspsと比較してカリウムの量の九倍以上に結合する。143,149ZS-9の作用開始は1-6時間であり、効果の持続時間は4-12時間である。 いくつかの研究では、10g/日のカリウムを1時間で0.4mmol/L、4時間で0.7mmol/L減少させて、その使用を支持している。58–60
-patiromerとZS-9を比較したメタ分析では、patiromerは治療3日目までにカリウムを0.36mEq/L減少させることが分かった。61ZS-9は、一時間で0.17mEq/L、2日で0.67mEq/Lの減少を示しています。61

C)透析-これはカリウムを除去する最も効果的な方法であり、カリウムは1時間で1mmol/L、2-3時間で2mmol/L減少する。 より低いカリウムの透析液および高められた血の流れはより速い血清のカリウムの減少で起因できます。4,5
–機械の血液ポンプ速度と血漿から透析液への濃度の増加は、数分以内にカリウムを減少させる可能性があるため、透析の重要性(特に心停止)。4,5,41
–透析後にリバウンド高カリウム血症が見られることがあり、透析前のカリウムレベルに関連している可能性が高い。4,5
–腎不全、尿を産生できない、他の治療に抵抗性の高カリウム血症、心停止、著しい組織破壊と診断された患者の早期に血液透析を考慮すべきである。62-64
: 透析は決定的なカリウム除去に最も有効である。 SPSは有効ではなく、結腸壊死の危険性のために避けるべきである。
あなたは透析に関する腎臓科医に電話し、ECGを繰り返し、速度72bpmで正常な洞調律を示します。 Nephrologistは彼女が患者を見るために右の下にあることを示す。
高カリウム血症による心停止はどうなりますか?
高カリウム血症は心筋細胞の安静電位を変化させ、ナトリウムチャネルの不活性化および伝導を遮断する。 高カリウム血症のために逮捕された患者は、即時の圧迫およびACLS措置を必要とする。28,29
–既知の腎不全、重大な病気、または血液透析の病歴を有する心停止患者は、カリウムを測定する迅速な血液ガス評価を保証する。
–病因としての高カリウム血症の疑いは、塩化カルシウム10%(1ampまたは10mL)を必要とし、qrs<100msまで、末梢IVまたは中央線を介して繰り返し投与する。28,29
–インスリンとグルコースと同様に、エピネフリンを提供する必要があります。
–重炭酸ナトリウムは1ampとして提供することができます。
–高カリウム血症がVBGまたは他の実験室試験で確認されると、血液透析が不可欠です。
–ROSCは塩化カルシウム膜安定化後に発生することがあり、これは20-30分間持続する。 この時点で、細胞内のシフトと排除が目標です。4,5,28,29,65
キーポイント
–カリウムは生理学において重要な役割を果たし、主に細胞内に見出される。 高カリウム血症は、主に心臓および神経筋細胞における細胞膜電位の変化をもたらす。
–心電図は最初の必須検査であるが、所見の欠如は高カリウム血症を除外するためには信頼できない。
–管理には、心臓膜安定化、経細胞シフト、および排泄が含まれる。
–グルコン酸カルシウム10%は、患者が心停止していない限り、膜安定化のために与えることができ、10mLの塩化カルシウムを与えるべきである。
–βアゴニストとグルコースとの短時間作用型インスリンは、カリウムを細胞内にシフトさせるのに有効である。 右旋糖の注入は血清のブドウ糖に基づいて提供されるべきです。
–重炭酸ナトリウムは、患者が酸血症でない限り推奨されない。
-排泄には尿中利尿、消化管除去、血液透析が含まれる。
–SPSまたはkayexalateは推奨されません。 Patiromerおよびナトリウムのジルコニウムのcyclosilicateを含む新しい薬物はGIの排泄物のための約束を保持します。
–透析はカリウムを除去する究極の手段です。 乳酸リンガーとPlasmalyteは、必要に応じて流体の再水和のために安全かもしれません。
参考文献/続きを読む:
- ファリディABワイズベルグLS 酸-塩基、電解質および代謝異常。 で:クリティカルケア医学:成人における診断と管理の原則。 パリーロJE,デリンジャー RP(Eds). 第三版。 Philadelphia,Elsevier,2008;1203-1243.
- マウントDB,Zandi-Nejad K.カリウムバランスの障害. In:Brenner and Rector’s The Kidney,9th Ed,WB Saunders&Company,Philadelphia2011. 640頁
- ブラウン カリウムの恒常性および臨床含意。 Am J Med.1984年11月5日;77(5A):3-10。
- 腎臓国際2016;89:546-554.
- ヴァイスベルクLS. 重度の高カリウム血症の管理。 クリティカルケアMed. 2008;36(12):3246-51.
- Gennari FJ:カリウム恒常性の障害。 低カリウム血症および高カリウム血症。 クリットケアクリン2002;18:273-288
- スティーブンスさん、ダンレイさん、 入院患者の高カリウム血症。 Int Urol Nephrol2000;32:177-180.
- 低カリウム血症および高カリウム血症。 メド-クリン-ノース-アム… 1997;81(3):611-639.
- Fisch C.電解質障害と心臓不整脈の関係。 循環1973;47:408-419。
- Surawicz B.電解質と心電図。 1974年(昭和55年)に卒業した。:123–129.
- Freeman K,Feldman JA,Mitchell P,et al. 高カリウム血症の治療までの時間に対する提示および心電図の影響。 Academmed. 2008Mar;15(3):239-49.
- Mattu A,Brady WJ,Robinson D.高カリウム血症の心電図症状。 Am J Emerg Med. 2000; 18: 721–729.
- ダッジHT、グラントRP、Seavey PW。 正常および異常な心電図に対する誘発高カリウム血症の効果。 Am Heart J.1953May;45(5):725-40.
- レンヌKD,Slovis CM,Slovis BS. 医師がECGから高カリウム血症を予測する能力。 アン-エメリッヒ-メド… 1 9 9 1Nov;2 0(1 1):1 2 2 9−3 2.
- Szerlip HM,Weiss J,Singer I.心電図症状のない深遠な高カリウム血症。 アム-ジェイ-ディ-ディ… 1986Jun;7(6):461-5.
- モンタギュー BT、ウエレットJR、ブラー GK。 高カリウム血症におけるECG変化の頻度の遡及的レビュー。 腎臓のアメリカの社会の臨床ジャーナル:CJASN。 2008;3(2):324-330.
- チェンバレンM.高カリウム血症の緊急治療。 ランセット 1964;1:464–467.
- Bisogno JL,Langley A,Von Dreele MM. 単離されたラット心臓における高カリウム血症の心電図効果を逆転させるためのカルシウムの効果:前向き、用量応答研究。 Crit Care Med1994;22:697-704.
- Martin T,Kang Y,Robertson K,et al. 肝機能の非存在下での塩化カルシウムおよびグルコン酸カルシウムのイオン化および血行力学的効果。 麻酔1 9 9 0;7 3:6 2−5.
- Davey M,Caldicott D.高カリウム血症の管理におけるカルシウム塩。 救急医療ジャーナル:EMJ。 2002;19(1):92-93.
- Cote CJ,Drop LJ,Daniels AL,et al. 塩化カルシウム対グルコン酸カルシウム: 子供および犬のイオン化および心血管の効果の比較。 麻酔学1987;66:465-70。
- Ballantyne F III,Davis LD,Reynolds Ew Jr,et al. ナトリウムによる高カリウム血性心電図変化の逆転のための細胞基礎。 Am J Physiol1975;229:935-940。
- Batterink J,Cessford TA,Taylor RAI. 成人における高カリウム血症の急性管理のための薬理学的介入。 2015年、第10号の『Cochrane Database Of Systematic Reviews』に掲載された。 アート。 いいえ。.:CD010344. DOI:10.1002/14651858.CD010344.pub2.
- Mahoney BA,Smith WA,Lo DS,et al. 高カリウム血症のための緊急介入。 Cochrane Database Syst Rev.2005Apr18;(2):CD003235.
- Elliott MJ,Ronksley PE,Clase CM,et al. 急性高カリウム血症患者の管理。 2010;182:1631–1635.
- ハレルZ、カメルKS。 緊急高カリウム血症の管理における静脈内インスリンの最適用量および投与方法:系統的レビュー。 Barretti p,ed. プロスワン 2016;11(5):e0154963.
- Ho K.a非常に迅速な応答:骨格筋におけるインスリン刺激カリウムおよびグルコース輸送。 Clin J Am Soc Nephrol. 2011;6:1513–1516.
- Soar J,Perkins GD,Abbas G,et al. 欧州蘇生協議会の蘇生ガイドライン2010セクション8。 特別な状況での心停止:電解質異常、中毒、溺死、偶発的な低体温、温熱療法、喘息、アナフィラキシー、心臓手術、外傷、妊娠、感電。 蘇生… 2010;81:1400–1433.
- Vanden Hoek TL,Morrison LJ,Shuster M,et al. パート12:特別な状況での心停止:2010年アメリカ心臓協会心肺蘇生と緊急心血管ケアのためのガイドライン。 循環。 2010;122(suppl3):S829-S861.
- 李Q、周MT、王Y、et al. 肝移植の無肝期における高カリウム血症に対するインスリンの影響。 2004年10月24日27時9分に行われた世界ジュニア選手権では準決勝で敗退した。
- allon M,Copkney C.Albuterol and insulin for treatment of hyperkalemia in hemodialysis patients. Kidney Int1 9 9 0;3 8(5):8 6 9−7 2。
- Allon M,Shanklin N.透析患者における血漿カリウムに対する重炭酸塩投与の効果:インスリンおよびアルブテロールとの相互作用。 Am J腎臓Dis1996;28:508-14.
- マハジャンSK,マングラM,キショレK. 末期腎疾患における高カリウム血症の急性治療におけるアミノフィリンおよびインスリン–デキストロース注入の比較J Assoc Physicians India2001;49:1082-5.
- ヌギNN,McLigeyo SO,Kayima JK. 腎不全患者における経細胞勾配を変化させることによる高カリウム血症の治療:様々な治療の効果East Afr Med J1997;74:503-9。
- Schafers S,Naunheim R,Vijayan A,et al. 高カリウム血症の処置のインシュリンベースの激しい安定に続くhypoglycemiaの発生。 J-Hosp Med. 2012;7(3):239-242.
- アペルJ,ロイトラクルS,ボールドウィンD. 末期腎疾患の患者におけるインスリンによる高カリウム血症の治療における低血糖。 Clin腎臓J.2014;7(3):248-250.
- Goldfarb S,Cox M,Singer I,et al. 高血糖によって誘発される急性高カリウム血症:ホルモンメカニズム。 アン-インターンMed. 1976;84:426–432.
- パーマー BF. カリウム恒常性の調節。 Clin J Am Soc Nephrol. 2015;10:1050–1060.
- 骨格筋におけるNa、Kポンプの調節。 腎臓Int1989;35:1-13。
- モラティノスJ,Reverte M.血漿カリウムに対するカテコールアミンの影響: α-およびβ-アドレナリン受容体の役割。 ファンダムクリンファルコール。 1993;7(3-4):143-53.
- 末期腎疾患におけるアロンM.高カリウム血症:メカニズムと管理。 J Am Soc Nephrol1995;6:1134.
- Allon M,Dunlay R,Copkney C.血液透析患者における急性高カリウム血症のためのネブライズされたアルブテロール。 アン-インターンMed. 1989;110:426-9.
- Allon M,Shanklin N.その後の透析カリウム除去に対するアルブテロール処理の効果。 Am J腎臓Dis1995;26:607-13.
- Blumberg A,Weidmann P,Shaw S,et al. 末期腎不全における血漿カリウムおよび主要な調節因子に対する様々な治療アプローチの効果。 医学のアメリカのジャーナル。 1988;85(4):507–12.
- イクバルZ、フリードマンEA。 腎不全における高カリウム血症のPreferredtherapy:腎臓学の訓練プログラムN Engl J Medの調査. 1989Jan5;320(1):60-1.
- Blumberg A,Weidmann P,Ferrari P.末期腎不全における血漿カリウムに対する重炭酸塩の長期投与の影響。 腎臓Int. 1992;41:369–374.
- Fraley DS,Adler S. 一定の血液pHにもかかわらず、重炭酸塩による高カリウム血症の補正.腎臓Int. 1977年11月;12(5):354-60。
- Gutierrez R,Schlessinger F,Oster JR,et al. 末期腎疾患患者における血漿カリウム濃度に対する高張性対等張性重炭酸ナトリウムの影響。 鉱夫の電解物Metab。 1991;17(5):297-302.
- Jentzer JC,DeWald TA,Hernandez AF. 心不全におけるループ利尿薬とチアジド型利尿薬の組み合わせ。 J-Am-Coll. 2010Nov2;56(19):1527-34.
- Scherr L,Ogden DA,Mead AW,et al. 陽イオン交換樹脂による高カリウム血症の管理。 N Engl J Med1961;264:115-119.
- Flinn RB,Merrill JP,Welzant WR,et al. 新しいナトリウム交換樹脂とソルビトールによるオリグ尿患者の治療;予備報告。 N Engl J Med. 1961年1月19日;264:111-5。
- Sterns RH,Rojas M,Bernstein P,et al. 高カリウム血症の治療のためのイオン交換樹脂:それらは安全で効果的ですか? J-Am-Soc所属。 2010月;21(5):733-5.
- ベッカリMV,Meaney CJ. 高カリウム血症の治療のためのpatiromer、ジルコニウムcyclosilicateナトリウム、およびポリスチレンスルホン酸ナトリウムの臨床的有用性:エビデンスベースのレビュー。 コア証拠。 2017;12:11-24.
- Weir MA,Juurlink DN,Gomes T,et al. Β遮断薬、トリメトプリムスルファメトキサゾール、および高齢者の入院を必要とする高カリウム血症のリスク:ネストされた症例対照研究。 Clin J Am Soc Nephrol. 2010;5:1544–1551.
- Huang I.RLY5016:血清カリウム制御のための新規で吸収されない治療用ポリマー。 J-Am-Soc所属。 2010;21:482A–483A.
- Bakris GL,Pitt B,Weir MR,ET al,AMETHYST-DN研究者のための. 高カリウム血症および糖尿病性腎疾患患者における血清カリウムレベルに対するpatiromerの効果:AMETHYST-DNランダム化臨床試験。 ジャマ 2015;314:151–161.
- Montaperto AG,Gandhi MA,Gashlin LZ,et al. Patiromer:臨床レビュー。 Curr Med Res Opin. 2016;32(1):155-64.
- Packham DK,Kosiborod M.高カリウム血症の治療におけるジルコニウムシクロケイ酸ナトリウムの薬力学および薬物動態。 専門家のOpinの薬剤MetabのToxicol。 2016年5月;12(5):567-73.
- Ash SR,Singh B,Lavin PT,et al. 慢性腎臓病患者における高カリウム血症の治療に関する第2相試験は、選択的カリウムトラップZS-9が安全で効率的であることを示唆している。 腎臓Int. 2015;88:404–411.
- Packham DK,Rasmussen HS,Lavin PT,et al. 高カリウム血症にはシクロケイ酸ジルコニウムナトリウムがある。 N Engl J Med. 2015;372:222–231.
- Meaney CJ,Beccari MV,Yang Y,et al. PatiromerおよびナトリウムのジルコニウムのCyclosilicateの系統検討そしてメタアナリシス:高カリウム血症の処置のための新しいArmamentarium。 2017Apr;37(4):401-411.
- Blumberg A,Roser HW,Zehnder C,et al. 血液透析中および透析後の末期腎不全患者における血漿カリウム;透析カリウム除去および全身カリウムとの関係。 ネフローレンダイヤル移植。 1997;12:1629–1634.
- Feig P,Shook A,Sterns R.血液透析中のカリウム除去が血漿カリウム濃度に及ぼす影響。 ネフロン 1981;27:25–30.
- Agar BU,Culleton BF,Fluck R,Leypoldt JK. 血液透析中のカリウム動態。 血液型はA型。 2015;19:23–32.
- Alfonzo AV, Simpson K, Deighan C, Campbell S, Fox J. Modifications to advanced life support in renal failure. Resuscitation 2007;73:12–28.