Auteurs: Brit Long, MD (@long_brit, Médecin traitant de SAUSHEC EM) et Justin R. Warix, DO, FAAEM (Médecin traitant de ME, Hôpital Central Peninsula, Soldotna, AK) // Édité par: Alex Koyfman, MD (@EMHighAK, Médecin traitant de ME, UT Southwestern Medical Centre / Hôpital commémoratif Parkland)
Bienvenue aux cas emDocs! Aujourd’hui, nous avons une discussion basée sur des cas sur un sujet clé de la GU, avec un aperçu de certaines controverses et des traitements de pointe.
—————————-
Une femme de 62 ans ayant des antécédents de maladie rénale sous dialyse, d’hypertension et de CAD présente des nausées et une faiblesse. Elle a raté la séance de dialyse d’aujourd’hui. Son VS est normal, et son examen est également normal. Quel est votre premier test que vous obtenez?
- L’ECG!
- Quelle est la littérature derrière ce régime? Y a-t-il quelque chose de mieux?
- Avant de commencer, abordons quelques notions de base.
- Prise en charge
- 1) Stabilisation de la membrane cardiaque
- 2) Déplacement transcellulaire
- Traitement combiné
- 3) Excrétion de potassium
- Que se passe-t-il en cas d’arrêt cardiaque dû à une hyperkaliémie?
- Points clés
- Références / Lectures complémentaires:
L’ECG!
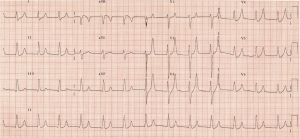
Vous voyez de grandes ondes T pointues avec absence d’ondes P. Le VBG revient avec du potassium de 7,3 mmol/L, du sodium de 140 mmol/L et du lactate normal. Vous demandez votre régime standard d’hyperkaliémie, ou C BIG K DROP – voir plus de https://canadiem.org/tiny-tip-hyperkalemia-management/
Ce régime se compose classiquement de calcium (gluconate ou sel de chlorure), de bêta-agoniste (10-20 mg d’albutérol nébulisé) et / ou de bicarbonate (1 amp), d’insuline (10 unités régulières / Glucose D50 1 amp), de Kayexalate (15-30 g par voie orale ou rectale), de Diurétiques (Furosémide 40 mg) et d’unité rénale pour La dialyse Du Patient.
Quelle est la littérature derrière ce régime? Y a-t-il quelque chose de mieux?
Avant de commencer, abordons quelques notions de base.
– Les changements de ces niveaux affectent les potentiels membranaires cellulaires et entraînent des symptômes cardiaques et neuromusculaires. La pompe Na-K-ATPase joue un rôle important dans le gradient de la membrane cellulaire.
– Hyperkaliémie légère: 5,5-6,5 mEq / L (près de 10% des patients admis).4-7
Étiologie: Les causes de l’élévation du potassium comprennent: excessive exogenous potassium, excessive endogenous potassium (hemolysis, rhabdomyolysis, burns, tumor lysis syndrome, trauma), redistribution (acidemia, medications (succinylcholine, beta-blockers), and insulin deficiency), decrease in excretion (renal failure/injury, decreased mineral corticoids, medications), factitious (hemolysis, thrombocytosis, venipuncture issue, leukocytosis).5-8
Clinical Manifestations: Since potassium plays an important role in Na-K-ATPase physiology, hyperkalemia can result in several important effects, primarily cardiac and neuromuscular. Cependant, les caractéristiques cliniques ne sont pas spécifiques et comprennent une faiblesse générale, une léthargie ou une confusion. Les réflexes tendineux profonds peuvent être déprimés ou absents, bien que les nerfs crâniens, la fonction du diaphragme et la sensation soient généralement normaux. Les effets gastro-intestinaux comprennent des nausées, des vomissements et de la diarrhée.
– L’ECG est l’un des tests diagnostiques les plus importants dans l’hyperkaliémie. On pense classiquement que les changements prévus suivent 1) Les ondes T culminées, 2) l’allongement de l’intervalle PR avec perte de l’onde p, 3) l’élargissement du QRS, 4) le motif de l’onde sinusoïdale et 6) l’asystole. Les ondes T pointues sont le résultat de changements potentiels de la membrane au repos.9-12
– Ces modifications n’apparaissent cependant pas dans l’ordre. Dodge et coll. les patients trouvés peuvent évoluer du rythme sinusal à la fibrose V.13 ECG montre une sensibilité de 34 à 43% pour prédire l’hyperkaliémie, avec une spécificité de 85 à 86%.12,14
Notre patient présentait une faiblesse et des modifications de l’ECG. Vous avez demandé plusieurs médicaments, et commençons notre plongée profonde dans le traitement de l’hyperkaliémie.
Prise en charge

1) Stabilisation de la membrane cardiaque
Le calcium diminue l’effet de dépolarisation de l’hyperkaliémie et réduit le potentiel seuil des myocytes cardiaques en quelques minutes.4,5,17-19 Cela stabilise la membrane cellulaire cardiaque, mais cela n’entraîne pas de déplacement transcellulaire ni d’excrétion de potassium, ce qui nécessite d’autres médicaments.
– Le calcium peut être administré sous deux formes: sel de chlorure ou de gluconate. Le sel de chlorure de Ca contient 13,6 meq dans 10 mL, tandis que le sel de gluconate de Ca contient 4,6 meq dans 10 mL.Le gluconate de 4,5,18,19 Ca peut être administré par une ligne IV périphérique. L’extravasation du chlorure de Ca peut provoquer une nécrose tissulaire, et la ligne centrale est recommandée si possible (sauf situation de code.) 4,5
– CaCl 1 g contient environ 270 mg de Ca2+, tandis que 3 ampoules de gluconate de calcium en contiennent la quantité équivalente (environ 90 mg de Ca2+ par ampoule).18,19
Conclusion: 1g (10 mL) de gluconate de Ca IV doit être administré aux patients présentant des résultats d’ECG (ondes T culminantes ou pires), avec réévaluation dans les 5 minutes. Plus de calcium doit être fourni si aucun changement ou aggravation de l’ECG n’est observé. Un patient en arrêt cardiaque ou avec accès central doit recevoir 1 g de chlorure de Ca IV.
Existe-t-il une autre option pour la stabilisation cardiaque? Une solution saline hypertonique (3%) peut être utilisée dans des bolus de 100 ml, bien que cela ait été principalement étudié chez des patients atteints d’hyponatrémie et d’hyperkaliémie.22
2) Déplacement transcellulaire
Ceci doit se produire avec ou immédiatement après le calcium afin de redistribuer le potassium.4,5,23-25

A) Insuline et Glucose – Ces mesures réduisent la kaliémie de manière dose-dépendante.4,5,23-26 L’activation de la Na-K-ATPase et le recrutement de la pompe intracellulaire (récepteurs GLUT4) dans la membrane cellulaire sont responsables du transport de K intracellulaire.27
– Classiquement, une insuline régulière de 10 à 20 unités est fournie, avec 25 g de dextrose (un amp de D50) si la glycémie est inférieure à 250 mg / dL.4,5,28,29
– Le début de l’action de l’insuline / glucose est inférieur à 15 minutes (plus communément 5 à 10 minutes) et le temps d’action maximal est de 25 à 30 minutes.23,24 La durée d’action est de 2 heures.
– Les facteurs incluent l’absence de diabète antérieur, l’absence de médicaments pour diabétiques et une glycémie inférieure avant le traitement. Une lésion ou une maladie rénale est un facteur potentiel, car l’insuline est métabolisée par voie rénale.4,5,36
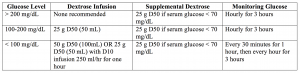
Bottom Line: Insuline à courte durée d’action 10 unités IV, avec perfusion de glucose comme ci-dessus.

B) Les bêta–agonistes-Catécholamines augmentent l’activité de la pompe Na-K-ATPase et du cotransporteur Na-K-2Cl.1-5,39,40
– L’albutérol nébulisé est administré à des doses de 10 à 20 mg, plutôt que les 5 mg normaux pour les maladies obstructives.
– Le lévalbutérol et l’albutérol démontrent une capacité égale à diminuer le potassium.4,5,23,24
– Albutérol peut être administré par voie intraveineuse à des doses de 0,50 mg et la terbutaline peut être administrée par voie IM à des doses de 0,25 mg. 4,5,23,24,31,41-43
– Le potassium diminue de 0,6 mmol / L avec 10 mg et de 1,0 mmol / L avec 20 mg en une heure.31,41-43
– Le début est de 20 à 30 minutes, avec une durée de plus de deux heures.31,41-43
– Les formulations IV comprennent l’épinéphrine, l’albutérol 0,5 mg ou le salbutamol 2,5 mg, bien que les effets secondaires soient plus fréquents.23,24,34
Conclusion: Albutérol 20 mg dans 4 mL de solution saline normale nébulisée en 10 minutes.

C) Bicarbonate de sodium – Bolus le bicarbonate de sodium a été recommandé pour le traitement aigu de l’hyperkaliémie, sur la base d’études évaluant la perfusion prolongée de bicarbonate (sur plusieurs heures).23,24,31,32,44-46
– Cependant, la littérature chez les patients ayant un pH normal ne soutient pas le bicarbonate pour l’hyperkaliémie.4,5,23,24
Traitement combiné
– Allon et coll. trouve une diminution maximale du potassium de 1,21 mmol / L avec l’insuline glucose IV avec l’albutérol nébulisé.31
Conclusion: Le bicarbonate de sodium peut être utilisé chez les patients présentant une acidémie et une hyperkaliémie, mais n’est pas utile chez d’autres patients. La thérapie combinée est efficace avec un bêta-agoniste et de l’insuline / glucose dans le potassium changeant.
Le glucose du patient est de 153. Vous donnez du gluconate de calcium 10% 10 mL IV, suivi de 10 unités d’insuline à action courte avec un amp D50 et 20 mg d’albutérol nébulisé. Quelle est votre prochaine étape ?
3) Excrétion de potassium
Les moyens d’excrétion comprennent l’urine, le système gastro-intestinal et le sang.1-5 Reins sont la voie d’excrétion prédominante. Les médecins doivent évaluer l’état du volume du patient et sa capacité à produire de l’urine. Si le patient peut produire de l’urine, un diurétique est une option valable.4,5 Cependant, l’hémodialyse est le meilleur moyen d’éliminer définitivement le potassium.

A) Diurèse urinaire – Cela peut être utilisé lors de la préparation du patient à l’hémodialyse. La diurèse urinaire n’est pas utile si le patient ne peut pas produire d’urine, bien qu’elle puisse être utile chez les patients présentant une fonction rénale modérément compromise.4,5
– Les diurétiques de l’anse tels que le furosémide fournissent la plus grande excrétion urinaire de potassium.
– Ces agents sont les meilleurs chez les patients atteints d’hypervolémie ou d’euvolémie. S’il est fourni, les médecins doivent surveiller attentivement le débit urinaire et les électrolytes.

B) GI – Plusieurs options sont disponibles, plusieurs nouveaux agents offrant de meilleures options que Kayexalate.
– Le polystyrène sulfonate de sodium (SPS), ou Kayexalate, est une résine échangeuse d’ions qui échange du sodium contre de l’ammonium, du calcium, du magnésium et du potassium pour permettre l’élimination du potassium par les fèces.4,5,23-26 Malheureusement, la littérature derrière le SPS est extrêmement faible, des études récentes et des revues Cochrane recommandant son utilisation.50,51 Ce médicament fournit une charge de sodium tout en exposant le patient à un risque de constipation, d’obstruction et, pire encore, d’ischémie et de nécrose intestinales. Le médicament possède même un avertissement de boîte noire de la FDA.4,5,23,24,52 Pour plus, voir http://www.emdocs.net/skeptical-em-myths-evidence/ et http://rebelem.com/kayexalate-useful-treatment-hyperkalemia-emergency-department/
– Le Patiromer est un polymère synthétique constitué de billes sphériques non absorbables.52,53 Le début d’action du médicament est de 7 à 48 heures, avec une durée d’effet de 12 à 24 heures. 52 à 54 volontaires sains présentent une diminution du potassium liée à la dose de 15 à 20 mmol.55-57 doses de 15-30g / jour semblent efficaces. L’effet indésirable le plus fréquent est l’hypomagnésémie (8,6%), bien qu’aucune dysrythmie cardiaque n’ait été détectée chez ces patients. Il est à noter que le médicament possède un avertissement de boîte noire pour une séparation d’au moins six heures des autres médicaments par voie orale.4

C) Dialyse – C’est le moyen le plus efficace d’éliminer le potassium, le potassium diminuant de 1 mmol / L à 1 heure et de 2 mmol / L à 2-3 heures. Une diminution du dialysat de potassium et une augmentation du flux sanguin peuvent entraîner une diminution plus rapide du potassium sérique.4,5
– Une hyperkaliémie de rebond peut être observée après la dialyse, probablement liée aux taux de potassium prédialysés.4,5
Résultat net: La dialyse est la plus efficace pour éliminer définitivement le potassium. Le SPS n’est pas efficace et doit être évité en raison de son risque de nécrose colique.
Vous appelez le néphrologue concernant la dialyse et répétez un ECG, qui démontre un rythme sinusal normal avec un taux de 72 bpm. La néphrologue déclare qu’elle sera juste en bas pour voir le patient.
Que se passe-t-il en cas d’arrêt cardiaque dû à une hyperkaliémie?
L’hyperkaliémie modifie le potentiel de repos des cardiomyocytes, entraînant l’inactivation des canaux sodiques et bloquant la conduction. Les patients en arrêt dû à une hyperkaliémie nécessitent des compressions immédiates et des mesures de LCA.28,29
– Les patients en arrêt cardiaque ayant des antécédents connus d’insuffisance rénale, de maladie grave ou sous hémodialyse justifient une évaluation rapide des gaz sanguins mesurant le potassium.
– Le ROSC peut survenir après une stabilisation de la membrane du chlorure de calcium, qui dure 20 à 30 minutes. À ce stade, le déplacement intracellulaire et l’élimination sont des objectifs.4,5,28,29,65
Points clés
– L’ECG est le premier test essentiel, mais l’absence de résultats ne peut être invoquée pour exclure l’hyperkaliémie.
– Du gluconate de calcium à 10% peut être administré pour la stabilisation membranaire, sauf si le patient est en arrêt cardiaque, dans lequel 10 mL de chlorure de calcium doivent être administrés.
Références / Lectures complémentaires:
- Faridi AB, Weisberg LS. Anomalies acido-basiques, électrolytiques et métaboliques. Dans: Médecine des soins intensifs: Principes de diagnostic et de prise en charge chez l’adulte. Parrillo JE, Dellinger RP (Dir.). Troisième édition. Philadelphie, Elsevier, 2008; 1203-1243.
- Mount DB, Zandi-Nejad K. Troubles de l’équilibre potassique. Dans: Brenner et Rector’s The Kidney, 9e Éd., WB Saunders & Company, Philadelphie 2011. p. 640.
- Marron RS. Homéostasie potassique et implications cliniques. Am J Med.1984 5 novembre; 77(5A): 3-10.
- Rein International 2016; 89:546-554.
- Weisberg LS. Prise en charge de l’hyperkaliémie sévère. Soins Critiques Med. 2008;36(12):3246-51.
- Gennari FJ: Troubles de l’homéostasie potassique. Hypokaliémie et hyperkaliémie. Soin Crit Clin 2002;18:273-288
- Stevens MS, Dunlay RW. Hyperkaliémie chez les patients hospitalisés. Int Urol Nephrol 2000; 32:177-180.
- Mandal AK. Hypokaliémie et hyperkaliémie. Med Clin Nord Am. 1997;81(3):611-639.
- Fisch C. Relation des perturbations électrolytiques aux arythmies cardiaques. Circulation 1973; 47:408-419.
- Surawicz B. Les électrolytes et l’électrocardiogramme. Postgrad Med 1974; 55:123–129.
- Freeman K, Feldman JA, Mitchell P, et al. Effets de la présentation et de l’électrocardiogramme à temps pour le traitement de l’hyperkaliémie. Acad Emerg Med. 2008 Mars; 15(3): 239-49.
- Mattu A, Brady WJ, Robinson D. Manifestations électrocardiographiques de l’hyperkaliémie. Am J Emerg Med. 2000; 18: 721–729.
- Dodge HT, Grant RP, Seavey PW. L’effet de l’hyperkaliémie induite sur l’électrocardiogramme normal et anormal. Am Heart J.1953 Mai; 45 (5): 725-40.
- Wrenn KD, Slovis CM, Slovis BS. La capacité des médecins à prédire l’hyperkaliémie à partir de l’ECG. Ann Emerg Med. 1991 Nov; 20 (11): 1229-32.
- Szerlip HM, Weiss J, Singer I. Hyperkaliémie profonde sans manifestations électrocardiographiques. Je suis Malade des reins. 1986 Juin; 7(6): 461-5.
- Montague BT, Ouellette JR, Buller GK. Examen rétrospectif de la Fréquence des changements ECG dans l’hyperkaliémie. Journal clinique de la Société américaine de Néphrologie : CJASN. 2008;3(2):324-330.
- Chamberlain M. Traitement d’urgence de l’hyperkaliémie. Lancet. 1964;1:464–467.
- Bisogno JL, Langley A, Von Dreele MM. Effet du calcium pour inverser les effets électrocardiographiques de l’hyperkaliémie dans le cœur de rat isolé: Une étude prospective dose-réponse. Crit Care Med 1994; 22:697-704.
- Martin T, Kang Y, Robertson K, et al. Ionisation et effets hémodynamiques du chlorure de calcium et du gluconate de calcium en l’absence de fonction hépatique. Anesthésie 1990; 73:62-5.
- Davey M, Caldicott D. Sels de calcium dans la gestion de l’hyperkaliémie. Journal de médecine d’urgence: EMJ. 2002;19(1):92-93.
- Cote CJ, Drop LJ, Daniels AL, et al. Chlorure de calcium versus gluconate de calcium: comparaison de l’ionisation et des effets cardiovasculaires chez les enfants et les chiens. Anesthésiologie 1987; 66:465-70.
- Ballantyne F III, Davis LD, Reynolds EW Jr, et al. Base cellulaire pour l’inversion des changements électrocardiographiques hyperkaliémiques par le sodium. Am J Physiol 1975; 229:935-940.
- Batterink J, Cessford TA, Taylor RAI. Interventions pharmacologiques pour la prise en charge aiguë de l’hyperkaliémie chez l’adulte. Base de données Cochrane des revues systématiques 2015, numéro 10. Art. Aucun.: CD010344. DOI: 10.1002/14651858.CD010344.pub2.
- Mahoney BA, Smith WA, Lo DS, et al. Interventions d’urgence pour l’hyperkaliémie. Cochrane Database Syst Rev. 2005 18 avril; (2): CD003235.
- Elliott MJ, Ronksley PE, Clase CM, et al. Prise en charge des patients atteints d’hyperkaliémie aiguë. 2010;182:1631–1635.
- Harel Z, Kamel KS. Dose optimale et Méthode d’administration de l’insuline intraveineuse dans la prise en charge de l’Hyperkaliémie d’urgence: Une revue systématique. Barretti P, éd. PLoS UN. 2016; 11(5): e0154963.
- Ho K. Une réponse extrêmement rapide: transport du potassium et du glucose stimulés par l’insuline dans le muscle squelettique. Clin J Am Soc Néphrol. 2011;6:1513–1516.
- Soar J, Perkins GD, Abbas G, et al. Lignes Directrices du Conseil Européen de Réanimation pour la réanimation 2010 Section 8. Arrêt cardiaque dans des circonstances particulières: anomalies électrolytiques, empoisonnement, noyade, hypothermie accidentelle, hyperthermie, asthme, anaphylaxie, chirurgie cardiaque, traumatisme, grossesse, électrocution. Réanimation. 2010;81:1400–1433.
- Vanden Hoek TL, Morrison LJ, Shuster M, et al. Partie 12: arrêt cardiaque dans des situations spéciales: Lignes directrices 2010 de l’American Heart Association pour la Réanimation cardiopulmonaire et les soins cardiovasculaires d’urgence. Circulation. 2010;122 (complément 3): S829-S861.
- Li Q, Zhou MT, Wang Y, et al. Effet de l’insuline sur l’hyperkaliémie au stade anhépatique de la transplantation hépatique. World J Gastroenterol 2004; 10:2427-9.
- Allon M, Copkney C. Albuterol et insuline pour le traitement de l’hyperkaliémie chez les patients hémodialysés. Rein Int 1990; 38 (5): 869-72.
- Allon M, Shanklin N. Effet de l’administration de bicarbonate sur le potassium plasmatique chez les patients dialysés: interactions avec l’insuline et l’albutérol. Am J Rein Dis 1996; 28:508-14.
- Mahajan SK, Mangla M, Kishore K. Comparaison des perfusions d’aminophylline et d’insuline-dextrose dans le traitement aigu de l’hyperkaliémie dans la maladie rénale terminale J Assoc Physicians India 2001; 49: 1082-5.
- Ngugi NN, McLigeyo SO, Kayima JK. Traitement de l’hyperkaliémie en modifiant le gradient transcellulaire chez les patients atteints d’insuffisance rénale: effet de diverses thérapies East Afr Med J 1997; 74: 503-9.
- Schafers S, Naunheim R, Vijayan A, et al. Incidence de l’hypoglycémie après stabilisation aiguë à base d’insuline du traitement de l’hyperkaliémie. J Hosp Med. 2012;7(3):239-242.
- Apel J, Reutrakul S, Baldwin D. Hypoglycémie dans le traitement de l’hyperkaliémie par l’insuline chez les patients atteints d’insuffisance rénale terminale. Clin Rein J. 2014; 7 (3): 248-250.
- Goldfarb S, Cox M, Singer I, et al. Hyperkaliémie aiguë induite par l’hyperglycémie: mécanismes hormonaux. Ann Stagiaire Med. 1976;84:426–432.
- Palmer BF. Régulation de l’homéostasie potassique. Clin J Am Soc Néphrol. 2015;10:1050–1060.
- Clausen T, Everts ME. Régulation de la pompe Na, K dans le muscle squelettique. Rein Int 1989; 35:1-13.
- Moratinos J, Reverte M. Effets des catécholamines sur le potassium plasmatique: le rôle des récepteurs alpha et bêta-adrénergiques. Fundam Clin Pharmacol. 1993;7(3-4):143-53.
- Allon M. Hyperkaliemia in end-stage renal disease: mechanisms and management. J Am Soc Nephrol 1995; 6:1134.
- Allon M, Dunlay R, Copkney C. albutérol nébulisé pour l’hyperkaliémie aiguë chez les patients sous hémodialyse. Ann Stagiaire Med. 1989;110:426-9.
- Allon M, Shanklin N. Effect of albuterol treatment on subsequent dialytic potassium removal. Am J Rein Dis 1995; 26:607-13.
- Blumberg A, Weidmann P, Shaw S, et al. Effect of various therapeutic approaches on plasma potassium and major regulating factors in terminal renal failure. Journal américain de médecine. 1988;85(4):507–12.
- Iqbal Z, Friedman EA. Preferredthérapie de l’hyperkaliémie dans l’insuffisance rénale: enquête sur la formation en néphrologie – programme N Engl J Med. 1989 Jan 5; 320(1):60-1.
- Blumberg A, Weidmann P, Ferrari P. Effet de l’administration prolongée de bicarbonate sur le potassium plasmatique dans l’insuffisance rénale terminale. Rein Int. 1992;41:369–374.
- Fraley DS, Adler S. Correction de l’hyperkaliémie par le bicarbonate malgré un pH sanguin constant. Rein Int. 1977 Nov; 12(5): 354-60.
- Gutierrez R, Schlessinger F, Oster JR, et al. Effect of hypertonic versus isotonic sodium bicarbonate on plasma potassium concentration in patients with end-stage renal disease. Metab électrolyte mineur. 1991;17(5):297-302.
- Jentzer JC, DeWald TA, Hernandez AF. Combinaison de diurétiques de l’anse avec des diurétiques de type thiazidique dans l’insuffisance cardiaque. Je Suis Coll Cardiol. 2010 Nov 2; 56 (19): 1527-34.
- Scherr L, Ogden DA, Hydromel AW, et al. Prise en charge de l’hyperkaliémie avec une résine échangeuse de cations. N Engl J Med 1961; 264:115-119.
- Flinn RB, Merrill JP, Welzant WR, et al. Traitement du patient oligurique avec une nouvelle résine échangeuse de sodium et du sorbitol; un rapport préliminaire. En anglais J Med. 19 janvier 1961; 264:111-5.
- Sterns RH, Rojas M, Bernstein P, et al. Résines échangeuses d’ions pour le traitement de l’hyperkaliémie: sont-elles sûres et efficaces? Je Suis Soc Néphrol. 2010 Mai; 21(5): 733-5.
- Beccari MV, Meaney CJ. Utilité clinique du patiomère, du cyclosilicate de zirconium de sodium et du polystyrène sulfonate de sodium pour le traitement de l’hyperkaliémie: une revue fondée sur des preuves. Preuves fondamentales. 2017;12:11-24.
- Weir MA, Juurlink DN, Gomes T, et al. Les bêta-bloquants, le triméthoprime sulfaméthoxazole et le risque d’hyperkaliémie nécessitant une hospitalisation chez les personnes âgées: une étude cas-témoins imbriquée. Clin J Am Soc Néphrol. 2010;5:1544–1551.
- Huang I. RLY5016: un nouveau polymère thérapeutique non absorbé pour le contrôle du potassium sérique. Je Suis Soc Néphrol. 2010; 21:482A-483A.
- Bakris GL, Pitt B, Weir MR, et al, pour les enquêteurs de l’AMÉTHYSTE-DN. Effet du patiromer sur le taux de potassium sérique chez les patients présentant une hyperkaliémie et une maladie rénale diabétique: l’essai clinique randomisé AMETHYST-DN. JAMA. 2015;314:151–161.
- Montaperto AG, Gandhi MA, Gashlin LZ, et al. Patiromer: une revue clinique. Curr Med Res Opin. 2016;32(1):155-64.
- Packham DK, Kosiborod M. Pharmacodynamics and pharmacocinetics of sodium zirconium cyclosilicate in the treatment of hyperkaliemia. Médicament expert Opin Metab Toxicol. 2016 Mai; 12 (5): 567-73.
- Ash SR, Singh B, Lavin PT, et al. Une étude de phase 2 sur le traitement de l’hyperkaliémie chez les patients atteints d’insuffisance rénale chronique suggère que le piège à potassium sélectif, ZS-9, est sûr et efficace. Rein Int. 2015;88:404–411.
- Packham DK, Rasmussen HS, Lavin PT, et al. cyclosilicate de zirconium de sodium dans l’hyperkaliémie. En anglais J Med. 2015;372:222–231.
- Meaney CJ, Beccari MV, Yang Y, et al. Revue systématique et Méta-Analyse du Patiomère et du Cyclosilicate de Zirconium Sodique: Un Nouvel arsenal pour le traitement de l’Hyperkaliémie. 2017 Avril; 37 (4): 401-411.
- Blumberg A, Roser HW, Zehnder C, et al. Potassium plasmatique chez les patients présentant une insuffisance rénale terminale pendant et après l’hémodialyse; relation avec l’élimination dialytique du potassium et le potassium corporel total. Greffe de cadran Néphrol. 1997;12:1629–1634.
- Feig P, Shook A, Sterns R. Effet de l’élimination du potassium pendant l’hémodialyse sur la concentration plasmatique de potassium. Néphron. 1981;27:25–30.
- Gélose BU, Culleton BF, Fluck R, Leypoldt JK. Cinétique du potassium pendant l’hémodialyse. Hémodial Int. 2015;19:23–32.
- Alfonzo AV, Simpson K, Deighan C, Campbell S, Fox J. Modifications to advanced life support in renal failure. Resuscitation 2007;73:12–28.