Autori: Brit Lungo, MD (@long_brit, SAUSHEC EM Medico curante) e Justin R. Warix, FARE, FAAEM (EM Medico curante, Penisola Centrale Ospedale, Soldotna, AK) // Edito da: Alex Koyfman, MD (@EMHighAK, EM Medico curante, UT Southwestern Medical Center / Parkland Memorial Hospital)
bentornato a emDocs Casi! Oggi abbiamo una discussione basata su casi su un argomento principale EM, con uno sguardo ad alcune polemiche e trattamenti all’avanguardia.
—————————-
Una donna di 62 anni con una storia di malattia renale in dialisi, ipertensione e CAD presenta nausea e debolezza. Ha saltato la seduta di dialisi di oggi. Il suo VS sono normali, e il suo esame è anche normale. Qual è il tuo primo test che ottieni?
- L’ECG!
- Qual è la letteratura dietro questo regime? C’è qualcosa di meglio?
- Prima di iniziare, copriamo alcune nozioni di base.
- Gestione
- 1) Stabilizzazione della membrana cardiaca
- 2) Spostamento transcellulare
- Trattamento di combinazione
- 3) Escrezione di potassio
- Cosa succede in arresto cardiaco a causa di iperkaliemia?
- Punti chiave
- Riferimenti / Ulteriori letture:
L’ECG!
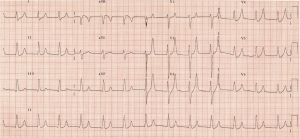
Vedete grandi onde T con picco con assenza di onde P. Il VBG ritorna con potassio di 7,3 mmol / L, con sodio 140 mmol / L e lattato normale. Chiedi il tuo regime di iperkaliemia standard, o C BIG K DROP – vedi di più da https://canadiem.org/tiny-tip-hyperkalemia-management/
Questo regime è classicamente costituito da calcio (gluconato o sale cloruro), Beta agonista (10-20 mg albuterolo nebulizzato) e/o bicarbonato (1 amp), Insulina (10 unità regolari/Glucosio D50 1 amp), Kayexalato (15-30 g orale o rettale), Diuretici (Furosemide 40 mg), e Del paziente.
Qual è la letteratura dietro questo regime? C’è qualcosa di meglio?
Prima di iniziare, copriamo alcune nozioni di base.
– I cambiamenti in questi livelli influenzano i potenziali della membrana cellulare e provocano sintomi cardiaci e neuromuscolari. La pompa Na-K-ATPasi svolge un ruolo importante nel gradiente della membrana cellulare.
– Iperkaliemia lieve: 5,5-6,5 mEq / L (vicino al 10% dei pazienti ricoverati).4-7
– I livelli moderati sono 6.5-7.5 mEq/L e severo > 7.5 mEq/L. 4-7
Eziologia: Le cause di potassio elevato includono: excessive exogenous potassium, excessive endogenous potassium (hemolysis, rhabdomyolysis, burns, tumor lysis syndrome, trauma), redistribution (acidemia, medications (succinylcholine, beta-blockers), and insulin deficiency), decrease in excretion (renal failure/injury, decreased mineral corticoids, medications), factitious (hemolysis, thrombocytosis, venipuncture issue, leukocytosis).5-8
Clinical Manifestations: Since potassium plays an important role in Na-K-ATPase physiology, hyperkalemia can result in several important effects, primarily cardiac and neuromuscular. Tuttavia, le caratteristiche cliniche sono aspecifiche e includono debolezza generale, letargia o confusione. I riflessi tendinei profondi possono essere depressi o assenti, sebbene i nervi cranici, la funzione del diaframma e la sensazione siano in genere normali. Gli effetti GI includono nausea, vomito e diarrea.
– L’ECG è uno dei test diagnostici più importanti nell’iperkaliemia. I cambiamenti previsti sono classicamente pensati per seguire 1) Onde T con picco, 2) Prolungamento dell’intervallo PR con perdita di onda p, 3) Allargamento QRS, 4) Modello di onda sinusoidale e 6) Asistolia. Le onde T con picco sono il risultato di cambiamenti potenziali di membrana a riposo.9-12
– Queste modifiche non appaiono però in ordine. Dodge et al. i pazienti trovati possono progredire dal ritmo sinusale a V fib.13 ECG dimostra una sensibilità del 34-43% nella previsione dell’iperkaliemia, con specificità dell ‘ 85-86%.12,14
– Una lenta variazione del potassio sierico può non provocare alterazioni dell’ECG e livelli superiori a 9,0 mEq/L possono non dimostrare i risultati attesi.12,15
Il nostro paziente ha presentato debolezza e cambiamenti ECG. Hai chiesto diversi farmaci e iniziamo la nostra profonda immersione nel trattamento dell’iperkaliemia.
Gestione
– Il trattamento non dipende dalla causa dell’iperkaliemia, ma deve concentrarsi sull’inversione o sull’evitare effetti e complicanze aritmiche.
– Stabilire la rete di sicurezza di accesso IV, monitoraggio continuo, e O2.
– La gestione si concentra sulla stabilizzazione cardiaca, sullo spostamento transcellulare e sull’escrezione di potassio. Questo deve iniziare immediatamente una volta che si sospetta iperkaliemia, sia da cambiamenti ECG (comprese le onde T con picco) o da potassio > 6,5 mmol / L. 4,5,10,11,16

1) Stabilizzazione della membrana cardiaca
Il calcio diminuisce l’effetto di depolarizzazione dell’iperkaliemia e riduce il potenziale di soglia dei miociti cardiaci in pochi minuti.4,5,17-19 Questo stabilizza la membrana cellulare cardiaca, ma non provoca spostamento transcellulare o escrezione di potassio, che richiede altri farmaci.
– Il calcio può essere somministrato in due forme: sale di cloruro o gluconato. Il sale di cloruro di Ca contiene 13,6 meq in 10 ml, mentre il sale di gluconato di Ca contiene 4,6 meq in 10 ml.4,5,18,19 Ca gluconato può essere somministrato attraverso una linea IV periferica. Lo stravaso di cloruro di Ca può causare necrosi tissutale e, se possibile, si raccomanda la linea centrale (a meno che non si verifichi una situazione di codice.) 4,5
– CaCl 1 g contiene circa 270 mg di Ca2+, mentre 3 fiale di gluconato di calcio contiene la quantità equivalente (circa 90 mg di Ca2+ per fiala).18,19
– La letteratura suggerisce che il gluconato di Ca ha un tempo di insorgenza simile a quello del cloruro di Ca e potrebbe non richiedere attività epatica. Diversi studi condotti in pazienti sottoposti a trapianto di fegato dimostrano un aumento simile della Ca dopo entrambe le formulazioni.19-21 Uno studio condotto su cani e pazienti pediatrici dimostra risultati simili.21
Bottom Line: 1g (10 mL) Ca gluconato IV deve essere fornito ai pazienti con risultati ECG (onde T con picco o peggio), con rivalutazione entro 5 minuti. Deve essere fornito più calcio se non si osservano cambiamenti o peggioramenti nell’ECG. Un paziente in arresto cardiaco o con accesso centrale deve essere somministrato 1 g di Ca cloruro IV.
Esiste un’altra opzione per la stabilizzazione cardiaca? La soluzione salina ipertonica (3%) può essere utilizzata in boli da 100 ml, sebbene questo sia stato studiato prevalentemente in pazienti con iponatriemia e iperkaliemia.22
2) Spostamento transcellulare
Questo deve avvenire con o immediatamente dopo il calcio al fine di ridistribuire il potassio.4,5,23-25

A) Insulina e glucosio – Queste misure riducono il potassio sierico in modo dose-dipendente.4,5,23-26 L’attivazione di Na-K-ATPasi e il reclutamento intracellulare della pompa (recettori GLUT4) alla membrana cellulare sono responsabili del trasporto intracellulare di K.27
– Classicamente, viene fornita insulina regolare 10-20 unità, con destrosio 25 g (un amp di D50) se i livelli di glucosio nel sangue sono inferiori a 250 mg/dL.4,5,28,29
– L’insulina e il glucosio diminuiscono il potassio di 0,45-0,61 mmol / L entro 15 minuti, 30-32 0.87 mmol / L a 30 minuti, 33, 34 e 0,47 mmol / L a un’ora.23,24,33,34 Altri studi suggeriscono che può provocare una diminuzione fino a 1,2 mmol / L. 23,24
– L’insulina / glucosio ha inizio d’azione meno di 15 minuti (più comunemente 5-10 minuti) e il tempo di azione massima 25-30 minuti.23,24 La durata dell’azione è di 2 ore.
– La quantità di glucosio da fornire può essere difficile da determinare e la tabella 1 seguente offre un mezzo facile da seguire per determinare ciò che dovrebbe essere fornito.
– I fattori includono assenza di diabete precedente, assenza di farmaci diabetici e riduzione del glucosio prima del trattamento. La lesione renale o la malattia è un fattore potenziale, poichè l’insulina è metabolizzata renalmente.4,5,36
– Un potenziale cambiamento include l ‘ uso di insulina ad azione breve, come lispro o aspart, che possiedono emivita più breve, sono assorbite più rapidamente e non sono prolungate in caso di insufficienza/lesione renale. Questo può essere fornito come bolo di insulina ad azione breve di sole 10 unità, oppure come bolo di 6 unità seguito da 20 unità / ora di infusione di lispro o aspart. Questi regimi forniscono diminuzioni simili nel potassio sierico mentre con conseguente meno ipoglicemia.4,5
– Il glucosio solo non è raccomandato, che può provocare ipertonicità e iperkaliemia.37,38
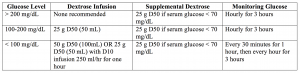
Bottom Line: insulina ad azione breve 10 unità IV, con infusione di glucosio come sopra.

B) Beta agonisti – catecolamine aumentare l’attività della pompa Na-K-ATPasi e il cotransporter Na-K-2Cl.1-5,39,40
– L’albuterolo nebulizzato viene somministrato in dosi di 10-20 mg, piuttosto che il normale 5 mg per la malattia ostruttiva.
– Levalbuterolo e albuterolo dimostrano pari capacità di diminuire il potassio.4,5,23,24
-Albuterolo può essere somministrato IV in dosi di 0,50 mg e terbutalina può essere somministrata IM in dosi di 0,25 mg. 4,5,23,24,31,41-43
– Il potassio diminuisce di 0,6 mmol / L con 10 mg e 1,0 mmol / L con 20 mg in un’ora.31,41-43
– L’esordio è di 20-30 minuti, con durata superiore a due ore.31,41-43
– Le formulazioni IV includono epinefrina, albuterolo 0,5 mg o salbutamolo 2,5 mg, anche se gli effetti collaterali sono più comuni.23,24,34
– Gli effetti collaterali includono tremore, palpitazioni e ansia. Le forme IV hanno un maggiore rischio di aumento della pressione sanguigna e mal di testa.
Linea di fondo: Albuterolo 20 mg in soluzione salina normale da 4 mL nebulizzata per 10 minuti.

C) Bicarbonato di sodio – bolo il bicarbonato di sodio è stato raccomandato per il trattamento acuto dell’iperkaliemia, sulla base di studi che valutano l’infusione prolungata di bicarbonato (oltre le ore).23,24,31,32,44-46
– Tuttavia, la letteratura in pazienti con pH normale non supporta il bicarbonato per l’iperkaliemia.4,5,23,24
Trattamento di combinazione
– L’uso di più agenti fornisce il miglior mezzo di ridistribuzione del potassio, con Cochrane review che raccomanda insulina combinata, glucosio e beta agonisti.4,5,23-26
– Allon et al. trova la massima diminuzione del potassio di 1,21 mmol / L con glucosio di insulina IV con albuterolo nebulizzato.31
– Il bicarbonato non deve essere usato a meno che il paziente non sia acidemico.4,5
Bottom Line: il bicarbonato di sodio può essere utilizzato in pazienti con acidemia e iperkaliemia, ma non è utile in altri pazienti. La terapia di combinazione è efficace con beta agonista e insulina / glucosio nello spostamento del potassio.
Il glucosio del paziente è 153. Si dà gluconato di calcio 10% 10 mL IV, seguito da 10 unità di insulina a breve durata d’azione con un amp D50 e 20 mg albuterolo nebulizzato. Qual è il tuo prossimo passo?
3) Escrezione di potassio
I mezzi di escrezione includono urina, sistema GI e sangue.1-5 Reni sono la via predominante di escrezione. I medici devono valutare lo stato del volume del paziente e la capacità di produrre urina. Se il paziente può produrre urina, un diuretico è un’opzione valida.4,5 Tuttavia, l’emodialisi è il miglior mezzo per la rimozione definitiva del potassio.

A) Diuresi urinaria – Questo può essere usato durante la preparazione del paziente per l’emodialisi. La diuresi urinaria non è utile se il paziente non può produrre urina, sebbene possa essere utile nei pazienti con funzionalità renale moderatamente compromessa.4,5
– I diuretici dell’ansa come la furosemide forniscono la massima escrezione urinaria di potassio.

B) GI – Sono disponibili diverse opzioni, con diversi nuovi agenti che offrono opzioni migliori di Kayexalate.
– Sodio polistirene solfonato (SPS), o Kayexalato, è una resina a scambio ionico che scambia sodio per ammonio, calcio, magnesio e potassio per consentire l’eliminazione del potassio attraverso le feci.4,5,23-26 Purtroppo, la letteratura dietro SPS è estremamente debole, con recenti studi e recensioni Cochrane raccomandando contro il suo uso.50,51 Questo farmaco fornisce un carico di sodio mentre pone il paziente a rischio di stitichezza, ostruzione e, peggio ancora, ischemia intestinale e necrosi. Il farmaco possiede anche un avvertimento scatola nera dalla FDA.4,5,23,24,52 Per ulteriori informazioni, vedere http://www.emdocs.net/skeptical-em-myths-evidence/ e http://rebelem.com/kayexalate-useful-treatment-hyperkalemia-emergency-department/
– Patiromer è un polimero sintetico costituito da perline sferiche non assorbibili.52,53 L’inizio dell’azione del farmaco è 7-48 ore, con durata dell’effetto 12-24 ore. 52-54 Volontari sani dimostrano una diminuzione del potassio dose-correlata di 15-20 mmol.55-57 Dosi di 15-30 g/die sembrano efficaci. L’effetto indesiderato più comune include ipomagnesiemia (8,6%), sebbene non siano state riscontrate aritmie cardiache in quei pazienti. Da notare, il farmaco possiede un avvertimento scatola nera per la separazione di almeno sei ore da altri farmaci orali.4
– Il ciclosilicato di zirconio di sodio (ZS-9) è un polimero sintetico costituito da perline sferiche non assorbibili.53,54 Il farmaco si lega più di nove volte la quantità di potassio rispetto a SPS, poiché un poro legante all’interno della struttura cristallina si lega specificamente al potassio.L’inizio di azione di 143,149 ZS-9 è di 1-6 ore, con la durata di effetto 4-12 ore. Diversi studi supportano il suo uso, con 10g / die che diminuisce il potassio di 0,4 mmol / L a un’ora e 0,7 mmol/L a 4 ore.58-60
– Una meta-analisi ha confrontato patiromer e ZS-9, trovando patiromer diminuisce il potassio di 0,36 mEq/L entro il giorno 3 del trattamento.61 ZS – 9 dimostra una diminuzione di 0,17 mEq/L a un’ora e 0,67 mEq / L a 2 giorni.61

C) Dialisi – Questo è il modo più efficace per rimuovere il potassio, con il potassio che diminuisce di 1 mmol/L a 1 ora e 2 mmol/L per 2-3 ore. Il dializzato di potassio più basso e il flusso sanguigno aumentato possono provocare le diminuzioni più rapide del potassio sierico.4,5
– Gli aumenti della velocità della pompa del sangue della macchina e della concentrazione da plasma a dializzato possono diminuire il potassio in pochi minuti; quindi l’importanza della dialisi (specialmente nell’arresto cardiaco).4,5,41
– L’iperkaliemia di rimbalzo può essere osservata dopo dialisi, probabilmente correlata ai livelli di potassio predialisi.4,5
– L’emodialisi deve essere considerata precocemente nei pazienti con insufficienza renale diagnosticata, incapacità di produrre urina, iperkaliemia resistente ad altri trattamenti, arresto cardiaco e marcata distruzione tissutale.62-64
Linea di fondo: La dialisi è più efficace nella rimozione definitiva del potassio. L’SPS non è efficace e deve essere evitato a causa del rischio di necrosi del colon.
Chiami il nefrologo riguardo alla dialisi e ripeti un ECG, che dimostra il normale ritmo sinusale con velocità 72 bpm. Il nefrologo afferma che sarà proprio giù per vedere il paziente.
Cosa succede in arresto cardiaco a causa di iperkaliemia?
L’iperkaliemia altera il potenziale di riposo dei cardiomiociti, con conseguente inattivazione dei canali del sodio e blocco della conduzione. I pazienti in arresto a causa di iperkaliemia richiedono compressioni immediate e misure ACLS.28,29
– I pazienti con arresto cardiaco con anamnesi di insufficienza renale nota, malattia critica o in emodialisi giustificano una rapida valutazione dei gas ematici che misurano il potassio.
– Il bicarbonato di sodio può essere fornito come 1 amp.
– Una volta che l’iperkaliemia è confermata su VBG o altri test di laboratorio, l’emodialisi è essenziale.
Punti chiave
– Il potassio svolge un ruolo chiave nella fisiologia e si trova prevalentemente intracellulare. L’iperkaliemia provoca cambiamenti nei potenziali della membrana cellulare, principalmente nelle cellule cardiache e neuromuscolari.
– L’ECG è il primo test essenziale, ma l’assenza di risultati non può essere invocata per escludere l’iperkaliemia.
– La gestione include la stabilizzazione della membrana cardiaca, lo spostamento transcellulare e l’escrezione.
– Gluconato di calcio 10% può essere somministrato per la stabilizzazione della membrana a meno che il paziente non sia in arresto cardiaco, in cui devono essere somministrati 10 ml di cloruro di calcio.
– I beta agonisti e l’insulina ad azione breve con glucosio sono efficaci nello spostamento intracellulare del potassio. L’infusione di destrosio deve essere fornita in base al glucosio sierico.
– L’escrezione comprende diuresi urinaria, eliminazione GI ed emodialisi.
– La dialisi è il mezzo ultimo per rimuovere il potassio. Ringer lattati e plasmalyte possono essere più sicuri per la reidratazione dei liquidi, se necessario.
Riferimenti / Ulteriori letture:
- Faridi AB, Weisberg LS. Anomalie acido-base, elettrolitiche e metaboliche. In: Medicina Critica: Principi di diagnosi e gestione negli adulti. Parrillo JE, Dellinger RP (a cura di). Terza edizione. Filadelfia, Elsevier, 2008;1203-1243.
- Mount DB, Zandi-Nejad K. Disturbi dell’equilibrio del potassio. In: Brenner e Rector’s The Kidney, 9th Ed, WB Saunders & Company, Philadelphia 2011. pag. 640.
- Marrone RS. Omeostasi del potassio e implicazioni cliniche. Sono J Med.1984 Novembre 5; 77 (5A): 3-10.
- Rene internazionale 2016;89:546-554.
- Weisberg LS. Gestione dell’iperkaliemia grave. Crit Cura Med. 2008;36(12):3246-51.
- Gennari FJ: Disturbi dell’omeostasi del potassio. Ipopotassiemia e iperkaliemia. Crit Cura Clin 2002;18:273-288
- Stevens MS, Dunlay RW. Iperkaliemia nei pazienti ospedalizzati. Int Urol Nephrol 2000; 32: 177-180.
- Mandal AK. Ipopotassiemia e iperkaliemia. Med Clin Nord Am. 1997;81(3):611-639.
- Fisch C. Relazione dei disturbi elettrolitici alle aritmie cardiache. Circolazione 1973; 47: 408-419.
- Surawicz B. Elettroliti ed elettrocardiogramma. Postgrad Med 1974; 55:123–129.
- Freeman K, Feldman JA, Mitchell P, et al. Effetti della presentazione e dell’elettrocardiogramma in tempo per il trattamento dell’iperkaliemia. Acad Emerg Med. 2008 Mar; 15 (3): 239-49.
- Mattu A, Brady WJ, Robinson D. Manifestazioni elettrocardiografiche di iperkaliemia. Am J Emerg Med. 2000; 18: 721–729.
- Dodge HT, Grant RP, Seavey PW. L’effetto dell’iperkaliemia indotta sull’elettrocardiogramma normale e anormale. Am Cuore J. 1953 maggio; 45 (5): 725-40.
- Wrenn KD,Slovis CM, Slovis BS. La capacità dei medici di prevedere l’iperkaliemia dall’ECG. Ann Emerg Med. 1991 Novembre; 20 (11): 1229-32.
- Szerlip HM,Weiss J, Singer I. Iperkaliemia profonda senza manifestazioni elettrocardiografiche. Am J Rene Dis. 1986 Giugno; 7(6): 461-5.
- Montague BT, Ouellette JR, Buller GK. Revisione retrospettiva della frequenza dei cambiamenti ECG nell’iperkaliemia. Rivista clinica della Società Americana di Nefrologia: CJASN. 2008;3(2):324-330.
- Chamberlain M. Trattamento di emergenza dell’iperkaliemia. Lancet. 1964;1:464–467.
- Bisogno JL, Langley A, Von Dreele MM. Effetto del calcio per invertire gli effetti elettrocardiografici dell’iperkaliemia nel cuore isolato del ratto: uno studio prospettico dose-risposta. Crit Cura Med 1994; 22:697-704.
- Martin T, Kang Y, Robertson K, et al. Ionizzazione ed effetti emodinamici del cloruro di calcio e del gluconato di calcio in assenza di funzionalità epatica. Anestesia 1990; 73: 62-5.
- Davey M, Caldicott D. Sali di calcio nella gestione dell’iperkaliemia. Rivista di medicina di emergenza: EMJ. 2002;19(1):92-93.
- Cote CJ, Drop LJ, Daniels AL, et al. Cloruro di calcio contro gluconato di calcio: confronto tra ionizzazione ed effetti cardiovascolari nei bambini e nei cani. Anestesiologia 1987; 66: 465-70.
- Ballantyne F III, Davis LD, Reynolds EW Jr, et al. Base cellulare per l’inversione dei cambiamenti elettrocardiografici iperkalemici da parte del sodio. Am J Physiol 1975; 229: 935-940.
- Batterink J, Cessford TA, Taylor RAI. Interventi farmacologici per la gestione acuta dell’iperkaliemia negli adulti. Cochrane Database of Systematic Reviews 2015, Issue 10. Arte. No.: CD010344. DOI: 10.1002 / 14651858.CD010344. pub2.
- Mahoney BA, Smith WA, Lo DS, et al. Interventi di emergenza per iperkaliemia. Cochrane Database Syst Rev. 2005 Aprile 18; (2): CD003235.
- Elliott MJ, Ronksley PE, Clase CM, et al. Gestione di pazienti con iperkaliemia acuta. 2010;182:1631–1635.
- Harel Z, Kamel KS. Dose ottimale e metodo di somministrazione di insulina endovenosa nella gestione dell’iperkaliemia di emergenza: una revisione sistematica. Barretti P, ed. PLoS UNO. 2016; 11(5): e0154963.
- Ho K. Una risposta criticamente rapida: potassio stimolato dall’insulina e trasporto del glucosio nel muscolo scheletrico. Clin J Am Soc Nephrol. 2011;6:1513–1516.
- Soar J, Perkins GD, Abbas G, et al. European Resuscitation Council Guidelines for Resuscitation 2010 Sezione 8. Arresto cardiaco in circostanze particolari: anomalie elettrolitiche, avvelenamento, annegamento, ipotermia accidentale, ipertermia, asma, anafilassi, chirurgia cardiaca, trauma, gravidanza, elettrocuzione. Rianimazione. 2010;81:1400–1433.
- Vanden Hoek TL, Morrison LJ, Shuster M, et al. Parte 12: arresto cardiaco in situazioni speciali: 2010 Linee guida American Heart Association per la rianimazione cardiopolmonare e la cura cardiovascolare di emergenza. Circolazione. 2010;122 (suppl 3): S829-S861.
- Li Q, Zhou MT, Wang Y, et al. Effetto dell’insulina sull’iperkaliemia durante lo stadio anepatico del trapianto di fegato. Mondo J Gastroenterol 2004;10:2427-9.
- Allon M, Copkney C. Albuterolo e insulina per il trattamento dell’iperkaliemia nei pazienti in emodialisi. Rene Int 1990;38(5):869-72.
- Allon M, Shanklin N. Effetto della somministrazione di bicarbonato sul potassio plasmatico nei pazienti in dialisi: interazioni con insulina e albuterolo. Am J Rene Dis 1996; 28: 508-14.
- Mahajan SK, Mangla M, Kishore K. Confronto delle infusioni di aminofillina e insulina–destrosio nella terapia acuta dell’iperkaliemia nella malattia renale allo stadio terminale J Assoc Physicians India 2001; 49: 1082-5.
- Ngugi NN, McLigeyo SO, Kayima JK. Trattamento dell’iperkaliemia alterando il gradiente transcellulare in pazienti con insufficienza renale: effetto di vari terapeutici East Afr Med J 1997; 74: 503-9.
- Schafers S, Naunheim R, Vijayan A, et al. Incidenza di ipoglicemia a seguito di stabilizzazione acuta a base di insulina del trattamento iperkaliemia. J Hosp Med. 2012;7(3):239-242.
- Apel J, Reutrakul S, Baldwin D. Ipoglicemia nel trattamento dell’iperkaliemia con insulina in pazienti con malattia renale allo stadio terminale. Clin Rene J. 2014;7(3):248-250.
- Goldfarb S, Cox M, Singer I, et al. Iperkaliemia acuta indotta da iperglicemia: meccanismi ormonali. Ann Stagista Med. 1976;84:426–432.
- Palmer BF. Regolazione dell’omeostasi del potassio. Clin J Am Soc Nephrol. 2015;10:1050–1060.
- Clausen T, Everts ME. Regolazione della Na, K-pompa nel muscolo scheletrico. Rene Int 1989; 35:1-13.
- Moratinos J, Reverte M. Effetti delle catecolamine sul potassio plasmatico: il ruolo di alfa e beta-adrenocettori. Fundam Clin Pharmacol. 1993;7(3-4):143-53.
- Allon M. Iperkaliemia nella malattia renale allo stadio terminale: meccanismi e gestione. J Am Soc Nephrol 1995; 6: 1134.
- Allon M, Dunlay R, Copkney C. Albuterolo nebulizzato per iperkaliemia acuta in pazienti in emodialisi. Ann Stagista Med. 1989;110:426-9.
- Allon M, Shanklin N. Effetto del trattamento con albuterolo sulla successiva rimozione dialitica del potassio. Am J Rene Dis 1995;26:607-13.
- Blumberg A, Weidmann P, Shaw S, et al. Effetto di vari approcci terapeutici sul potassio plasmatico e sui principali fattori regolatori nell’insufficienza renale terminale. American Journal of Medicine. 1988;85(4):507–12.
- Iqbal Z, Friedman EA. Preferitoterapia dell’iperkaliemia nell’insufficienza renale: indagine sulla formazione nefrologica-programma N Engl J Med. 1989 Gen 5; 320 (1): 60-1.
- Blumberg A, Weidmann P, Ferrari P. Effetto della somministrazione prolungata di bicarbonato sul potassio plasmatico nell’insufficienza renale terminale. Rene Int. 1992;41:369–374.
- Fraley DS, Adler S. Correzione dell’iperkaliemia mediante bicarbonato nonostante il pH costante del sangue.Rene Int. 1977 Novembre; 12 (5): 354-60.
- Gutierrez R, Schlessinger F, Oster JR, et al. Effetto del bicarbonato di sodio ipertonico rispetto a quello isotonico sulla concentrazione plasmatica di potassio in pazienti con malattia renale allo stadio terminale. Miner Elettrolita Metab. 1991;17(5):297-302.
- Jentzer JC, DeWald TA, Hernandez AF. Combinazione di diuretici dell’ansa con diuretici di tipo tiazidico nell’insufficienza cardiaca. J Am Coll Cardiol. 2010 Novembre 2; 56 (19): 1527-34.
- Scherr L, Ogden DA, Mead AW, et al. Gestione dell’iperkaliemia con una resina a scambio cationico. 1961; 264: 115-119.
- Flinn RB, Merrill JP, Welzant WR, et al. Trattamento del paziente oligurico con una nuova resina a scambio di sodio e sorbitolo; una relazione preliminare. N Ingl J Med. 1961 Gennaio 19; 264: 111-5.
- Sterns RH, Rojas M, Bernstein P, et al. Resine a scambio ionico per il trattamento dell’iperkaliemia: sono sicure ed efficaci? J Am Soc Nephrol. 2010 Maggio; 21(5): 733-5.
- Beccari MV, Meaney CJ. Utilità clinica di patiromer, ciclosilicato di zirconio sodico e solfonato di polistirene sodico per il trattamento dell’iperkaliemia: una revisione basata sull’evidenza. Prove fondamentali. 2017;12:11-24.
- Weir MA, Juurlink DN, Gomes T, et al. Beta-bloccanti, trimetoprim sulfametossazolo e rischio di iperkaliemia che richiede il ricovero in ospedale negli anziani: uno studio caso-controllo nidificato. Clin J Am Soc Nephrol. 2010;5:1544–1551.
- Huang I. RLY5016: un romanzo, non assorbito, polimero terapeutico per il controllo del potassio sierico. J Am Soc Nephrol. 2010;21: 482A–483A.
- Bakris GL, Pitt B, Weir MR, et al, per gli investigatori AMETISTA-DN. Effetto di patiromer sul livello di potassio sierico in pazienti con iperkaliemia e malattia renale diabetica: lo studio clinico randomizzato AMETISTA-DN. JAMA. 2015;314:151–161.
- Montaperto AG, Gandhi MA, Gashlin LZ, et al. Patiromer: una revisione clinica. Curr Med Res Opin. 2016;32(1):155-64.
- Packham DK, Kosiborod M. Farmacodinamica e farmacocinetica del ciclosilicato di zirconio sodico nel trattamento dell’iperkaliemia. Esperto Opin Farmaco Metab Toxicol. 2016 Più; 12 (5): 567-73.
- Ash SR, Singh B, Lavin PT, et al. Uno studio di fase 2 sul trattamento dell’iperkaliemia in pazienti con malattia renale cronica suggerisce che la trappola selettiva del potassio, ZS-9, è sicura ed efficiente. Rene Int. 2015;88:404–411.
- Packham DK, Rasmussen HS, Lavin PT, et al. Ciclosilicato di zirconio di sodio in iperkaliemia. N Ingl J Med. 2015;372:222–231.
- Meaney CJ, Beccari MV, Yang Y, et al. Revisione sistematica e Meta-analisi di Patiromer e ciclosilicato di zirconio sodico: un nuovo Armamentario per il trattamento dell’iperkaliemia. 2017 Aprile;37 (4):401-411.
- Blumberg A, Roser HW, Zehnder C, et al. Potassio plasmatico in pazienti con insufficienza renale terminale durante e dopo emodialisi; relazione con rimozione dialitica del potassio e potassio corporeo totale. Trapianto di Nefrol Dial. 1997;12:1629–1634.
- Feig P, Shook A, Sterns R. Effetto della rimozione del potassio durante l’emodialisi sulla concentrazione plasmatica di potassio. Nefrone. 1981;27:25–30.
- Agar BU, Culleton BF, Fluck R, Leypoldt JK. Cinetica del potassio durante l’emodialisi. Emodial Int. 2015;19:23–32.
- Alfonzo AV, Simpson K, Deighan C, Campbell S, Fox J. Modifications to advanced life support in renal failure. Resuscitation 2007;73:12–28.